Vaikuttavat aineet: flutikasoni (flutikasonipropionaatti)
FLUSPIRAL 50 mcg Paineistettu suspensio inhalaatiota varten
Fluspiral -pakkausselosteita on saatavana seuraaviin pakkauksiin:- FLUSPIRAL 50 mcg Paineistettu suspensio inhalaatiota varten
- Fluspiral 125 mcg Paineistettu inhalaatiosuspensio, Fluspiral 250 mcg Paineistettu inhalaatiosuspensio
- Fluspiral 100 mcg inhalaatiojauhe, Fluspiral 250 mcg inhalaatiojauhe, Fluspiral 500 mcg inhalaatiojauhe,
- FLUSPIRAL 500 mcg / 2 ml Sumutettava suspensio - Nebules
Käyttöaiheet Miksi Fluspiralia käytetään? Mitä varten se on?
Tämä lääke sisältää vaikuttavana aineena flutikasonipropionaattia, joka kuuluu kortikosteroideiksi kutsuttujen lääkkeiden ryhmään.
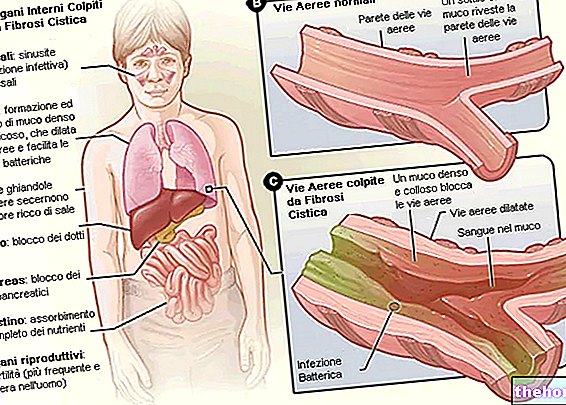
Flutikasonipropionaatti vähentää keuhkojen turvotusta ja tulehdusta (tulehdusta ehkäisevä vaikutus).
Tämä lääke on tarkoitettu astmasairauden ja keuhkoputkentulehduksen hoitoon (keuhkoputken kaliipin väheneminen).
Vasta -aiheet Kun Fluspiralia ei tule käyttää
Älä käytä Fluspiralia
- jos olet allerginen flutikasonipropionaatille tai tämän lääkkeen jollekin muulle aineelle.
Käyttöä koskevat varotoimet Mitä sinun on tiedettävä, ennen kuin otat Fluspiral -valmistetta
Keskustele lääkärin tai apteekkihenkilökunnan kanssa ennen kuin otat Fluspiral -valmistetta.
Ota erityisesti yhteys lääkäriisi, jos:
- sinulla on aktiivinen tai lepotilassa oleva tuberkuloosi (tuberkuloosi, bakteerin aiheuttama tarttuva tauti)
- on diabeetikko
- sinulla on krooninen obstruktiivinen keuhkosairaus (COPD)
- siirtyy oraalisesta steroidihoidosta inhaloitavaan flutikasoniin. Tässä tapauksessa lääkäri hoitaa sinua erityisen huolellisesti, ja hänen on seurattava säännöllisesti lisämunuaisten toimintaa ja lopetettava suun kautta annettava hoito vähitellen inhalaatiohoidon aloittamisen jälkeen. Siksi on suositeltavaa käyttää tunnusta, joka osoittaa, että saatat tarvita hoitoa. kortikosteroidien kanssa stressin aikana.
Jos hengityksesi vaikeutuu (bronkospasmi ja lisääntynyt hengenahdistus) Fluspiralin käytön seurauksena, lopeta lääkkeen käyttö ja ota välittömästi yhteys lääkäriisi.
Yhteisvaikutukset Mitkä lääkkeet tai elintarvikkeet voivat muuttaa Fluspiralin vaikutusta
Kerro lääkärille, sairaanhoitajalle tai apteekkihenkilökunnalle, jos parhaillaan käytät, olet äskettäin käyttänyt tai saatat käyttää muita lääkkeitä.
Kerro erityisesti lääkärille tai apteekkihenkilökunnalle, jos käytät jotakin seuraavista lääkkeistä:
- ritonaviiri, eräänlainen viruslääke, joka tunnetaan proteaasin estäjänä;
- ketokonatsoli, sieni -infektioiden hoitoon käytettävä lääke
Fluspiral ruuan ja juoman kanssa
Voit käyttää Fluspiralia milloin tahansa vuorokauden aikana ruoan kanssa tai ilman.
Varoitukset On tärkeää tietää, että:
Systeemisen kortikosteroidihoidon korvaaminen inhaloitavilla kortikosteroideilla voi laukaista allergisia sairauksia.
Astman hoito on yleensä suoritettava sairauden vakavuuteen mukautetun hoitosuunnitelman puitteissa. lääkärisi on vahvistettava vasteesi hoitoon sekä kliinisesti että keuhkojen toimintakokeilla.
Tarve käyttää lääkkeitä useammin astman oireiden hallitsemiseksi viittaa sairauden hallinnan huonontumiseen; tässä tapauksessa lääkärisi on muutettava hoitosuunnitelmaasi.
Äkillinen astman paheneminen on mahdollisesti hengenvaarallinen, ja tässä tapauksessa lääkärin on harkittava kortikosteroidiannoksen nostamista. Älä lopeta äkillisesti flutikasonipropionaattihoitoa.
Kun käytetään inhaloitavia glukokortikoideja (kuten flutikasonipropionaattia), varsinkin kun niitä määrätään suurina annoksina pitkäksi aikaa, voi esiintyä systeemisiä (koko organismin) vaikutuksia. Näitä vaikutuksia esiintyy vähemmän kuin suun kautta otettavia glukokortikoidihoitoja käytettäessä.
Mahdollisia systeemisiä vaikutuksia ovat Cushingin tauti (kliininen tila, jolle on tunnusomaista liiallinen glukokortikoidien määrä veressä, mikä johtaa lihavuuteen, kasvojen ilmeettömyys, ihon punoitus, laajat venytysmerkit ja paksut hiukset, etenkin kasvoilla), cushingoid -ulkonäkö (tyypillinen ihmisille, joilla on Cushingin tauti), lisämunuaisen vajaatoiminta (lisämunuaisen toiminnan heikkeneminen), kasvun hidastuminen lapsilla ja nuorilla, vähentynyt luun mineraalitiheys, kaihi (silmän sisäisen linssin sameus), glaukooma (vaikea silmäsairaus) ja harvemmin erilaisia psyykkisiä tai käyttäytymisvaikutuksia, mukaan lukien psykomotorinen yliaktiivisuus, ärtyneisyys, unihäiriöt, ahdistuneisuus, masennus tai käyttäytymishäiriöt (erityisesti lapsilla) (ks. kohta 4 "Mahdolliset haittavaikutukset"). Siksi on tärkeää, että inhaloitavan kortikosteroidiannos on pienin mahdollinen jonka kanssa se toimitetaan astman tehokas hallinta säilyi.
On suositeltavaa seurata säännöllisesti inhaloitavilla kortikosteroideilla pitkäaikaishoitoa saavien lasten pituutta.
Jotkut ihmiset voivat olla herkempiä inhaloitavien kortikosteroidien vaikutuksille kuin useimmat potilaat.
Poikia on esiintynyt erittäin harvinaisissa tapauksissa akuutista lisämunuaiskriisistä, kun he ovat altistuneet suositelluille annoksille (noin 1000 mikrogrammaa päivässä) pitkiä aikoja (useita kuukausia tai vuosia).
Raskaus ja imetys
Jos olet raskaana tai imetät, epäilet olevasi raskaana tai jos suunnittelet lapsen hankkimista, kysy lääkäriltä tai apteekista neuvoa ennen tämän lääkkeen käyttöä.
Ajaminen ja koneiden käyttö
Fluspiral ei todennäköisesti vaikuta ajokykyyn tai koneiden käyttökykyyn.
Annos, antotapa ja antamisaika Fluspiralin käyttö: Annostus
Fluspiralia on saatavana kolmessa eri vahvuudessa. Lääkäri päättää, minkä annoksen tarvitset. Käytä tätä lääkettä juuri sen verran kuin lääkäri on määrännyt. Jos olet epävarma, kysy neuvoa lääkäriltä, sairaanhoitajalta tai apteekista.
Tämän lääkkeen käyttö
Aikuiset
Vakioannos on 200 mikrogrammaa vuorokaudessa jaettuna kahteen 100 mikrogramman annokseen. Annosta voidaan nostaa jopa 400 mikrogrammaan päivässä.
Aloitusannosta voidaan myöhemmin säätää, kunnes kontrolli on saavutettu, tai pienentää pienimpään tehokkaaseen annokseen yksilöllisen vasteen mukaan.
Vaikeissa muodoissa enimmäisannos 2000 mikrogrammaa päivässä voi mahdollistaa riittävän taudinhallinnan vähentämällä oraalisten steroidien käyttöä.
Pahenemisten aikana 2000 mikrogramman vuorokausiannokset voivat joissakin tapauksissa korvata oraaliset steroidisyklit.
Lapset (1--4 -vuotiaat)
100 mikrogrammaa kahdesti vuorokaudessa annettuna kasvonaamarilla varustetulla välikelaitteella (lapsilla käytettävä välikelaite).
Yli 4 -vuotiaat lapset
Vakioannos on 100 mikrogrammaa vuorokaudessa jaettuna kahteen 50 mikrogramman annokseen.
Annosta voidaan nostaa jopa 200 mikrogrammaan päivässä.
On suositeltavaa, että steroideilla, mukaan lukien Fluspiral Pressurized Suspension, hoidettujen lasten pituutta lääkäri seuraa säännöllisesti.
Jos olet käyttänyt suuria annoksia inhaloitavaa steroidia pitkään, saattaa joskus olla tarpeen käyttää lisäannoksia steroidia, esimerkiksi stressaavissa olosuhteissa, kuten auto -onnettomuudessa tai ennen leikkausta. Lääkärisi voi päättää määrätä steroidilisän tänä aikana.
Potilaiden, joita on pitkään hoidettu suurilla steroidiannoksilla, mukaan lukien Fluspiral -paineistettu suspensio, ei tule lopettaa lääkkeen ottamista äkillisesti ilmoittamatta asiasta lääkärille. Äkillinen hoidon lopettaminen voi aiheuttaa huonovointisuutta ja oireita, kuten oksentelua, uneliaisuutta, pahoinvointia, päänsärkyä, väsymystä, ruokahaluttomuutta, alhaista verensokeria (hypoglykemiaa) ja painonmuutoksia.
Käyttöohjeet
Joidenkin ihmisten on vaikea suihkuttaa lääkettä heti inhalaation aloittamisen jälkeen.
Välikappale auttaa ratkaisemaan tämän ongelman.
Lääkärisi, sairaanhoitajasi tai apteekkihenkilökunnan tulee näyttää sinulle inhalaattorin käyttö.
Älä käytä Fluspiral -paineistettua suspensiota muuten kuin määrätty, muuten lääke ei ehkä lievitä astmaa.
Lääke on paineistetussa tölkissä, joka on sijoitettu muovikoteloon suukappaleen kanssa.
Tarkista inhalaattorin toiminta
- Kun käytät inhalaattoria ensimmäistä kertaa, kokeile sen toimivuutta. Irrota suukappaleen kansi painamalla sivuja varovasti peukalolla ja etusormella ja vedä se ulos.
- Varmistaaksesi, että se toimii, ravista sitä hyvin, suuntaa suukappale poispäin itsestäsi ja suihkuta annos ilmaan. Jos et käytä inhalaattoria viikkoon tai pidempään, suihkuta kahdesti ilmaan.
Inhalaattorin käyttö
Ennen inhalaattorin käyttöä on tärkeää aloittaa hengitys mahdollisimman hitaasti.
- Kun käytät inhalaattoria, pysy pystyssä tai istu pystyasennossa.
- Irrota suukappaleen kansi (kuten ensimmäisessä kuvassa). Tarkista sisältä ja ulkoa, että suukappale on puhdas ja vapaa esineistä.
- Ravista inhalaattoria 4 tai 5 kertaa varmistaaksesi, että kaikki esineet on poistettu ja että inhalaattorin sisältö sekoittuu tasaisesti.
- Pidä inhalaattoria pystyssä peukalosi pohjassa, suukappaleen alla.Hengitä ulos, kunnes tuntuu mukavalta.Älä hengitä vielä.
- Aseta suukappale suuhusi hampaiden väliin. Sulje huulet sen ympärille purra sitä.
- Hengitä sisään suun kautta. Heti sisäänhengityksen aloittamisen jälkeen paina purkin kantta vapauttaaksesi roiskeen lääkettä. Tee tämä samalla kun hengität tasaisesti ja syvään.
- Pidätä hengitystä; Ota inhalaattori ulos suustasi ja sormesi inhalaattorin yläosasta. Pidätä hengitystäsi muutaman sekunnin ajan tai kunnes se tuntuu mukavalta.
- Jos lääkäri on määrännyt sinua ottamaan kaksi inhalaatiota, odota noin puoli minuuttia ennen kuin hengität toisen annoksen toistamalla vaiheet 3--7.
- Aseta käytön jälkeen takaisin suukappaleen suojus, jotta pöly ei pääse sisään. Sulje kansi tiukasti painamalla sitä, kunnes se napsahtaa paikalleen.
Inhalaattorin puhdistaminen
Inhalaattorin tukkeutumisen estämiseksi on tärkeää puhdistaa se vähintään kerran viikossa.
- poista paineistettu säiliö inhalaattorista ja irrota suukappaleen kansi;
- älä koskaan poista metallipurkkia muovikääreestä;
- puhdista inhalaattori ja suukappaleen suojus kostealla liinalla;
- laita ne kuivumaan lämpimään paikkaan. Vältä liiallista kuumuutta;
- laita paineistettu säiliö takaisin inhalaattoriin ja aseta suukappaleen kansi takaisin paikalleen.Älä laita metallisäiliötä veteen.
Jos unohdat käyttää Fluspiralia
- Ota seuraava annos sen eräpäivän vuoksi.
- Älä ota kaksinkertaista annosta korvataksesi unohtamasi annoksen.
Jos lopetat Fluspiralin käytön
- Älä lopeta hoitoa, vaikka tuntisit olosi paremmaksi, ellei lääkäri kehota sinua tekemään niin.
Jos sinulla on kysymyksiä tämän lääkkeen käytöstä, käänny lääkärin, sairaanhoitajan tai apteekkihenkilökunnan puoleen.
Yliannostus Mitä tehdä, jos olet ottanut liikaa Fluspiralia?
Jos käytät enemmän Fluspiralia kuin sinun pitäisi, ota yhteys lääkäriisi mahdollisimman pian.
On tärkeää ottaa lääkärin määräämä annos. Älä nosta tai pienennä annosta kysymättä lääkäriltäsi neuvoa.
Sivuvaikutukset Mitkä ovat Fluspiralin sivuvaikutukset
Kuten kaikki lääkkeet, tämäkin lääke voi aiheuttaa haittavaikutuksia. Kaikki eivät kuitenkaan niitä saa.
Jos huomaat jonkin seuraavista vakavista haittavaikutuksista, lopeta tämän lääkkeen käyttö ja mene heti lääkäriin, koska saatat tarvita kiireellistä lääkärin hoitoa:
- allergiset reaktiot (voi esiintyä enintään 1 käyttäjällä 100: sta) - oireita ovat ihottuma, punoitus, kutina tai rakkulat, kuten nokkosihottuma tai nokkosihottuma;
- vaikeat allergiset reaktiot (voi esiintyä enintään 1 käyttäjällä 10000: sta) - oireita ovat kasvojen, huulten, suun, kielen tai kurkun turvotus, joka voi aiheuttaa nielemis- tai hengitysvaikeuksia, kutiava ihottuma, heikkouden tunne ja pyörrytys ja romahtaminen;
- hengitys tai hengityksen vinkuminen pahenee pian inhalaattorin käytön jälkeen.
Muita haittavaikutuksia ovat:
Hyvin yleinen (voi esiintyä useammalla kuin yhdellä henkilöllä 10: stä)
- sammas suussa ja kurkussa
Yleinen (voi esiintyä enintään 1 käyttäjällä 10: stä)
- kuiva kieli tai kurkku;
- käheä ääni.
Suun ja kurkun ongelmia voidaan vähentää tietyillä toimenpiteillä heti annoksen hengittämisen jälkeen.
Nämä ovat hampaiden harjaamista, suun huuhtelua tai kuristamista vedellä ja sylkemistä. Kerro lääkärillesi, jos sinulla on näitä suun tai kurkun ongelmia, mutta älä lopeta hoitoa, elleivät he niin kehota.
Lisäksi seuraavia haittavaikutuksia on raportoitu potilailla, joilla on krooninen obstruktiivinen keuhkosairaus (COPD):
- keuhkokuume ja keuhkoputkentulehdus (keuhkoinfektio); kerro lääkärillesi, jos saat jonkin seuraavista oireista: lisääntynyt ysköksen tuotanto, ysköksen värin muutos, kuume, vilunväristykset, lisääntynyt yskä, lisääntynyt hengitysvaikeus;
- mustelmat.
Harvinaiset (voi esiintyä enintään 1 käyttäjällä 1000: sta)
- sammas (kandidiaasi) ruokatorvessa
Hyvin harvinainen (voi esiintyä enintään 1 käyttäjällä 10000: sta)
- unihäiriöt tai huolestuneisuus, liiallinen innostus ja ärtyneisyys näitä vaikutuksia esiintyy todennäköisemmin nuorilla;
- nivelkivut;
- huono ruoansulatus;
- veren sokeripitoisuus (glukoosi) voi nousta;
- Fluspiralia käytettäessä keho voi vaikuttaa steroidien tuotantoon. Tämä tapahtuu todennäköisemmin, jos suuria annoksia käytetään pitkään aikaan (esim. 400 mikrogrammaa päivässä lapsilla).
Tämä voi aiheuttaa:
- nuorten kasvun hidastuminen;
- ns. Cushingin oireyhtymä, tila, jolle on tunnusomaista liiallinen steroidihormonien määrä verenkierrossa, mikä voi aiheuttaa luiden ohenemista ja silmäongelmia (kuten kaihi ja glaukooma, joka on silmänpaineen nousu).
Lääkärisi auttaa estämään tämän tapahtumasta varmistamalla, että käytät pienintä steroidiannosta oireiden hallintaan.
Vaikka esiintymistiheyttä ei tunneta, seuraavia haittavaikutuksia voi esiintyä:
- masennus, levottomuus tai hermostuneisuus näitä vaikutuksia esiintyy todennäköisemmin lapsilla.
- nenäverenvuoto.
Ota yhteys lääkäriisi mahdollisimman pian, jos:
- 7 päivän käytön jälkeen Fluspiralin hengenahdistus tai hengenahdistus ei parane tai pahenee;
- suurten inhaloitavien steroidiannosten käytön jälkeen huonovointisuutta ilmenee oireina, kuten vatsakipu, pahoinvointi, ripuli, päänsärky ja uneliaisuus. Tämä voi tapahtua "infektion, kuten" virusinfektion aikana, tai kun sinulla on vatsavaivoja. On tärkeää, että steroidiannosta ei lopeteta äkillisesti, koska se voi pahentaa astmaa ja aiheuttaa myös ongelmia kehon hormoneissa.
Sivuvaikutusten ilmoittaminen
Jos havaitset haittavaikutuksia, käänny lääkärin tai apteekkihenkilökunnan puoleen, mukaan lukien mahdolliset haittavaikutukset, joita ei ole mainittu tässä pakkausselosteessa. Voit ilmoittaa haittavaikutuksista myös suoraan (ks. Yhteystiedot alla) kansallisen ilmoitusjärjestelmän kautta osoitteessa www.agenziafarmaco.
Vanhentuminen ja säilyttäminen
- Ei lasten ulottuville eikä näkyville.
- Puhdista inhalaattori viikoittain osion "Puhdistus" mukaisesti.
- Älä käytä tätä lääkettä etiketissä ja kotelossa mainitun viimeisen käyttöpäivämäärän "EXP" jälkeen. Viimeinen käyttöpäivämäärä tarkoittaa kuukauden viimeistä päivää.
- Säilytä alle 30 ° C.Suojaa pakkaselta ja suoralta auringonvalolta.
- Jos inhalaattori on hyvin kylmä, ota metallisäiliö pois muovisäiliöstä ja lämmitä sitä käsissäsi muutaman minuutin ajan ennen käyttöä. Älä koskaan käytä mitään muuta sen lämmittämiseen.
- Metallipurkki on paineen alla. Älä lävistä, riko tai polta, vaikka se on ilmeisesti tyhjä.
- Älä heitä lääkkeitä viemäriin tai talousjätteisiin. Kysy apteekista, kuinka heittää pois lääkkeet, joita et enää käytä. Tämä auttaa suojelemaan ympäristöä.
Muita tietoja
Mitä Fluspiral sisältää
- Vaikuttava aine on flutikasonipropionaatti.
- Toinen komponentti on HFA 134a.
Miltä Fluspiral paineistettu suspensio näyttää ja pakkauksen sisältö
- Fluspiral paineistettu suspensio sisältää tölkin, annostelijan ja kannen pölyltä suojaamiseksi.
- Jokainen tölkki sisältää 120 annosta 50 mikrogrammaa flutikasonipropionaattia.
Alkuperäinen pakkausseloste: AIFA (Italian lääkevirasto). Sisältö julkaistu tammikuussa 2016. Esitetyt tiedot eivät välttämättä ole ajan tasalla.
Jotta saat käyttöösi uusimman version, on suositeltavaa käyttää AIFA: n (Italian Medicines Agency) verkkosivustoa. Vastuuvapauslauseke ja hyödyllistä tietoa.
01.0 LÄÄKEVALMISTEEN NIMI
FLUSPIRAL
02.0 LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS
FLUSPIRAL 125 mcg- Paineistettu suspensio inhalaatiota varten
Painesäiliö, jossa on 120 suihketta, sisältää:
Vaikuttava aine: flutikasonipropionaatti (125 mcg painallusta kohden) 15,00 mg
FLUSPIRAL 250 mcg - Paineistettu suspensio inhalaatiota varten
Painesäiliö, jossa on 120 suihketta, sisältää:
Vaikuttava aine: flutikasonipropionaatti (250 mcg annosta kohti) 30,00 mg
FLUSPIRAL 50 mcg - Paineistettu suspensio inhalaatiota varten
Painesäiliö, jossa on 120 suihketta, sisältää:
Vaikuttava aine: flutikasonipropionaatti (50 mcg painallusta kohden) 6,00 mg
FLUSPIRAL 250 mcg - inhalaatiojauhe
DISKUS -inhalaattorissa, jossa on 60 annosliuskaa
Yksi annos sisältää:
Vaikuttava aine: flutikasonipropionaatti 250 mcg
Apuaineet: laktoosi
FLUSPIRAL 500 mcg - inhalaatiojauhe
DISKUS -inhalaattorissa, jossa on 60 annosliuskaa
Yksi annos sisältää:
Vaikuttava aine: flutikasonipropionaatti 500 mcg
Apuaineet: laktoosi
FLUSPIRAL 100 mcg - inhalaatiojauhe
DISKUS -inhalaattorissa, jossa on 60 annosliuskaa
Yksi annos sisältää:
Vaikuttava aine: flutikasonipropionaatti 100 mcg
Apuaineet: laktoosi
Täydellinen apuaineluettelo, katso kohta 6.1
03.0 LÄÄKEMUOTO
Paineistettu suspensio inhalaatiota varten.
Jauhe inhalaatiota varten
04.0 KLIINISET TIEDOT
04.1 Käyttöaiheet
Astmaattisten sairauksien ja bronkostenoositilojen kehittymisen hallinta.
04.2 Annostus ja antotapa
Flutikasonipropionaattia tulee antaa vain suun kautta hengitettynä.
Potilaita tulee neuvoa inhaloitavan flutikasonipropionaattihoidon ennaltaehkäisevästä luonteesta ja sitä tulee käyttää säännöllisesti myös oireiden häviämisen jälkeen.
Potilaille on kerrottava, että lääkkeen teho ei ole välitön, ja siksi se on otettava säännöllisesti; terapeuttisen vaikutuksen alkaminen on 4–7 päivää, vaikka joissakin tapauksissa paraneminen voi tapahtua jo ensimmäisten 24 tunnin aikana potilailla ei ole aiemmin hoidettu inhaloitavilla steroideilla.
Jos potilas havaitsee nopeavaikutteisten beeta2-agonistien tehon heikkenemisen tai useamman käytön, on hakeuduttava lääkärin hoitoon.
Flutikasonipropionaatin annos on sovitettava yksittäisen potilaan mukaan astman vakavuuden ja hoidon vaiheen mukaan.
Kun potilaan hengitystoiminta on vakiintunut, vuorokausiannosta tulee pienentää asteittain yksilöllisen vasteen mukaan, kunnes saavutetaan pienin tehokas ylläpitoannos.
Hoitoa flutikasonipropionaatilla ei pidä lopettaa äkillisesti.
Lääkkeen annosta ei tarvitse pienentää iäkkäillä potilailla tai potilailla, joilla on maksan tai munuaisten vajaatoiminta.
FLUSPIRAL - Paineistettu suspensio inhalaatiota varten
Kuten kaikki lääkkeet, jotka annetaan inhalaationa, annostellulla aerosolilla, on suositeltavaa ottaa annos kahdella inhalaatiolla.
Potilailla, joiden liikkeiden koordinointi on heikkoa, voidaan käyttää sopivia välikappaleita.
FLUSPIRAL - jauhe inhalaatiota varten
Jokaisen annoksen sisältö hengitetään suoraan erityisestä moniannosinhalaattorista (DISKUS), joka mahdollistaa lääkkeen hengittämisen myös niille potilaille, jotka eivät pysty käyttämään paineistettua aerosolia oikein.
Aikuiset
Siellä vakioannos on 200 mcg päivässä, jaettuna kahteen 100 mcg: n annokseen.
Annosta voidaan nostaa jopa 400 mikrogrammaan päivässä.
Aloitusannosta voidaan myöhemmin säätää, kunnes kontrolli on saavutettu, tai pienentää pienimpään tehokkaaseen annokseen yksilöllisen vasteen mukaan.
Lääkärin tulee olla tietoinen siitä, että flutikasonipropionaatti on yhtä tehokas kuin muut inhaloitavat steroidit noin puolen mikrogramman vuorokausiannoksella. Esimerkiksi 100 mikrogrammaa flutikasonipropionaattia vastaa suunnilleen 200 mikrogramman annosta beklometasonidipropionaattia (CFC: tä sisältävissä formulaatioissa) tai budesonidia.
Flutikasonipropionaatin teho- ja siedettävyysprofiili sallii tämän inhaloitavan steroidin käytön myös vaikeita muotoja sairastavilla potilailla, jotka joutuvat usein turvautumaan suun kautta otettaviin steroideihin.Näillä potilailla flutikasonipropionaatti maksimiannoksella 2000 mcg päivässä voi mahdollistaa riittävän taudinhallinnan vähentämällä rajusti oraalisten steroidien käyttöä.
Pahenemisten aikana flutikasonipropionaatin annokset 2000 mcg päivässä voivat joissakin tapauksissa korvata oraaliset steroidisyklit.
Yli 4 -vuotiaat lapset
Siellä vakioannos on 100 mcg päivässä, jaettuna kahteen 50 mcg: n annokseen.
Annosta voidaan nostaa 200 mikrogrammaan päivässä.
Niille potilaille, joilla astmaa ei saada riittävästi hallintaan, lisähyötyä voidaan saavuttaa nostamalla annosta 200 mikrogrammaan kahdesti vuorokaudessa.
Hoito tulee aloittaa annoksella, joka vastaa sairauden vakavuutta.
Annosta voidaan myöhemmin säätää, kunnes kontrolli on saavutettu, tai pienentää pienimpään tehokkaaseen annokseen yksilöllisen vasteen mukaan.
On huomattava, että vain 50 mcg paineistettua inhalaatiosuspensiota voidaan käyttää tämän annoksen antamiseen.
Paineistettu inhalaatiosuspensio ei ehkä salli tarvittavan lapsiannoksen antamista; jos näin on, harkitse jauhemaisen flutikasonipropionaatin antoa inhalaation kautta DISKUS -inhalaattorin kautta.
Lapset 1-4 vuotta
FLUSPIRAL - Paineistettu suspensio inhalaatiota varten
100 mcg kahdesti vuorokaudessa, kun sitä käytetään kasvonaamarilla varustetulla välikelaitteella (lapsilla käytettävä välikelaite).
Flutikasonipropionaatin antaminen nuoremmille lapsille on hyödyllistä usein toistuvien ja jatkuvien astmaoireiden hallinnassa, ja se on tarkoitettu vain, jos oireita ei saada riittävästi hallintaan kerran vuorokaudessa annettavalla beeta -agonistihoidolla.
Suurin sallittu annos lapsilla on 200 mcg kahdesti vuorokaudessa.
1–4 -vuotiailla lapsilla tehdyt kliiniset tutkimukset ovat osoittaneet, että astman oireiden optimaalinen hallinta saavutetaan antamalla 100 mikrogrammaa kahdesti vuorokaudessa.
Nuoremmilla lapsilla tarvitaan suurempia annoksia kuin vanhemmilla lapsilla, koska lääkkeiden jakelun tehokkuus on heikentynyt hengitysteiden pienemmän kaliiperin, välikappaleen käytön tarpeen ja nenän kautta hengitettävän määrän lisääntymisen vuoksi.
Astman diagnoosia ja hoitoa on seurattava jatkuvasti.
FLUSPIRAL - jauhe inhalaatiota varten
Inhalaatiojauheen farmaseuttinen muoto ei sovellu 1-4 -vuotiaille lapsille; katso lääkkeen annostuksesta tässä ikäryhmässä FLUSPIRALin paineistettua inhalaatiosuspensiota koskevat tiedot.
04.3 Vasta -aiheet
Yliherkkyys vaikuttavalle aineelle tai kohdassa 6.1 mainituille apuaineille.
04.4 Varoitukset ja käyttöön liittyvät varotoimet
Astman hoito on yleensä suoritettava sairauden vakavuuteen mukautetun hoitosuunnitelman puitteissa. potilaan vaste hoitoon on varmistettava sekä kliinisesti että keuhkojen toimintakokeilla, jos ne ovat saatavilla.
Nopeasti vaikuttavien inhaloitavien beeta2-agonistien käytön tarve useammin osoittaa astman hallinnan pahenemista; tässä tilanteessa potilaan hoitosuunnitelmaa on muutettava.
Äkillinen ja progressiivinen astman paheneminen on mahdollisesti hengenvaarallinen, ja kortikosteroidiannoksen nostamista on harkittava. Riskiryhmään kuuluville potilaille suositellaan päivittäistä huippuvirtauksen seurantaa.
Systeemisiä vaikutuksia voi esiintyä inhaloitavilla kortikosteroideilla, erityisesti kun niitä määrätään suurina annoksina pitkiä aikoja. Näiden vaikutusten esiintyminen on epätodennäköisempää kuin suun kautta otettavalla kortikosteroidihoidolla. Mahdollisia systeemisiä vaikutuksia ovat Cushingin oireyhtymä, Cushingoid -näkökohta, lisämunuaisen vajaatoiminta, kasvun hidastuminen lapsilla ja nuorilla, luun mineraalitiheyden väheneminen, kaihi, glaukooma ja harvemmin erilaiset psykologiset tai käyttäytymiseen liittyvät vaikutukset, mukaan lukien psykomotorinen yliaktiivisuus, unihäiriöt, ahdistuneisuus, masennus tai aggressio (erityisesti lapsilla). Siksi on tärkeää, että inhaloitavan kortikosteroidiannos on pienin mahdollinen annos, jolla astma saadaan tehokkaasti hallintaan.
Poikia on esiintynyt erittäin harvinaisissa tapauksissa akuuttia lisämunuaiskriisiä suositelluilla suuremmilla annoksilla (noin 1000 mcg / vrk, kun ne annetaan inhalaationa paineistetun suspension kanssa tai vastaavat annokset muita inhaloitavia kortikosteroideja tai muita flutikasonipropionaattimuotoja) pitkiä aikoja (useita kuukausia tai vuosia) (ks. kohta 4.8).
On suositeltavaa seurata säännöllisesti pitkäaikaista inhaloitavaa kortikosteroidihoitoa saavien lasten pituutta.
Koska lisämunuaisen vaste on riittämätön, potilaita, jotka ovat aiemmin saaneet suun kautta otettavia steroideja ja jotka siirretään inhaloitavaan flutikasonipropionaattihoitoon, tulee hoitaa erityisen huolellisesti, lisämunuaisten toimintaa on seurattava säännöllisesti, systeeminen steroidihoito on lopetettava asteittain ja potilaita on neuvottava kantaa merkkiainetta, joka osoittaa, että he saattavat tarvita täydentävää kortikosteroidihoitoa stressin aikana.
Mahdollisuus saada riittämätön lisämunuaisen vaste hätätilanteissa (mukaan lukien kirurgiset toimenpiteet) ja myös valinnaisissa toimenpiteissä, jotka todennäköisesti aiheuttavat stressiä, on aina pidettävä mielessä, erityisesti potilailla, jotka käyttävät suuria annoksia pitkään. Kliiniseen tilanteeseen sopivaa kortikosteroidihoitoa tulee harkita (ks. Kohta 4.9).
Systeemisen kortikosteroidihoidon korvaaminen inhalaatiohoidolla voi paljastaa allergioita, kuten allergisen nuhan tai ihottuman, jotka aiemmin oli peitetty systeemisillä lääkkeillä.
Hoitoa flutikasonipropionaatilla ei pidä lopettaa äkillisesti.
Veren glukoosipitoisuuden nousua on raportoitu hyvin harvoin (ks. Kohta 4.8), ja tämä on otettava huomioon määrättäessä lääkettä potilaille, joilla on aiemmin ollut diabetes mellitus.
Kuten kaikkien inhaloitavien kortikosteroidien kohdalla, erityistä huomiota on kiinnitettävä potilaisiin, joilla on aktiivinen tai lepotilassa oleva keuhkotuberkuloosi.
Kliinisesti merkittäviä yhteisvaikutuksia on raportoitu markkinoille tulon jälkeen flutikasonipropionaattia ja ritonaviiria saaneilla potilailla, mikä on johtanut systeemisiin kortikosteroidivaikutuksiin, mukaan lukien Cushingin oireyhtymä ja lisämunuaisen vajaatoiminta. Siksi flutikasonipropionaatin ja ritonaviirin samanaikaista käyttöä tulee välttää, ellei mahdollinen hyöty potilaalle on suurempi kuin systeemisten kortikosteroidihaittavaikutusten riski (ks. kohta 4.5).
Kuten muidenkin inhaloitavien lääkkeiden kohdalla, paradoksaalista bronkospasmia ja lisääntynyttä hengenahdistusta voi ilmetä heti lääkkeen ottamisen jälkeen. Tässä tapauksessa ota välittömästi nopeavaikutteinen bronkodilataattori, lopeta flutikasonipropionaattihoito välittömästi, arvioi potilas uudelleen ja aloita tarvittaessa vaihtoehtoinen hoito (ks. Kohta 4.8) ).
Keuhkokuumeraporttien määrä lisääntyi tutkimuksissa, joissa oli mukana keuhkoahtaumatautipotilaita, jotka saivat 500 mikrogrammaa flutikasonipropionaattia (ks. Kohta 4.8) Lääkärien on oltava valppaita keuhkokuumeen mahdollisen kehittymisen suhteen keuhkoahtaumatautipotilailla, koska keuhkokuumeen ja pahenemisen kliiniset piirteet ovat usein päällekkäisiä.
FLUSPIRAL - Paineistettu suspensio inhalaatiota varten
Jos käytetään paineistettua suspensiota, potilaan inhalaatiotekniikka on tarkistettava sen varmistamiseksi, että inhalaattorin aktivointi synkronoidaan sisäänhengityksen kanssa, jotta varmistetaan lääkkeen optimaalinen kulkeutuminen keuhkoihin.
Koska lääkkeen systeeminen imeytyminen tapahtuu keuhkojen kautta, välilevyn käyttö voi lisätä lääkkeen pitoisuutta keuhkoissa ja siten systeemisten haittavaikutusten riskiä.
FLUSPIRAL - jauhe inhalaatiota varten
Fluspiral-inhalaatiojauhe sisältää laktoosia: Potilaiden, joilla on harvinainen perinnöllinen galaktoosi-intoleranssi, Lapp-laktaasin puutos tai glukoosi-galaktoosi-imeytymishäiriö, ei tule käyttää tätä lääkevalmistetta (ks. Myös kohta 4.5).
Laktoosi -apuaine sisältää maitoproteiineja, joten se ei sovellu henkilöille, jotka eivät siedä maitoproteiineja.
04.5 Yhteisvaikutukset muiden lääkevalmisteiden kanssa sekä muut yhteisvaikutukset
Normaaleissa olosuhteissa flutikasonipropionaatin pitoisuudet plasmassa ovat pieniä inhalaation jälkeen, mikä johtuu laajasta ensikierron metaboliasta ja sytokromi P450 3A4: n välittämästä suuresta systeemisestä puhdistumasta suolessa ja maksassa. Yhteisvaikutukset ovat siksi epätodennäköisiä.
Terveillä vapaaehtoisilla tehty yhteisvaikutustutkimus osoitti, että ritonaviiri (erittäin voimakas sytokromi P450 3A4: n estäjä) voi merkittävästi nostaa flutikasonipropionaatin pitoisuutta plasmassa, mikä johtaa merkittävästi pienempiin seerumin kortisolipitoisuuksiin.
Markkinoille tulon jälkeen käytön kliinisesti merkittäviä yhteisvaikutuksia on raportoitu potilailla, joita hoidettiin intranasaalisesti tai inhaloituna flutikasonipropionaatilla ja ritonaviirilla, mikä on johtanut systeemisiin kortikosteroidivaikutuksiin, mukaan lukien Cushingin oireyhtymä ja lisämunuaisen vajaatoiminta.
Siksi flutikasonipropionaatin ja ritonaviirin samanaikaista käyttöä tulee välttää, ellei mahdollinen hyöty potilaalle ole suurempi kuin systeemisten kortikosteroidien sivuvaikutusten riskit.
Tutkimukset ovat osoittaneet, että muut sytokromi P450 3A4: n estäjät lisäävät merkityksettömiä (erytromysiini) ja vähäisiä (ketokonatsoli) systeemisiä altistuksia flutikasonipropionaatille ilman, että seerumin kortisolipitoisuudet vähenevät merkittävästi. Varovaisuutta on kuitenkin noudatettava käytettäessä voimakkaita sytokromi P450 3A4: n estäjiä (esim. Ketokonatsoli) ) annetaan samanaikaisesti, koska flutikasonipropionaatin systeeminen altistus voi lisääntyä.
04.6 Raskaus ja imetys
Hedelmällisyys
Ihmisen hedelmällisyydestä ei ole tietoja. Eläinkokeet flutikasonilla eivät ole osoittaneet vaikutuksia miesten ja naisten hedelmällisyyteen. Eläinkokeet, joissa arvioitiin flutikasonipropionaatin mahdollisia vaikutuksia lisääntymistoimintoihin, ovat osoittaneet vain ne vaikutukset, jotka ovat ominaisia glukokortikoideille systeemisellä altistustasolla, joka on paljon suurempi kuin suositellulla terapeuttisella inhaloitulla annoksella havaitut vaikutukset.
Raskaus
Raskaana olevista naisista on vain vähän tietoja. Flutikasonipropionaatin käyttöä raskauden aikana tulee harkita vain, jos odotettu hyöty äidille on suurempi kuin sikiölle mahdollisesti aiheutuvat riskit.
Retrospektiivisen epidemiologisen tutkimuksen tulokset osoittavat, että vakavien synnynnäisten epämuodostumien (MCM) riski yksin flutikasonipropionaatille ja yhdessä salmeterolin kanssa altistumisen jälkeen ei ole suurempi kuin muilla inhaloitavilla kortikosteroideilla altistumisen riski raskauden ensimmäisen kolmanneksen aikana (ks. kohta 5.1 Kliiniset tutkimukset).
Ruokinta-aika
Ei tiedetä, erittyykö flutikasonipropionaatti äidinmaitoon.
Rotille annetun ihonalaisen annon jälkeen flutikasonipropionaattia todettiin äidinmaidosta mitattavissa olevilla plasman pitoisuuksilla. Plasman pitoisuudet ovat kuitenkin todennäköisesti alhaiset potilailla, jotka saavat flutikasonipropionaattia suositelluilla inhaloitavilla annoksilla.
Antamista imetyksen aikana tulee harkita vain, jos odotettu hyöty äidille on suurempi kuin sikiölle mahdollisesti aiheutuvat riskit.
04.7 Vaikutus ajokykyyn ja koneiden käyttökykyyn
Fluspiral ei vaikuta ajokykyyn ja koneiden käyttökykyyn
04.8 Haittavaikutukset
Haittavaikutukset on lueteltu alla elimen, elimen / järjestelmän ja esiintymistiheyden mukaan. Esiintymistiheydet on määritelty seuraavasti: hyvin yleinen (≥1 / 10), yleinen (≥1 / 100,
Infektiot ja tartunnat
Hyvin yleinen: suun ja kurkun kandidiaasi.
Joillakin potilailla voi esiintyä nielun kandidiaasia (sammas). Tällaiset potilaat voivat hyötyä huuhtelemalla suunsa vedellä lääkkeen ottamisen jälkeen Oireinen kandidiaasi voidaan hoitaa paikallisella sienilääkkeellä lopettamatta flutikasonipropionaatin käyttöä.
Yleinen: keuhkokuume (keuhkoahtaumatautipotilailla)
Hyvin harvinainen: ruokatorven kandidiaasi
Immuunijärjestelmän häiriöt
Yliherkkyysreaktioita, jotka ilmenevät seuraavasti:
Melko harvinainen: Ihon yliherkkyysreaktiot.
Hyvin harvinainen: angioedeema (pääasiassa kasvojen ja nielun turvotus), hengitysoireet (hengenahdistus ja / tai bronkospasmi) ja anafylaktiset reaktiot.
Endokriiniset patologiat
Mahdollisia systeemisiä vaikutuksia ovat (ks. Kohta 4.4):
Hyvin harvinainen: Cushingin oireyhtymä, Cushingoid -ulkonäkö, lisämunuaisen vajaatoiminta, kasvun hidastuminen, vähentynyt luun mineraalitiheys, kaihi, glaukooma.
Aineenvaihdunta- ja ravitsemushäiriöt
Hyvin harvinainen: Hyperglykemia.
Psyykkiset häiriöt
Hyvin harvinainen: Ahdistus, unihäiriöt ja käyttäytymishäiriöt, mukaan lukien psykomotorinen yliaktiivisuus ja ärtyneisyys (pääasiassa lapsilla).
Tuntematon: masennus ja aggressio (pääasiassa lapsilla).
Hengityselimet, rintakehä ja välikarsina
Yleinen: käheys.
Joillakin potilailla voi esiintyä käheyttä; jopa näissä tapauksissa voi olla edullista huuhdella suu vedellä heti inhalaation jälkeen.
Hyvin harvinainen: paradoksaalinen bronkospasmi (ks. Kohta 4.4).
Tuntematon: nenäverenvuoto
Iho ja ihonalainen kudos
Yleinen: mustelmat
Epäillyistä haittavaikutuksista ilmoittaminen.
Ilmoittaminen epäillyistä haittavaikutuksista, jotka ilmenevät lääkkeen myyntiluvan myöntämisen jälkeen, on tärkeää, koska se mahdollistaa lääkkeen hyöty -haitta -tasapainon jatkuvan seurannan. Terveydenhuollon ammattilaisia pyydetään ilmoittamaan kaikista epäillyistä haittavaikutuksista kansallisen ilmoitusjärjestelmän kautta. "Osoite www. agenziafarmaco.gov.it/it/responsabili.
04.9 Yliannostus
Oireet ja merkit
Lääkkeen akuutti hengittäminen suositelluilla annoksilla voi johtaa hypotalamus-aivolisäke-lisämunuaisen akselin tilapäiseen tukahduttamiseen. Tämä ei yleensä edellytä hätätoimenpiteiden aloittamista, koska lisämunuaisen toiminta palautuu normaalisti muutamassa päivässä.
Jos hyväksyttyjä suurempia annoksia käytetään pitkiä aikoja, lisämunuaisen toiminta voi merkittävästi heikentyä. Lisämunuaisreservin seuranta voi olla tarpeen.
On ollut erittäin harvinaisia akuutteja lisämunuaiskriisejä lapsilla, jotka ovat altistuneet suositelluille annoksille (tyypillisesti 1000 mikrog / vrk ja enemmän) pitkiä aikoja (useita kuukausia tai vuosia); havaittuja ilmenemismuotoja olivat hypoglykemia ja tajunnan heikkenemisen ja / tai kouristusten seuraukset).
Tilanteita, jotka voivat mahdollisesti laukaista akuutin lisämunuaiskriisin, ovat altistuminen traumalle, leikkaukselle, infektiolle tai annoksen nopeaan pienentämiseen.
Hoito
Potilaita, joita hoidetaan suuremmilla annoksilla kuin hyväksyttyjä, tulee seurata tarkoin ja annosta on pienennettävä vähitellen.
05.0 FARMAKOLOGISET OMINAISUUDET
05.1 Farmakodynaamiset ominaisuudet
Farmakoterapeuttinen ryhmä: Obstruktiivisten hengitysteiden oireyhtymien lääkkeet - inhaloitavat glukokortikoidit.
ATC -koodi: R03BA05
Toimintamekanismi
Flutikasonipropionaatilla, joka annetaan inhalaationa suositeltuina annoksina, on voimakas tulehdusta ehkäisevä vaikutus keuhkoihin, mikä vähentää oireita ja astman pahenemisvaiheita.
Kliiniset tutkimukset
Flutikasonipropionaattia sisältävät lääkkeet raskaana oleville naisille, joilla on astma
Epidemiologinen havainnollinen retrospektiivinen kohorttitutkimus, jossa käytettiin Yhdistyneen kuningaskunnan sähköisiä terveystietoja, arvioitiin MCM: ien riskiä inhaloitavalle flutikasonipropionaatille ja salmeteroli-flutikasonipropionaattiyhdistelmälle altistumisen jälkeen verrattuna inhaloituihin kortikosteroideihin, jotka eivät sisältäneet flutikasonipropionaattia raskauden ensimmäisen kolmanneksen aikana Ei vertailua lumelääkkeeseen tehtiin tässä tutkimuksessa.
Ensimmäisessä raskauskolmanneksessa inhaloitaville kortikosteroideille altistuneiden 5362 raskaana olevan naisen kohortissa havaittiin 131 MCM -diagnoosia vuoden aikana; 1612 (30%) altistettiin flutikasonipropionaatille tai salmeteroli-flutikasonipropionaatille, joista 42: llä diagnosoitiin MCM. Oikaistu todennäköisyyskerroin MCM -diagnooseille yli vuoden ajan oli 1,1 (95%: n luottamusväli: 0,5 - 2,3) keskivaikeaa astmaa sairastavilla naisilla, jotka olivat alttiina flutikasonipropionaatille, verrattuna kortikosteroideihin, jotka eivät sisältäneet flutikasonipropionaattia, ja 1,2 (95%: n luottamusväli: 0,7 -) 2.0) naisilla, joilla on huomattava tai vaikea astma. MCM: ien riskissä ei havaittu eroja ensimmäisen kolmanneksen flutikasonipropionaatti-altistuksen jälkeen verrattuna salmeteroli-flutikasonipropionaattiyhdistelmään. MCM: n absoluuttinen riski eri astman vakavuusalueilla vaihteli 2,0 - 2,9 / 100 flutikasonipropionaatille altistettua raskautta.
05.2 Farmakokineettiset ominaisuudet
Imeytyminen
Flutikasonipropionaatin absoluuttinen hyötyosuus kullakin inhalaation säätelijän tyypillä arvioitiin vertaamalla inhalaation ja laskimonsisäisen annostelun farmakokineettisiä tietoja kussakin tutkimuksessa ja tutkimusten välillä. Terveillä aikuisilla arvioitiin flutikasonipropionaatti -inhalaattorijauheen Diskus (7,8%) ja flutikasonipropionaatin inhalaatiosumutteen (10,9%) absoluuttista hyötyosuutta. Alhaisempi systeeminen altistus inhaloitavalle flutikasonipropionaatille havaittiin potilailla, joilla oli astma tai krooninen obstruktiivinen keuhkosairaus (COPD). Systeeminen imeytyminen tapahtuu pääasiassa keuhkojen kautta ja on aluksi nopeaa, sitten pitkittynyttä. on systeemisen altistuksen lineaarinen kasvu suhteessa inhaloidun annoksen suurentamiseen.
Jakelu
Flutikasonipropionaatilla on suuri vakaan tilan jakautumistilavuus (noin 300 l). Sitoutuminen plasman proteiineihin on kohtalaista (91%).
Biotransformaatio
Flutikasonipropionaatti poistuu hyvin nopeasti systeemisestä verenkierrosta, pääasiassa metaboloitumalla inaktiiviseksi karboksyylihappoyhdisteeksi, CYP3A4 -entsyymijärjestelmän sytokromi P450: n avulla. Varovaisuutta on noudatettava annettaessa lääkkeitä, joiden tiedetään estävän CYP3A4 -entsyymijärjestelmää, koska flutikasonipropionaatille voi kehittyä systeeminen altistus.
Eliminaatio
Flutikasonipropionaatin eliminaatiolle on tunnusomaista "suuri plasmapuhdistuma (1150 ml / min) ja" eliminaation puoliintumisaika "noin 8 tuntia. Flutikasonipropionaatin munuaispuhdistuma on vähäinen (alle 0,2%) ja alle 5 % eliminoituu metaboliittina.
05.3 Prekliiniset tiedot turvallisuudesta
Toksikologiset testit ovat osoittaneet, että suuremmilla annoksilla kuin terapeuttiseen käyttöön ehdotetut vaikutukset ovat ainoa voimakas kortikosteroidille tyypillinen vaikutusten luokka.
Krooniset toksisuustutkimukset eivät osoittaneet erityyppisiä vaikutuksia, samoin kuin lisääntymistoksikologian ja teratogeneesin tutkimukset.
Flutikasonipropionaatin todettiin olevan ei-mutageeninen in vitro ja in vivo eikä ei-onkogeeninen jyrsijöillä.
Eläinmalleissa flutikasonipropionaatin ei havaittu ärsyttävän eikä herkistävän.
On osoitettu, että ponneaine HFA 134a, ei CFC, on useissa eläinlajeissa altistettu päivittäin ponneaineelle kahden vuoden ajan.
06.0 FARMASEUTTISET TIEDOT
06.1 Apuaineet
Paineistettu suspensio inhalaatiota varten
Polttoaine HFA 134a.
Jauhe inhalaatiota varten
Laktoosi (joka sisältää maitoproteiineja).
06.2 Yhteensopimattomuus
Ei oleellinen
06.3 Voimassaoloaika
FLUSPIRAL - Paineistettu suspensio inhalaatiota varten: 2 vuotta.
FLUSPIRAL 100mcg inhalaatiojauhe: 2 vuotta; FLUSPIRAL 250mcg inhalaatiojauhe, FLUSPIRAL 500mcg inhalaatiojauhe: 3 vuotta.
06.4 Säilytys
Paineistettu suspensio inhalaatiota varten
Aseta inhalaattorin kansi tiukasti paikalleen, kunnes kuulet napsahduksen.
Pakkaukset on pidettävä poissa auringonvalolta ja jäätymiseltä.
Kuten useimpien paineistettujen aerosolilääkkeiden kohdalla, terapeuttinen vaikutus voi olla heikompi, jos painesäiliö on kylmä.
Painesäiliöitä ei saa rikkoa, puhkaista tai polttaa, vaikka ne olisivatkin ilmeisesti tyhjiä.
Jauhe inhalaatiota varten
Säilytä kuivassa paikassa.
Säilytä alkuperäispakkauksessa.Herkkä kosteudelle.
Keskustelu on suljettu laminaattisuojuksella, joka on avattava vain, kun lääkevalmistetta käytetään ensimmäisen kerran. Avattu laminaatinkotelo on hävitettävä.
06.5 Välipakkauksen luonne ja pakkauksen sisältö
Laatikot, joissa on paineistettu alumiinisäiliö, jossa on annosteluventtiili ja suhteellinen inhalaattori.
FLUSPIRAL 125 mcg - Paineistettu suspensio inhalaatiota varten
- Painesäiliö, jossa 120 suihketta, 125 mcg
FLUSPIRAL 250 mcg - Paineistettu suspensio inhalaatiota varten
- Painesäiliö, jossa 120 suihketta 250 mcg
FLUSPIRAL 50 mcg - Paineistettu suspensio inhalaatiota varten
- Painesäiliö, jossa 120 suihketta 50 mcg
Valetusta muovimateriaalista (DISKUS) valmistetut moniannosinhalaattorit, joissa kussakin on kaistale, johon on järjestetty säännöllisesti erilliset läpipainopakkaukset, joista jokainen sisältää annoksen (100-250-500 mcg) inhalaatiojauhetta dispergoitua flutikasonia laktoosissa.
FLUSPIRAL 250 mcg - inhalaatiojauhe
DISKUS-inhalaattorissa, jossa on 60 annoksen 250 mcg liuskat
FLUSPIRAL 500 mcg - inhalaatiojauhe
DISKUS-inhalaattorissa, jossa 60 annoksen 500 mcg liuskat
FLUSPIRAL 100 mcg - inhalaatiojauhe
DISKUS-inhalaattorissa, jossa on 60 annoksen 100 mcg liuskat
06.6 Käyttö- ja käsittelyohjeet
FLUSPIRAL - Paineistettu suspensio inhalaatiota varten
Tarkista inhalaattorin toiminta
Ennen kuin käytät inhalaattoria ensimmäistä kertaa tai kun sitä ei ole käytetty viikkoon, poista suukappaleen suojus puristamalla sitä kevyesti sivuilta, ravista inhalaattoria voimakkaasti ja suihkuta sitten annos ilmaan varmistaaksesi, että se toimii.
Inhalaattorin käyttö.
Tärkeä: älä suorita 5, 6 ja 7 kohdassa mainittuja toimenpiteitä kiireellisesti. Sumutetun materiaalin vuotaminen inhalaattorin yläpuolelle tai suun sivuilta osoittaa, että inhalaatiota ei suoritettu oikein; toista sitten toimenpiteet kohdasta 2.
Jos lääkäri antaa erilaisia tietoja inhalaattorin käytöstä, noudata niitä huolellisesti. On myös suositeltavaa ilmoittaa lääkärille mahdollisista vaikeuksista.
Inhalaattorin puhdistaminen
Inhalaattori on puhdistettava vähintään kerran viikossa.
1. Poista paineistettu säiliö inhalaattorista ja poista suukappaleen suojus.
2. Puhdista inhalaattori ja suukappaleen suojus kostealla liinalla.
3. Aseta ne kuivumaan lämpimään paikkaan. Vältä liiallista kuumuutta.
4. Aseta paineistettu säiliö takaisin inhalaattoriin ja suojakorkki takaisin suukappaleeseen.
ÄLÄ upota säiliötä vedenpaineeseen
FLUSPIRAL - Hengitysjauhe DISKUS -inhalaattorissa
LEVYTIEDOT
Kun levy on poistettu laatikosta, se on "kiinni" -asennossa.
DISKUS sisältää 60 yksilöllisesti suojattua annosta lääkejauhetta.
Jokainen annos mitataan huolellisesti ja suojataan hygieenisesti. LEVY ei vaadi huoltoa eikä sitä voi ladata uudelleen.
DISKUS -laitteen yläosassa oleva annosilmaisin näyttää vielä käytettävissä olevien annosten määrän.
Numerot 5 - 0 ovat PUNAISIA, mikä osoittaa, että jäljellä on vain muutama annos.
DISKUS on helppokäyttöinen.
Ota lääkeannos noudattamalla seuraavia neljää yksinkertaista vaihetta:
1. Avaaminen
2. Annoksen valmistelu
3. Hengitys
4. Sulkeminen
MITEN LEVY TOIMII
Liu'uttamalla DISKUS -vipua suukappaleeseen avataan pieni reikä ja annos valmistetaan inhaloitavaksi. Kun DISKUS suljetaan, vipu palaa automaattisesti alkuperäiseen asentoonsa valmiina valmistamaan seuraavan lääkeannoksen.
Ulompi kansi suojaa LEVYÄ, kun sitä ei käytetä.
1. Avaaminen
Avaa levy pitämällä toisella kädellä kiinni ulkoosasta ja asettamalla toisen käden peukalo syvennykseen. Paina peukalolla samalla kun pyörität laitteen sisäosaa, kunnes kuulet napsahduksen.
2. Annoksen valmistelu
Pidä levyä suukappale käyttäjää kohti. Liu'uta vipua eteenpäin, kunnes se napsahtaa. DISKUS on nyt käyttövalmis.
Aina kun vipua siirretään, annos on saatavana inhalaatiota varten annoksen osoittimen osoittamalla tavalla.
Käytä vipua vain silloin, kun sinun on hengitettävä lääkettä, jotta annokset eivät mene hukkaan.
3. Hengitys
Lue tämä kohta huolellisesti ennen hengittämistä.
Pidä LEVY kaukana suustasi. Hengitä mahdollisimman syvään. Älä koskaan puhalla levyyn.
Aseta suukappale huuliesi väliin.
Hengitä syvään ja säännöllisesti LEVYN kautta, älä nenän kautta.
Poista LEVY suustasi.
Pidätä hengitystäsi noin 10 sekuntia tai niin kauan kuin mahdollista.
Hengitä ulos hitaasti.
4. Sulkeminen
Sulje levy asettamalla peukalo syvennykseen ja liu'uttamalla sitä taaksepäin niin pitkälle kuin se menee.
Kun DISKUS suljetaan, se antaa terävän sulkeutuvan äänen. Tämä palauttaa vivun automaattisesti alkuperäiseen asentoonsa.
DISKUS on nyt valmis käytettäväksi uudelleen.
Jos kaksi inhalaatiota on määrätty, DISKUS on suljettava ensimmäisen inhalaation jälkeen ja toistettava sitten vaiheet 1-4.
HUOMIO
Pidä LEVY kuivana.
Pidä levy suljettuna, kun sitä ei käytetä.
Älä koskaan puhalla levyyn.
Liu'uta vipua vasta, kun olet valmis ottamaan lääkkeen.
Hengitä levyltä vain suulla.
Älä ylitä suositeltua annosta.
07.0 MYYNTILUVAN HALTIJA
A.Menarini Industrie Farmaceutiche Riunite s.r.l. - Via Sette Santi, 1 - Firenze
Lisensoinut GlaxoSmithKline S.p.A. - Verona
Jälleenmyyjä myytävänä:
Luso Farmaco Institute of Italy S.p.A. - Milanofiori - Tie 6 - Rakennus L - Rozzano (MI)
08.0 MYYNTILUVAN NUMERO
FLUSPIRAL 125 mcg 120 toimitusta 125 mcg ALK: 028675179
FLUSPIRAL 250 mcg 120 suihketta 250 mcg A.I.C .: 028675181
FLUSPIRAL 50 mcg 120 suihkutusta 50 mcg A.I.C .: 028675104
FLUSPIRAL 250 mcg Inhalaatiojauhe
DISKUS-inhalaattorissa, jossa on 60 annoksen 250 mcg liuskat A.I.C.: 028675270
FLUSPIRAL 500 mcg Inhalaatiojauhe
DISKUS-inhalaattorissa, jossa on 60 annoksen 500 mikrogramman liuska A.I.C.: 028675282
FLUSPIRAL 100 mcg Inhalaatiojauhe
DISKUS-inhalaattorissa, jossa on 60 annoksen 100 mcg liuskat A.I.C.: 028675268
09.0 MYYNTILUVAN TAI UUDISTAMISPÄIVÄMÄÄRÄ
Toukokuu 2003 / Toukokuu 2008
10.0 TEKSTIN MUUTTAMISPÄIVÄMÄÄRÄ
Maaliskuuta 2017