Jotta voidaan puhua kahdestakymmenestä aminohaposta, jotka muodostavat proteiinirakenteet ja modifioidut, olisi tarpeen kuvata vähintään kaksitoista erikoistunutta metabolista reittiä.
Mutta miksi solut käyttävät niin monia aineenvaihduntareittejä, jotka vaativat energiaa (esimerkiksi entsyymien katalyyttisten paikkojen regeneroimiseksi), joista jokaisella on entsymaattinen perintö, aminohappojen katabolisoimiseksi? Lähes kaikista aminohapoista on mahdollista saada erikoistuneita reittejä käyttäen metaboliitteja, joita käytetään pienessä osassa energian tuottamiseen (esimerkiksi glukoneogeneesin ja ketonikappaleiden kautta), mutta jotka johtavat ennen kaikkea kompleksien muodostumiseen molekyylejä, joissa on paljon hiiliatomeja (esimerkiksi fenyylialaniinista ja tyrosiinista, hormoneja tuotetaan tähän tarkoitukseen erikoistuneissa lisämunuaisissa); jos toisaalta olisi helppoa tuottaa energiaa aminohapoista, toisaalta monimutkaisten molekyylien rakentaminen pienistä molekyyleistä alkaen: aminohappojen katabolian ansiosta he voivat hyödyntää luurankoaan saadakseen suurempia lajeja.
Terve henkilö hajottaa päivittäin kaksi tai kolme hektogrammaa aminohappoja: 60-100 g niitä on peräisin ruokavalion sisältämistä proteiineista, mutta yli 2 hehtogrammaa saadaan normaalista kehon osana olevien proteiinien normaalista kierrosta. näiden proteiinien aminohapot, jotka vaurioituvat redoksiprosesseissa, korvataan muilla ja katabolisoidaan).
Aminohapot antavat energiaa ATP: n suhteen: a-aminoryhmän poistamisen jälkeen jäljellä oleva hiilipitoinen aminohapporunko voi sopivien muutosten jälkeen päästä krebs-sykliin. Lisäksi, kun ravinteiden tarjonta puuttuu ja glukoosin määrä vähenee, glukoneogeneesi aktivoituu: glukoneogeneettisten aminohappojen sanotaan olevan niitä, jotka sopivien muutosten jälkeen voidaan viedä glukoneogeneesiin; glukoneogeneettiset aminohapot ovat niitä, jotka voidaan muuntaa pyruvaattiin tai fumaraattiin (fumaraatti voidaan muuntaa malaatiksi, joka lähtee mitokondrioista ja muuttuu sytoplasmassa oksaloasetaatiksi, josta voidaan saada fosfenolipyruvaatia). etikka-asetaatti.
Juuri kuvattu on erittäin tärkeä näkökohta, koska aminohapot voivat korjata sokerin puutteen välittömästi paastoamisen yhteydessä; jos paasto jatkuu, lipidien aineenvaihdunta puuttuu kahden päivän kuluttua (koska proteiinirakenteita ei voida hyökätä liikaa), tässä vaiheessa rasvahappot muuttuvat asetyylikoentsyymi A- ja ketonikappaleiksi, koska glukoneogeneesi on hyvin rajallinen. Paastoamisen jälkeen aivot myös sopeutuvat käyttämään ketonikappaleita.
A-aminoryhmän siirtyminen aminohapoista tapahtuu transaminointireaktion kautta; entsyymit, jotka katalysoivat tätä reaktiota, he sanovat itse asiassa, transaminaasit (tai aminotransferaasi). Nämä entsyymit käyttävät entsymaattista kofaktoria nimeltä pyridoksaalifosfaatti, joka puuttuu aldehydiryhmäänsä. Pyridoksaalifosfaatti on pyridoksiinin, joka on pääasiassa vihanneksissa oleva vitamiini (B6), fosforylaation tuote.
Transaminaaseilla on seuraavat ominaisuudet:
Korkea spesifisyys ketoglutaraatti-glutamaatti-a-parille;
Ne on nimetty toisen parin mukaan.
Transaminaasientsyymit sisältävät aina a-ketoglutaraatti-glutamaattiparin, ja ne erotetaan toisen mukana olevan parin mukaan.
Esimerkkejä:
L "aspartaattitransaminaasi eli GOT (glutamaatti-osaaliasetaattitransaminaasi): entsyymi siirtää a-aminoryhmän aspartaatista a-ketoglutaraatiksi, jolloin saadaan oksaloasetaattia ja glutamaattia.
L "alaniinitransaminaasi eli GTP (glutamaatti-pyruvaattitransaminaasi): entsyymi siirtää a-aminoryhmän "alaniinista" a-ketoglutaraattiin, jolloin saadaan pyruvaattia ja glutamaattia.
Eri transaminaasit käyttävät α-ketogluraattia aminohappojen aminoryhmän vastaanottajana ja muuttavat sen glutamaatiksi; kun taas muodostuneita aminohappoja käytetään ketonikappaleiden reitillä.
Tämäntyyppinen reaktio voi tapahtua molempiin suuntiin, koska ne katkeavat ja muodostavat siteitä, joilla on sama energiasisältö.
Transaminaasit ovat sekä sytoplasmassa että mitokondrioissa (ne ovat enimmäkseen aktiivisia sytoplasmassa) ja eroavat isoelektrisestä pisteestään.
Transaminaasit kykenevät myös dekarboksyloimaan aminohappoja.
On oltava tapa muuntaa glutamaatti takaisin α-ketoglutaraatiksi: tämä tehdään deaminoimalla.
Siellä glutamaattidehydrogenaasi se on entsyymi, joka kykenee muuttamaan glutamaatin a-ketoglutaraatiksi ja siten muuttamaan glutamaatin muodossa olevien aminohappojen aminoryhmät ammoniakiksi. Tapahtuu redoksiprosessi, joka kulkee a-amino-glutaraatin välituotteen läpi: ammoniakki ja a-ketoglutaraatti vapautuvat ja palaavat verenkiertoon.
Sitten aminohappojen aminoryhmien hävittäminen kulkee transaminaasien (jotka vaihtelevat substraatin mukaan) ja glutamaattidehydrogenaasin läpi, joka määrittää ammoniakin muodostumisen.
Glutamaattidehydrogenaasia on kahdenlaisia: sytoplasminen ja mitokondrioiden; kofaktori, joka on myös tämän entsyymin lisäsubstraatti, on NAD (P) +: glutamaattidehydrogenaasi käyttää joko NAD +: ta tai NADP +: ta vähentävän voiman hyväksyjänä. Sytoplasminen muoto suosii, vaikkakaan ei yksinomaan, NADP +: ta, kun taas mitokondriomuoto suosii NAD +: ta. Mitokondrioiden muodon tarkoituksena on hävittää aminoryhmät: se johtaa ammoniakin (joka on substraatti mitokondrioihin erikoistuneelle entsyymille) ja NADH: n (joka lähetetään hengitysketjuun) muodostumiseen. Sytoplasminen muoto toimii vastakkaiseen suuntaan, eli se käyttää ammoniakkia ja a-ketoglutaraattia glutamaatin tuottamiseksi (jolla on biosynteettinen kohde): tämä reaktio on pelkistävä biosynteesi ja käytetty kofaktori on NADPH.
Glutamaattidehydrogenaasi toimii, kun on välttämätöntä hävittää aminohapporyhmät, kuten ammoniakki (virtsan kautta) tai kun aminohappojen luurankoja tarvitaan energian tuottamiseen: tämän entsyymin negatiiviset modulaattorit ovat siksi indikaattoreita joilla on hyvä energian saatavuus (ATP, GTP ja NAD (P) H) ja positiivisina modulaattoreina järjestelmät, jotka osoittavat energian tarpeen (AMP, ADP, GDP, NAD (P) +, aminohapot ja kilpirauhashormonit).
Aminohapot (pääasiassa leusiini) ovat glutamaattidehydrogenaasin positiivisia modulaattoreita: jos aminohappoja on läsnä sytoplasmassa, niitä voidaan käyttää proteiinisynteesiin tai ne on hävitettävä, koska niitä ei voi kertyä (tämä selittää, miksi aminohapot ovat positiivisia modulaattoreita) ).
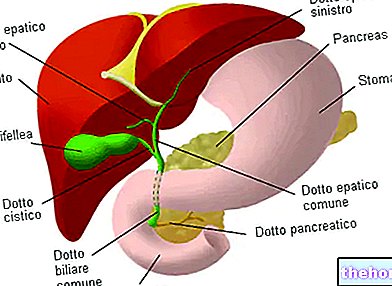
Ammoniakin hävittäminen: ureakierto
Kalat hävittävät ammoniakin viemällä sen veteen kidusten kautta; linnut muuttavat sen virtsahapoksi (joka on kondensaatiotuote) ja poistavat sen ulosteella. Katsotaanpa, mitä ihmisillä tapahtuu: olemme sanoneet, että glutamaattidehydrogenaasi muuttaa glutamaatin α- ketoglutaraatti ja ammoniakki, mutta emme ole sanoneet, että tämä tapahtuu vain maksan mitokondrioissa.
Ammoniakin hävittämisellä ureakierron kautta on keskeinen rooli mitokondrioiden transaminaaseilla.

Hiilidioksidi, bikarbonaatti-ionin (HCO3-) muodossa, aktivoidaan biotiinikofaktorilla, joka muodostaa karboksi-biotiinin, joka reagoi ammoniakin kanssa ja antaa karbamiinihappoa; seuraavassa reaktiossa käytetään ATP: tä fosfaatin siirtämiseksi karbamiinihapolle muodostaen karbamyylifosfaattia ja ADP: tä (ATP: n muuntaminen ADP: ksi on liikkeellepaneva voima karboksibiotiinin saamisessa.) Tätä vaihetta katalysoi karbamyylifosfaattisyntetaasi ja esiintyy mitokondrioissa. Karbamyylifosfaatti ja ornitiini ovat entsyymin substraatteja ornitiinitrans -karbamylaasi joka muuttaa ne sitrulliiniksi; tämä reaktio tapahtuu mitokondrioissa (hepatosyytit). Tuotettu sitrulliini lähtee mitokondrioista ja menee sytoplasmassa "toiminnan" allearginiinisukkinaattisyntetaasi: fuusio tapahtuu sitrulliinin ja aspartaatin hiilipitoisen rungon välillä nukleofiilisen hyökkäyksen ja veden poistamisen jälkeen. Arginiinisukkinaattisyntaasientsyymi vaatii ATP -molekyylin, joten siinä on energinen kytkentä: ATP: n hydrolyysi AMP: ksi ja pyrofosfaatiksi (jälkimmäinen muutetaan sitten kahdeksi ortofosfaattimolekyyliksi) tapahtuu poistamalla molekyyli d "vettä substraatista. eikä väliaineen veden vaikutuksesta.
"Seuraava entsyymi on"arginiinisukkinaasia: tämä entsyymi pystyy jakamaan arginiinisukkinaatin arginiiniksi ja fumaraatiksi sytoplasmassa.
Entsyymi täydentää ureakiertoa arginaasisaadaan ureaa ja ornitiinia; urea hävitetään munuaisten kautta (virtsa), kun ornitiini palaa mitokondrioihin ja jatkaa sykliä.
Arginiini muuttaa epäsuorasti ureakiertoa: arginiinin kertyminen osoittaa, että ureakiertoa on nopeutettava; arginiinin modulaatio on epäsuora, koska arginiini säätelee positiivisesti asetyyliglutamaattisyntetaasientsyymiä. Jälkimmäinen kykenee siirtämään asetyyliryhmän glutamaatin typelle: muodostuu N-asetyyliglutamaattia, joka on karbamyyli-fosfosyntaasientsyymin suora modulaattori.
Arginiini kerääntyy ureakierron metaboliitiksi, jos karbamyylifosfaatin tuotanto ei riitä ornitiinin hävittämiseen.
Ureaa tuotetaan vain maksassa, mutta on muitakin paikkoja, joissa ensimmäiset reaktiot tapahtuvat.
Aivot ja lihakset käyttävät erityisiä strategioita aminoryhmien poistamiseksi. Aivot käyttävät erittäin tehokasta menetelmää, jossa käytetään entsyymiä glutamiinisyntetaasi ja entsyymi glutamaasi: ensimmäinen on läsnä neuroneissa, kun taas toinen on maksassa. Tämä mekanismi on erittäin tehokas kahdesta syystä:
Kaksi aminoryhmää kuljetetaan aivoista maksaan yhdessä vehikkelissä;
Glutamiini on paljon vähemmän myrkyllistä kuin glutamaatti (glutamaatti myös siirtää hermosoluja eikä saa ylittää fysiologista pitoisuutta).
Kaloissa samanlainen mekanismi tuo aminohappojen aminoryhmän kiduksiin.
Lihaksesta (luuranko ja sydän) aminoryhmät saavuttavat maksan glukoosi-alaniinisyklin kautta; mukana oleva entsyymi on glutamiini-pyruvaattitransaminaasi: se sallii aminohapporyhmien (jotka ovat glutamaatin muodossa) saattamisen osaksi kansallista lainsäädäntöä, muuntaa pyruvaatin alaniiniksi ja samalla glutamaatin α-ketoglutaraatiksi lihaksessa ja katalysoi käänteinen prosessi maksassa.
Transaminaaseilla, joilla on eri tehtävät tai asemat, on myös rakenteellisia eroja ja ne voidaan määrittää elektroforeesilla (niillä on erilaiset isoelektriset pisteet).
Transaminaasien esiintyminen veressä voi olla oire maksan tai sydämen vauriosta (eli kudosvauriosta maksassa tai sydänsoluissa); transaminaasit ovat erittäin korkeita pitoisuuksia sekä maksassa että sydämessä: elektroforeesin avulla on mahdollista selvittää, onko vaurio tapahtunut maksassa tai sydänsoluissa.