-cloruro.jpg)
Mitä Lumark - Lutetium (177Lu) kloridi on ja mihin sitä käytetään?
Lumark sisältää radioaktiivista yhdistettä Lutetium (177Lu) kloridia ja sitä käytetään muiden lääkkeiden radioaktiiviseen merkintään. Radioleimaus on tekniikka, joka sisältää lääkkeen merkitsemisen (tai "merkitsemisen") radioaktiivisella yhdisteellä, jotta radioaktiivisuus voidaan kuljettaa tarvittavaan kehon osaan, esimerkiksi kasvaimen kohtaan.
Lumarkia ei anneta yksin potilaille - sitä käytetään vain radioaktiivisten lääkkeiden leimaamiseen, jotka on erityisesti kehitetty käytettäväksi Lumarkin kanssa.
Miten Lumarkia käytetään - Lutetium (177Lu) kloridia?
Lumarkia saavat käyttää vain asiantuntijat, joilla on kokemusta radioaktiivisesta merkinnästä.
Lumarkia ei koskaan anneta yksin. Radioleimaus Lumarkilla tapahtuu laboratoriossa. Radioleimattu lääke annetaan sitten potilaalle lääkkeen tuotetiedoissa annettujen ohjeiden mukaisesti.
Miten Lumark - Lutetium (177Lu) kloridi toimii?
Lumarkin vaikuttava aine, lutetium (177Lu) kloridi, on radioaktiivinen yhdiste, joka säteilee pääasiassa beetasäteilyksi kutsuttua säteilyä ja pienellä määrällä gammasäteilyä. Kun radioleimattu Lumarkilla, lääke kuljettaa säteilyn siihen kehon osaan, missä sitä tarvitaan, syöpäsolujen tappamiseen (terapeuttisessa käytössä) tai kuvien saamiseksi näytölle (diagnostiseen käyttöön).
Mitä hyötyä Lumark - Lutetium (177Lu) -kloridista on havaittu tutkimuksissa?
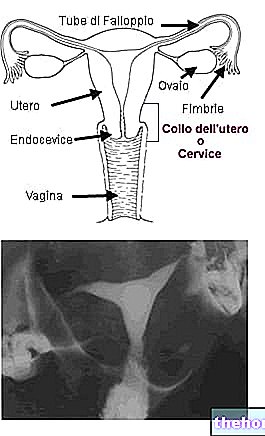
Koska lutetiumin (177Lu) käyttö lääkkeiden radioaktiiviseen merkintään on vakiintunutta, yhtiö esitti tieteellisestä kirjallisuudesta saatuja tietoja.Lukuiset julkaistut tutkimukset ovat osoittaneet, että lutetium (177Lu) on hyödyllinen lääkkeiden radioleimauksessa neuroendokriinisten kasvainten diagnosointiin ja hoitoon , ryhmä kasvaimia, jotka hyökkäävät hormoneja erittäviin soluihin kehon eri osissa, mukaan lukien haima, suolet, vatsa ja keuhkot.
Lumarkin hyödyt riippuvat suurelta osin radioleimaukseen käytetystä lääkkeestä.
Mitä riskejä Lumark - Lutetium (177Lu) kloridiin liittyy?
Lumarkin sivuvaikutukset ovat suuresti riippuvaisia siitä, minkä lääkkeen kanssa sitä käytetään, ja ne on kuvattu kyseisen lääkkeen pakkausselosteessa. Lumark itsessään on radioaktiivinen, joten kuten mikä tahansa muu radioaktiivinen lääke, sen käyttöön voi liittyä syövän ja perinnöllisten vikojen kehittymiseen liittyviä riskejä. Käytettävä Lumark -määrä on kuitenkin pieni ja siksi näitä riskejä pidetään vähäisinä. olisi varmistettava, että Lumarkin käytön odotetut hyödyt potilaille ovat suurempia kuin radioaktiivisuuden aiheuttamat riskit.
Lumarkilla radioleimattuja lääkkeitä ei tule käyttää raskaana oleville tai hedelmällisessä iässä oleville naisille. Pakkausselosteessa on luettelo kaikista Lumarkin käyttöä koskevista rajoituksista. Lisätietoja rajoituksista, joita sovelletaan Lumarkilla radioleimattuihin lääkkeisiin, on näiden lääkkeiden pakkausselosteissa
Miksi Lumark - Lutetium (177Lu) kloridi on hyväksytty?
Ihmisille tarkoitettuja lääkkeitä käsittelevä komitea (CHMP) katsoi, että lutetiumin (177Lu) käyttö lääkkeiden radioaktiiviseen merkintään on vakiintunutta ja tieteellisessä kirjallisuudessa hyvin dokumentoitua. Lumark -säteilyaltistuksen käyttöön liittyvät riskit Lumarkin tuotetiedot sisältävät ohjeita näiden riskien minimoimiseksi.
Lääkevalmistekomitea katsoi, että Lumarkin hyödyt ovat sen riskejä suuremmat, ja suositteli siksi myyntiluvan myöntämistä sille.
Miten voidaan varmistaa Lumark - Lutetium (177Lu) -kloridin turvallinen ja tehokas käyttö?
Lumarkin mahdollisimman turvallisen käytön varmistamiseksi on kehitetty riskinhallintasuunnitelma. Tämän suunnitelman perusteella Lumarkin valmisteyhteenvetoon ja pakkausselosteeseen on lisätty turvallisuustietoja, mukaan lukien asianmukaiset varotoimenpiteet, joita terveydenhuollon ammattilaisten ja potilaiden on noudatettava.
Lisätietoja on riskienhallintasuunnitelman yhteenvedossa
Muita tietoja Lumark - Lutetium (177Lu) -kloridista
Euroopan komissio antoi 19. kesäkuuta 2015 Lumarkille myyntiluvan, joka on voimassa koko Euroopan unionin alueella.
EPAR -lausunnon täydellinen versio ja yhteenveto Lumarkin riskinhallintasuunnitelmasta on viraston verkkosivustolla: ema.Europa.eu/Find medicine / Human medicines / European public assessment reports. Lisätietoja Lumark-hoidosta saa pakkausselosteesta (sisältyy EPAR-lausuntoon) tai lääkäriltä tai apteekista Tämä yhteenveto on päivitetty viimeksi 06-2015.
Tällä sivulla julkaistut tiedot Lumark - Lutetium (177Lu) kloridista voivat olla vanhentuneita tai puutteellisia. Jos haluat käyttää näitä tietoja oikein, katso Vastuuvapauslauseke ja hyödyllisiä tietoja -sivu.


.jpg)