Vaikuttavat aineet: Ketoprofeeni
ORUDIS 50 mg kovat kapselit
Orudis -pakkausselosteita on saatavana seuraaville pakkauskokoille:- ORUDIS 50 mg kovat kapselit
- ORUDIS 100 mg depotkapselit, ORUDIS 200 mg depotkapselit
- ORUDIS 100 mg / 2 ml injektioneste, liuos lihakseen
- ORUDIS 100 mg peräpuikot
- ORUDIS 5% geeli
Käyttöaiheet Miksi Orudista käytetään? Mitä varten se on?
FARMAKOTERAPEUTTINEN LUOKKA
Orudis, 2- (3-bentsoyylifenyyli) propionihappo tai ketoprofeeni, on ei-steroidinen tulehduskipulääke, jolla on voimakas tulehdusta, kipua ja kuumetta alentava vaikutus.
HOITO -OHJEET
Nivelreuma, selkärankareuma, akuutti kihti, nivelrikko eri paikkoja, iskias, radikuliitti, myalgia, bursiitti, jännetulehdus, tenosynoviitti, niveltulehdus, kapsuliitti, murskaukset, nyrjähdykset, dislokaatiot, lihaskyyneleet, laskimotulehdus, kivulias imusolmuketulehdus, pinnallinen tromboflebiitti ja keuhkosairaus.
Vasta -aiheet Kun Orudista ei tule käyttää
Orudis on vasta-aiheinen potilaille, joilla on aiemmin esiintynyt yliherkkyysreaktioita, kuten bronkospasmi, astmakohtauksia, nuhaa, nokkosihottumaa tai muita allergisia reaktioita, ketoprofeenille, asetyylisalisyylihapolle (ASA) tai muille ei-steroidisille tulehduskipulääkkeille (NSAID). näillä potilailla on raportoitu vakavia, harvoin kuolemaan johtavia anafylaktisia reaktioita (ks. myös sivuvaikutukset).
Orudis on vasta -aiheinen myös seuraavissa tapauksissa:
- yliherkkyys jollekin apuaineelle;
- raskauden kolmannen kolmanneksen aikana
- intensiivisen diureettihoidon aikana;
- vaikea munuaisten vajaatoiminta;
- vakavat maksan vajaatoiminnan muodot (maksakirroosi, vaikea hepatiitti);
- leukopenia ja trombosytopenia;
- potilailla, joilla on jatkuva verenvuoto
- hemorraginen diateesi;
- vaikea sydämen vajaatoiminta;
- aktiivinen mahahaava tai aiempi ruoansulatuskanavan verenvuoto, haavauma tai perforaatio.
- Orudis on yleensä vasta -aiheinen raskauden, imetyksen aikana (ks. Myös erityisvaroitukset) ja lasten iässä.
Käyttöä koskevat varotoimet Mitä sinun on tiedettävä, ennen kuin otat Orudista
Orudis 50 mg kapselit sisältävät laktoosia; Potilaiden, joilla on harvinainen perinnöllinen galaktoosi-intoleranssi, Lapp-laktaasin puutos tai glukoosi-galaktoosi-imeytymishäiriö, ei tule käyttää tätä lääkettä.
Haittavaikutuksia voidaan minimoida käyttämällä pienintä tehokasta annosta mahdollisimman lyhyen hoidon ajan, joka tarvitaan oireiden hallintaan.
Munuaisten toimintaa on seurattava huolellisesti hoidon alussa potilailla, joilla on sydämen vajaatoiminta, kirroosi ja nefroosi, diureettihoitoa saavilla potilailla, joilla on krooninen munuaisten vajaatoiminta etenkin iäkkäillä potilailla. , joka johtuu prostaglandiinien estämisestä ja johtaa munuaisten muutoksiin.
Varovaisuutta on noudatettava potilailla, joilla on aiemmin ollut kohonnut verenpaine ja / tai sydämen vajaatoiminta, koska NSAID -hoidon yhteydessä on raportoitu nesteen kertymistä ja turvotusta.
Kuten muidenkin ei-steroidisten tulehduskipulääkkeiden kohdalla, ketoprofeenin tulehdusta, kipua lievittävät ja kuumetta alentavat vaikutukset voivat peittää infektion läsnä ollessa infektion etenemisen oireita, kuten kuumetta.
Potilaiden, joiden maksan toimintakokeet ovat heikentyneet tai joilla on aiempi maksasairaus, transaminaasiarvot on arvioitava säännöllisesti, erityisesti pitkäaikaishoidon aikana. Ketoprofeenin käytön yhteydessä on raportoitu harvinaisia keltaisuutta ja hepatiittitapauksia.
Tulehduskipulääkkeiden käyttö voi heikentää naisten hedelmällisyyttä, eikä sitä suositella raskautta suunnitteleville naisille Naisilla, joilla on hedelmällisyysongelmia tai jotka tutkivat hedelmällisyyttä, on harkittava hoidon lopettamista.
Potilailla, joilla on astma, johon liittyy krooninen nuha, krooninen sinuiitti ja / tai nenän polyypit, on suurempi riski allergioille aspiriinille ja / tai tulehduskipulääkkeille kuin muulla väestöllä. Tämän lääkevalmisteen antaminen voi aiheuttaa astmakohtauksia tai bronkospasmeja. aspiriinille tai tulehduskipulääkkeille (ks. myös Vasta -aiheet).
Potilaita, joilla on hallitsematon hypertensio, kongestiivinen sydämen vajaatoiminta, todettu iskeeminen sydänsairaus, perifeerinen valtimotauti ja / tai aivoverisuonisairaus, saa hoitaa ketoprofeenilla vain huolellisen harkinnan jälkeen. Samanlaisia näkökohtia on harkittava ennen pitkäaikaishoidon aloittamista potilailla, joilla on sydän- ja verisuonitautien riskitekijöitä (esim. Kohonnut verenpaine, hyperlipidemia, diabetes mellitus, tupakointi).
Jos näköhäiriöitä, kuten näön hämärtymistä, ilmenee, hoito on lopetettava
Yhteisvaikutukset Mitkä lääkkeet tai elintarvikkeet voivat muuttaa Orudiksen vaikutusta
Kerro lääkärille tai apteekkihenkilökunnalle, jos olet äskettäin käyttänyt muita lääkkeitä, myös ilman reseptiä.
YHDISTYKSET EI SUOSITTELE
Muut ei-steroidiset tulehduskipulääkkeet (mukaan lukien selektiiviset syklo-oksigenaasi-2-estäjät) ja suuriannoksiset salisylaatit: lisääntynyt ruoansulatuskanavan haavaumien ja verenvuodon riski.
Antikoagulantit (hepariini ja varfariini) ja verihiutaleita estävät aineet (esim. Tiklopidiini ja klopidogreeli): lisääntynyt verenvuotoriski (ks. Varotoimet) Jos samanaikaista käyttöä ei voida välttää, potilaita on seurattava tarkasti.
Litium: riski kohota plasman litiumpitoisuuksia, jotka voivat joskus saavuttaa myrkyllisiä pitoisuuksia litiumin erittymisen vähentyessä munuaisten vuoksi. Tarvittaessa plasman litiumtasoja on seurattava mahdollisella annosmuutoksella NSAID -hoidon aikana ja sen jälkeen.
Metotreksaatti annoksilla yli 15 mg / viikko: metotreksaatin aiheuttama hematologisen toksisuuden riski kasvaa, erityisesti kun sitä annetaan suurina annoksina (> 15 mg / viikko); mahdollisesti johtuen metotreksaatin sitoutumisesta proteiineihin ja heikentyneestä munuaispuhdistumasta. Jos potilaalla on jo ketoprofeenihoito, hoito on lopetettava vähintään 12 tuntia ennen metotreksaatin antamista. Jos ketoprofeeni annetaan metotreksaattihoidon lopussa, on odotettava 12 tuntia ennen antamista.
VAROITUSTA KOSKEVAT YHDISTYKSET
Kortikosteroidit: lisääntynyt ruoansulatuskanavan haavaumien tai verenvuodon riski (ks. Myös erityisvaroitukset).
Diureetit: diureetteja käyttävillä potilailla ja heidän joukossaan, erityisesti dehydratoituneilla potilailla, on suuri riski sairastua munuaisten vajaatoimintaan, kun prostaglandiinien esto aiheuttaa munuaisten verenkierron heikkenemisen. Nämä potilaat on nesteytettävä ennen yhteiskäytön aloittamista. Ja munuaisten toimintaa on seurattava, kun hoito aloitetaan.
ACE: n estäjät ja angiotensiini II -antagonistit: Potilailla, joilla on munuaisten vajaatoiminta (esim. Dehydratoituneet potilaat tai iäkkäät potilaat), ACE: n estäjän tai angiotensiini II -antagonistin ja syklo-oksigenaasijärjestelmää estävien aineiden samanaikainen käyttö voi johtaa munuaisten toiminnan heikkenemiseen entisestään mukaan lukien mahdollinen akuutti munuaisten vajaatoiminta. Nämä yhteisvaikutukset on otettava huomioon potilailla, jotka käyttävät Orudista samanaikaisesti ACE: n estäjien tai angiotensiini II -reseptorin salpaajien kanssa, joten yhdistelmää on käytettävä varoen, erityisesti iäkkäillä potilailla.
Potilaiden tulee olla riittävästi nesteytettyjä ja munuaisten toimintaa on seurattava samanaikaisen hoidon aloittamisen jälkeen (ks. Varotoimet).
Metotreksaatti annoksilla alle 15 mg / viikko: Täydellinen verenkuva on tehtävä joka viikko yhdistelmähoidon ensimmäisten viikkojen aikana. Munuaisten vajaatoiminnan tai iäkkäiden potilaiden seurannan tulisi olla tiheämpää.
Pentoksifylliini: se määrittää lisääntyneen verenvuotoriskin. Lähempi kliininen seuranta ja verenvuodon seuranta on tarpeen.
HUOMIOITAVAT YHDISTYKSET
Verenpainelääkkeet (beetasalpaajat, angiotensiiniä konvertoivat entsyymit, diureetit): verenpainelääkityksen vähenemisen riski (tulehduskipulääkkeiden aiheuttama prostaglandiinien vasodilataation esto).
Trombolyytit: lisääntynyt verenvuotoriski.
Probenesidi: Probenesidin samanaikainen käyttö voi merkittävästi pienentää ketoprofeenin plasmapuhdistumaa. Selektiiviset serotoniinin takaisinoton estäjät (SSRI: t): lisääntynyt ruoansulatuskanavan verenvuodon riski (ks. Varotoimet).
Gemeprost: gemeprostin tehon heikkeneminen.
Kohdunsisäiset ehkäisyvälineet (IUD): laitteen tehokkuus voi heikentyä, mikä johtaa raskauteen.
Varoitukset On tärkeää tietää, että:
Orudiksen kaltaisiin lääkkeisiin voi liittyä pieni sydänkohtauksen (sydäninfarkti) tai aivohalvauksen riski. Kaikki riskit ovat todennäköisempiä suurilla annoksilla ja pitkillä hoidoilla. Älä ylitä suositeltua annosta tai hoidon kestoa.
Orudiksen samanaikaista käyttöä muiden tulehduskipulääkkeiden kanssa, mukaan lukien selektiiviset syklo-oksigenaasi-2-estäjät, tulee välttää.
Ruoansulatuskanavan verenvuoto, haavauma tai perforaatio: Ruoansulatuskanavan verenvuotoa, haavaumia ja perforaatioita, jotka voivat olla hengenvaarallisia, on raportoitu kaikkien tulehduskipulääkkeiden käytön aikana, milloin tahansa, joko varoitusoireiden kanssa tai ilman tai vakavia ruoansulatuskanavan tapahtumia.
Iäkkäillä potilailla ja potilailla, joilla on aiemmin ollut haavaumia, erityisesti jos ne ovat monimutkaisia verenvuodon tai perforaation kanssa (ks. Myös Vasta -aiheet), ruoansulatuskanavan verenvuotojen, haavaumien tai perforaatioiden riski on suurempi, jos NSAID -annoksia suurennetaan. Näiden potilaiden tulee aloittaa hoito pienimmällä mahdollisella annoksella. Suoja -aineiden (misoprostolin tai protonipumpun estäjien) samanaikaista käyttöä on harkittava näille potilaille ja myös potilaille, jotka käyttävät pieniä annoksia aspiriinia tai muita lääkkeitä, jotka voivat lisätä ruoansulatuskanavan tapahtumien riskiä (ks. Alla ja Yhteisvaikutukset).
Potilaiden, joilla on aiemmin ollut ruoansulatuskanavan toksisuutta, erityisesti vanhusten, on ilmoitettava kaikista vatsan oireista (erityisesti ruoansulatuskanavan verenvuodosta) erityisesti hoidon alkuvaiheessa.
Varovaisuutta on noudatettava potilailla, jotka käyttävät samanaikaisesti lääkkeitä, jotka voivat lisätä haavaumien tai verenvuotojen riskiä, kuten suun kautta otettavia kortikosteroideja, antikoagulantteja, kuten varfariinia, selektiivisiä serotoniinin takaisinoton estäjiä tai verihiutaleita estäviä aineita, kuten aspiriinia (ks. Yhteisvaikutukset).
Kun Orudis -hoitoa saavilla potilailla ilmenee ruoansulatuskanavan verenvuotoa tai haavaumia, hoito on lopetettava. Tulehduskipulääkkeitä tulee antaa varoen potilaille, joilla on aiemmin ollut maha -suolikanavan sairaus (haavainen paksusuolitulehdus, Crohnin tauti), koska nämä tilanteet voivat pahentua (ks. Myös sivuvaikutukset)
Iäkkäät potilaat: Iäkkäillä potilailla esiintyy enemmän tulehduskipulääkkeisiin liittyviä haittavaikutuksia, erityisesti maha -suolikanavan verenvuotoa ja perforaatiota, jotka voivat olla hengenvaarallisia (ks. Myös Annostus, antotapa ja -aika).
Vakavia ihoreaktioita, joista osa on hengenvaarallisia, mukaan lukien eksfoliatiivinen dermatiitti, Stevens-Johnsonin oireyhtymä ja toksinen epidermaalinen nekrolyysi, on raportoitu hyvin harvoin tulehduskipulääkkeiden käytön yhteydessä (ks. Haittavaikutukset). esiintyy useimmissa tapauksissa ensimmäisen hoitokuukauden aikana. Orudis -hoito on lopetettava heti, kun ihottumaa, limakalvovaurioita tai muita yliherkkyysoireita ilmenee.
Jos sinulla on sydänvaivoja tai aivohalvausongelmia tai jos sinulla on riski näihin tiloihin (esimerkiksi korkea verenpaine, diabetes tai korkea kolesteroli tai tupakointi), keskustele hoidostasi lääkärin tai apteekkihenkilökunnan kanssa.
Jotkut epidemiologiset todisteet viittaavat siihen, että ketoprofeeniin saattaa liittyä suurempi vakavan ruoansulatuskanavan toksisuuden riski kuin muihin tulehduskipulääkkeisiin, erityisesti suurilla annoksilla (ks. Myös Annos, antotapa ja -aika sekä vasta -aiheet).
Raskaus
Ketoprofeenin antoa ei suositella raskauden, imetyksen aikana eikä imeväisikäisenä, vaikka kokeellisesti ei havaittu alkio-sikiötoksisuutta, jos annostus on verrattavissa kliiniseen käyttöön.
Prostaglandiinisynteesin estäminen voi vaikuttaa haitallisesti raskauteen ja / tai alkion / sikiön kehitykseen.Epidemiologisten tutkimusten tulokset osoittavat, että abortin ja sydämen epämuodostumien ja mahalaukun riski lisääntyy prostaglandiinisynteesin estäjän käytön jälkeen. Raskauden alkuvaiheessa. Sydämen epämuodostumien absoluuttinen riski kasvoi alle 1%: sta noin 1,5%: iin. Riskin on arvioitu kasvavan annoksen ja hoidon keston myötä. Eläimillä prostaglandiinisynteesin estäjien antamisen on osoitettu aiheuttavan lisääntyneitä menetyksiä ennen ja jälkeen istutuksen ja alkion ja sikiön kuolleisuutta.
Lisäksi eri epämuodostumien, mukaan lukien sydän- ja verisuonitaudit, esiintyvyyttä on raportoitu enemmän eläimillä, joille on annettu prostaglandiinisynteesin estäjiä organogeenisen jakson aikana.
Raskauden ensimmäisen ja toisen kolmanneksen aikana Orudista tulee käyttää vain tarpeen mukaan. Jos Orudis -valmistetta käyttävät naiset, jotka yrittävät saada lasta tai raskauden ensimmäisen ja toisen kolmanneksen aikana, annoksen tulee olla mahdollisimman pieni ja hoidon keston mahdollisimman lyhyt.
Raskauden kolmannen kolmanneksen aikana kaikki prostaglandiinisynteesin estäjät voivat altistaa sikiön:
- sydän- ja keuhkotoksisuus (valtimokanavan ennenaikainen sulkeminen ja keuhkoverenpainetauti);
- munuaisten vajaatoiminta, joka voi edetä munuaisten vajaatoimintaan oligo-hydroamniosilla;
äiti ja vastasyntynyt raskauden lopussa:
- mahdollinen verenvuodon pidentyminen ja verihiutaleiden vastainen vaikutus, joka voi ilmetä jopa hyvin pienillä annoksilla;
- kohdun supistusten estäminen, joka johtaa synnytyksen viivästymiseen tai pitkittymiseen.
Lääkkeen käyttö lähellä synnytystä voi aiheuttaa muutoksia syntymättömän lapsen pienen verenkierron hemodynamiikassa ja aiheuttaa vakavia seurauksia hengitykselle.
Siksi ketoprofeeni on vasta -aiheinen raskauden kolmannen kolmanneksen aikana.
Ruokinta-aika
Koska tietoja ketoprofeenin erittymisestä äidinmaitoon ei ole saatavilla, sen käyttöä imetyksen aikana ei suositella.
Kysy lääkäriltäsi tai apteekista neuvoa ennen minkään lääkkeen käyttöä.
Vaikutus ajokykyyn ja koneiden käyttökykyyn
Potilaille on kerrottava uneliaisuuden, huimauksen tai kouristuskohtausten mahdollisuudesta, ja heidän tulee välttää ajamista tai toimintaa, joka vaatii erityistä valppautta, jos tällaisia oireita ilmenee.
Annostus ja käyttötapa Orudiksen käyttö: Annostus
Aikuisilla annos on 150-200 mg kerran päivässä (vastaa 3-4 kapselia päivässä) aterioiden yhteydessä.
Iäkkäiden potilaiden hoidossa annoksen on oltava huolellisesti lääkäri, jonka on arvioitava "mahdollinen edellä mainittujen annosten pienentäminen. Vaikka kliiniset ja farmakokineettiset tiedot eivät ole paljastaneet lisääntyneiden sekundaaristen ilmentymien ilmiöitä, on asianmukaista, kuten muidenkin lääkkeiden kohdalla, aloittaa hoito Orudis -kovilla kapseleilla pienimmällä suositellulla annoksella ja ylläpitohoidolla pienimmällä tehokkaalla annoksella.
Suurin päivittäinen annos on 200 mg. Riskin ja hyödyn tasapaino on harkittava huolellisesti ennen hoidon aloittamista 200 mg: n vuorokausiannoksella, eikä suurempia annoksia suositella (ks. Myös varotoimet).
Erityisryhmät
Potilaat, joilla on munuaisten vajaatoiminta ja iäkkäät potilaat On suositeltavaa pienentää aloitusannosta ja harjoittaa ylläpitohoitoa pienimmällä tehokkaalla annoksella. Yksilöllisiä säätöjä voidaan harkita vasta sen jälkeen, kun lääke on siedetty hyvin
Maksan vajaatoimintaa sairastavat potilaat
Tällaisia potilaita on seurattava tarkasti ja hoidettava pienimmällä tehokkaalla vuorokausiannoksella.
Lapset
Ketoprofeenin turvallisuutta ja tehoa ei ole tutkittu lapsilla
Yliannostus Mitä tehdä, jos olet ottanut liikaa Orudista
Yliannostustapauksia on raportoitu enintään 2,5 g: n ketoprofeeniannoksilla. Useimmissa tapauksissa havaitut oireet olivat luonteeltaan hyvänlaatuisia ja rajoittuivat uneliaisuuteen, uneliaisuuteen, pahoinvointiin, oksenteluun ja vatsakipuun.
Ketoprofeenin yliannostukseen ei ole spesifistä vastalääkettä. Jos epäillään vakavaa yliannostusta, suositellaan mahahuuhtelua sekä tuki- ja oireenmukaista hoitoa kuivumisen kompensoimiseksi, munuaisten toiminnan seuraamiseksi ja asidoosin korjaamiseksi.
Munuaisten vajaatoiminnassa hemodialyysi voi olla hyödyllinen lääkkeen poistamiseksi verenkierrosta.
Jos otat vahingossa liiallisen ORUDIS -annoksen, ilmoita siitä välittömästi lääkärillesi tai mene lähimpään sairaalaan.
JOS sinulla on epäilyksiä ORUDIS -laitteen käytöstä, ota yhteys lääkäriisi tai apteekkiin.
Sivuvaikutukset Mitkä ovat Orudisin sivuvaikutukset
Kuten kaikki lääkkeet, myös ORUDIS voi aiheuttaa haittavaikutuksia. Kaikki eivät kuitenkaan niitä saa.
Odotettujen esiintymistiheyksien luokittelu: hyvin yleinen (≥ 1/10), yleinen (≥ 1/100, <1/10), melko harvinainen (≥ 1/1000, <1/100), harvinainen (≥ 1/10000, <1/ 1000), hyvin harvinainen (<1/10000), tuntematon (koska saatavissa oleva tieto ei riitä arviointiin).
Ruoansulatuselimistö:
Yleisimmin havaitut haittavaikutukset ovat luonteeltaan ruoansulatuskanavaa.
Yleiset: dyspepsia, pahoinvointi, vatsakipu, oksentelu
Melko harvinainen: ummetus, ripuli, ilmavaivat, gastriitti
Harvinainen: haavainen stomatiitti, peptiset haavaumat
Tuntematon: paksusuolentulehduksen ja Crohnin taudin paheneminen, ruoansulatuskanavan perforaatio tai verenvuoto, joskus kuolemaan johtava, erityisesti vanhuksilla (ks. Erityisvaroitukset). Melena, hematemesis.
Iho ja ihonalainen kudos:
Melko harvinainen: ihottuma, kutina
Tuntematon: valoherkkyys, hiustenlähtö, nokkosihottuma, angioedeema, rakkulaiset reaktiot, mukaan lukien Stevens-Johnsonin ja Lyellin oireyhtymä, ja toksinen epidermaalinen nekrolyysi (hyvin harvoin)
Hengityselinten rintakehä ja välikarsina:
Harvinainen: astmakohtaukset
Tuntematon: bronkospasmi (erityisesti potilailla, joilla tiedetään olevan yliherkkyys asetyylisalisyylihappo -ASA: lle ja muille tulehduskipulääkkeille), nuha.
Hermosto:
Melko harvinainen: päänsärky, huimaus, uneliaisuus
Harvinainen: parestesia
Tuntematon: kouristukset, dysgeusia
Silmät:
Harvinainen: näön hämärtyminen (ks. Myös Varoitukset ja käyttöön liittyvät varotoimet)
Kuulo ja tasapainoelin
Harvinainen: tinnitus
Munuaiset ja virtsatiet:
Tuntematon: poikkeavuudet munuaisten toimintakokeissa, akuutti munuaisten vajaatoiminta, interstitiaalinen tubulaarinen nefriitti, nefroottinen oireyhtymä.
Maksa ja sappi:
Harvinainen: hepatiitti, kohonneet transaminaasiarvot, kohonnut seerumin bilirubiiniarvo maksasairauden vuoksi.
Veren ja imukudoksen häiriöt:
Harvinainen: verenvuodosta johtuva anemia
Tuntematon: agranulosytoosi, trombosytopenia, luuytimen aplasia.
Immuunijärjestelmän häiriöt
Tuntematon: anafylaktiset reaktiot (shokki mukaan lukien).
Psyykkiset häiriöt:
Tuntematon: mielialan muutokset.
Sydän:
Tuntematon: sydämen vajaatoiminta
Verisuonisto:
Tuntematon: verenpaine, vasodilataatio.
Yleisoireet ja antopaikassa todettavat haitat:
Melko harvinainen: turvotus, väsymys
Diagnostiset testit:
Harvinainen: painonnousu
Pakkausselosteen ohjeiden noudattaminen vähentää haittavaikutusten riskiä. Jos havaitset sellaisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa, kerro niistä lääkärille tai apteekkihenkilökunnalle. Joka tapauksessa tärkeän toissijaisen reaktion esiintyminen edellyttää hoidon välitöntä keskeyttämistä.
Vanhentuminen ja säilyttäminen
Viimeinen käyttöpäivä: katso pakkauksessa mainittu viimeinen käyttöpäivä. Viimeinen käyttöpäivämäärä viittaa tuotteeseen ehjässä pakkauksessa, oikein varastoituna.
VAROITUS: älä käytä lääkettä pakkauksessa mainitun viimeisen käyttöpäivämäärän jälkeen.
Säilytä enintään 30 ° C: n lämpötilassa.
Säilytä ulkopakkauksessa.Suojaa lääke valolta
SÄILYTÄ LÄÄKE POIS LASTEN ULOTTUVILTA.
Lääkkeitä ei tule heittää viemäriin eikä hävittää talousjätteiden mukana. Kysy apteekista, kuinka heittää pois käyttämättömät lääkkeet. Tämä auttaa suojelemaan ympäristöä.
SÄVELLYS
ORUDIS 50 mg kovat kapselit
Yksi kapseli sisältää:
Vaikuttava aine: ketoprofeeni 50 mg.
Apuaineet: magnesiumstearaatti, laktoosi. Kuoren komponentit: rautaoksidi (E172), titaanidioksidi (E171), gelatiini.
LÄÄKEMUOTO JA SISÄLTÖ
Kovat kapselit. "50 mg kovat kapselit" 30 kapselia
Alkuperäinen pakkausseloste: AIFA (Italian lääkevirasto). Sisältö julkaistu tammikuussa 2016. Esitetyt tiedot eivät välttämättä ole ajan tasalla.
Jotta saat käyttöösi uusimman version, on suositeltavaa käyttää AIFA: n (Italian Medicines Agency) verkkosivustoa. Vastuuvapauslauseke ja hyödyllistä tietoa.
01.0 LÄÄKEVALMISTEEN NIMI
ORUDIS
02.0 LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS
ORUDIS 50 mg kovat kapselit
Yksi kapseli sisältää:
Aktiivinen periaate: ketoprofeeni 50 mg.
ORUDIS 100 mg depotkapselit
Yksi kapseli sisältää:
Aktiivinen periaate: ketoprofeeni 100 mg.
ORUDIS 200 mg depotkapselit
Yksi kapseli sisältää:
Aktiivinen periaate: ketoprofeeni 200 mg.
Täydellinen apuaineluettelo, katso kohta 6.1.
03.0 LÄÄKEMUOTO
Kovat kapselit.
Depottabletit, kovat kapselit.
04.0 KLIINISET TIEDOT
04.1 Käyttöaiheet
Orudis 50 mg kovat kapselit se on tarkoitettu nivelreuman, selkärankareuman, akuutin kihdin, eri paikkojen nivelrikon, iskias, radikuliitti, myalgia, bursiitti, jännetulehdus, tenosynoviitti, niveltulehdus, kapsuliitti, murskaukset, nyrjähdykset, dislokaatiot, lihaskyyneleet, imusolmukkeet, pinnallinen tromboflebiitti, hoitoon , kivuliaat tulehdussairaudet hammaslääketieteessä, otolaryngologiassa, urologiassa ja keuhkosairaudessa.
Orudis 100 mg ja 200 mg depotkapselit se on tarkoitettu nivelreuman, nivelrikon, selkärankareuman, akuuttien nivel- ja periartikulaaristen oireiden (bursiitti, kapsuliitti, niveltulehdus, jännetulehdus) hoitoon; kohdunkaulan spondylitis, lannerangan kipu (repiminen, lumbago, iskias, fibrositis), tuki- ja liikuntaelimistön kipuoireyhtymät ja dysmenorrea.
04.2 Annostus ja antotapa
Lääkkeen käyttö on tarkoitettu vain aikuispotilaille.
Kovat kapselit : annos on 150-200 mg vuorokaudessa (vastaa 3-4 kapselia päivässä) jaettuna aterioiden kanssa;
Depottabletit, kovat kapselit : annos on 100-200 mg kerran päivässä potilaan painosta ja oireiden vakavuudesta riippuen. Orudis-depotkapselit on otettava suun kautta aterian jälkeen.
Suurin päivittäinen annos on 200 mg. Hyöty -riskisuhdetta on harkittava huolellisesti ennen hoidon aloittamista 200 mg: n vuorokausiannoksella, eikä suurempia annoksia suositella (ks. Myös kohta 4.4).
Haittavaikutuksia voidaan minimoida käyttämällä pienintä tehokasta annosta mahdollisimman lyhyen hoidon ajan, joka tarvitaan oireiden hallintaan (ks. Kohta 4.4).
Erityisryhmät
Munuaisten vajaatoimintaa sairastavat potilaat ja vanhukset
On suositeltavaa pienentää aloitusannosta ja harjoittaa ylläpitohoitoa pienimmällä tehokkaalla annoksella. Yksilöllisiä säätöjä voidaan harkita vasta sen jälkeen, kun lääke on siedetty hyvin (ks. Kohta 5.2).
Maksan vajaatoimintaa sairastavat potilaat
Tällaisia potilaita on seurattava tarkasti ja hoidettava pienimmällä tehokkaalla vuorokausiannoksella (ks. Kohdat 4.6 ja 5.2).
Lapset
Ketoprofeenin turvallisuutta ja tehoa ei ole tutkittu lapsilla.
04.3 Vasta -aiheet
Orudis on vasta-aiheinen potilaille, joilla on aiemmin esiintynyt yliherkkyysreaktioita, kuten bronkospasmi, astmakohtauksia, nuhaa, nokkosihottumaa tai muita allergisia reaktioita, ketoprofeenille, asetyylisalisyylihapolle (ASA) tai muille ei-steroidisille tulehduskipulääkkeille (NSAID). näillä potilailla on raportoitu vakavia, harvoin kuolemaan johtavia anafylaktisia reaktioita (ks. kohta 4.8).
Orudis on vasta -aiheinen myös seuraavissa tapauksissa:
• yliherkkyys jollekin apuaineelle;
• raskauden kolmannen kolmanneksen aikana
• intensiivisen diureettihoidon aikana;
• vaikea munuaisten vajaatoiminta;
• vaikeat maksan vajaatoiminnan muodot (maksakirroosi, vaikea hepatiitti);
• leukopenia ja trombosytopenia;
• potilaat, joilla on jatkuva verenvuoto
• hemorraginen diateesi;
• vaikea sydämen vajaatoiminta;
• aktiivinen mahahaava tai aiempi ruoansulatuskanavan verenvuoto, haavauma tai perforaatio.
Orudis on yleensä vasta -aiheinen raskauden, imetyksen aikana (ks. Kohta 4.6) ja lasten iässä.
04.4 Varoitukset ja käyttöön liittyvät varotoimet
Orudis 50 mg kapselit sisältävät laktoosia; Potilaiden, joilla on harvinainen perinnöllinen galaktoosi-intoleranssi, Lapp-laktaasin puutos tai glukoosi-galaktoosi-imeytymishäiriö, ei tule käyttää tätä lääkettä.
Orudis-depotkapselit sisältävät sakkaroosia: potilaiden, joilla on harvinaisia fruktoosi-intoleranssi-, glukoosi- / galaktoosi-imeytymishäiriöitä tai sakraasi-isomaltaasin vajaatoimintaa, ei tule käyttää tätä lääkettä.
Varoitukset
Haittavaikutuksia voidaan minimoida käyttämällä pienintä tehokasta annosta mahdollisimman lyhyen hoidon ajan, joka tarvitaan oireiden hallintaan (ks. Kohta 4.2 ja jäljempänä).
Orudiksen samanaikaista käyttöä muiden tulehduskipulääkkeiden kanssa, mukaan lukien selektiiviset syklo-oksigenaasi-2-estäjät, tulee välttää.
Ruoansulatuskanavan verenvuoto, haavauma tai perforaatio: Ruoansulatuskanavan verenvuotoa, haavaumia ja perforaatioita, jotka voivat olla hengenvaarallisia, on raportoitu kaikkien tulehduskipulääkkeiden käytön aikana, milloin tahansa, joko varoitusoireiden kanssa tai ilman tai vakavia ruoansulatuskanavan tapahtumia.
Iäkkäillä potilailla ja potilailla, joilla on ollut haavaumia, erityisesti jos ne ovat monimutkaisia verenvuodon tai perforaation kanssa (ks. Kohta 4.3), ruoansulatuskanavan verenvuotojen, haavaumien tai perforaatioiden riski on suurempi NSAID -annosten kasvaessa. Näiden potilaiden tulee aloittaa hoito pienimmällä mahdollisella annoksella. Suojaavien aineiden (misoprostolin tai protonipumpun estäjien) samanaikaista käyttöä on harkittava näille potilaille ja myös potilaille, jotka käyttävät pieniä annoksia aspiriinia tai muita lääkkeitä, jotka voivat lisätä ruoansulatuskanavan tapahtumien riskiä (ks. Alla ja kohta 4.5).
Potilaiden, joilla on aiemmin ollut ruoansulatuskanavan toksisuutta, erityisesti vanhusten, on ilmoitettava kaikista vatsan oireista (erityisesti ruoansulatuskanavan verenvuodosta) erityisesti hoidon alkuvaiheessa.
Varovaisuutta on noudatettava potilailla, jotka käyttävät samanaikaisesti lääkkeitä, jotka voivat lisätä haavaumien tai verenvuotojen riskiä, kuten suun kautta otettavia kortikosteroideja, antikoagulantteja, kuten varfariinia, selektiivisiä serotoniinin takaisinoton estäjiä tai verihiutaleita estäviä aineita, kuten aspiriinia (ks. Kohta 4.5).
Kun Orudis -hoitoa saavilla potilailla ilmenee ruoansulatuskanavan verenvuotoa tai haavaumia, hoito on lopetettava.
Tulehduskipulääkkeitä on annettava varoen potilaille, joilla on aiemmin ollut maha -suolikanavan sairaus (haavainen paksusuolitulehdus, Crohnin tauti), koska nämä tilanteet voivat pahentua (ks. Kohta 4.8).
Iäkkäät potilaat: Iäkkäillä potilailla esiintyy enemmän tulehduskipulääkkeisiin liittyviä haittavaikutuksia, erityisesti maha -suolikanavan verenvuotoa ja perforaatiota, jotka voivat olla hengenvaarallisia (ks. Kohta 4.2).
Vakavia ihoreaktioita, joista osa kuolemaan johtaneita, mukaan lukien eksfoliatiivinen dermatiitti, Stevens-Johnsonin oireyhtymä ja toksinen epidermaalinen nekrolyysi, on raportoitu hyvin harvoin tulehduskipulääkkeiden käytön yhteydessä (ks. Kohta 4.8). suurempi riski: reaktio alkaa useimmissa tapauksissa ensimmäisen hoitokuukauden aikana. Orudis -hoito on lopetettava heti, kun ihottumaa, limakalvovaurioita tai muita yliherkkyysoireita ilmenee.
Kliiniset tutkimukset ja epidemiologiset tiedot viittaavat siihen, että joidenkin tulehduskipulääkkeiden (etenkin suurina annoksina ja pitkäaikaishoidossa) käyttö voi liittyä jonkin verran suurentuneeseen valtimotromboottisten tapahtumien (esim. Sydäninfarkti tai aivohalvaus) riskiin. On riittävästi tietoja poissulkemiseksi samanlainen riski ketoprofeenille.
Jotkut epidemiologiset todisteet viittaavat siihen, että ketoprofeeniin saattaa liittyä suurempi vakavan ruoansulatuskanavan toksisuuden riski verrattuna muihin tulehduskipulääkkeisiin, erityisesti suurilla annoksilla (ks. Myös kohdat 4.2 ja 4.3).
Varotoimenpiteet
Munuaisten toimintaa on seurattava huolellisesti hoidon alussa potilailla, joilla on sydämen vajaatoiminta, kirroosi ja nefroosi, diureettihoitoa saavilla potilailla, joilla on krooninen munuaisten vajaatoiminta erityisesti iäkkäillä potilailla. munuaisveri, joka johtuu prostaglandiinien estämisestä ja johtaa munuaisten muutoksiin.
Varovaisuutta on noudatettava potilailla, joilla on aiemmin ollut lievä tai kohtalainen hypertensio ja / tai kongestiivinen sydämen vajaatoiminta, koska nesteen kertymistä ja turvotusta on raportoitu tulehduskipulääkkeiden käytön yhteydessä.
Kuten muidenkin ei-steroidisten tulehduskipulääkkeiden kohdalla, ketoprofeenin tulehdusta, kipua lievittävät ja kuumetta alentavat vaikutukset voivat peittää infektion läsnä ollessa infektion etenemisen oireita, kuten kuumetta.
Potilaiden, joiden maksan toimintakokeet ovat heikentyneet tai joilla on aiempi maksasairaus, transaminaasiarvot on arvioitava säännöllisesti, erityisesti pitkäaikaishoidon aikana. Ketoprofeenin käytön yhteydessä on raportoitu keltaisuutta ja hepatiittitapauksia.
Tulehduskipulääkkeiden käyttö voi heikentää naisten hedelmällisyyttä, eikä sitä suositella naisille, jotka aikovat tulla raskaaksi.
Naisilla, joilla on hedelmällisyysongelmia tai joille tehdään hedelmällisyystutkimuksia, hoidon lopettamista on harkittava.
Potilailla, joilla on astma, johon liittyy krooninen nuha, krooninen sinuiitti ja / tai nenän polyypit, on suurempi riski allergioista aspiriinille ja / tai tulehduskipulääkkeille kuin muulla väestöllä. Tämän lääkevalmisteen antaminen voi aiheuttaa astmakohtauksia tai bronkospasmin. aspiriinille tai tulehduskipulääkkeille (ks. kohta 4.3).
Potilaita, joilla on hallitsematon hypertensio, kongestiivinen sydämen vajaatoiminta, todettu iskeeminen sydänsairaus, perifeerinen valtimotauti ja / tai aivoverisuonisairaus, saa hoitaa ketoprofeenilla vain huolellisen harkinnan jälkeen. Samanlaisia näkökohtia on harkittava ennen pitkäaikaishoidon aloittamista potilailla, joilla on sydän- ja verisuonitautien riskitekijöitä (esim. Kohonnut verenpaine, hyperlipidemia, diabetes mellitus, tupakointi).
Jos näköhäiriöitä, kuten näön hämärtymistä, ilmenee, hoito on lopetettava.
Lääkkeen vuorovaikutuksessa arakidonihapon metabolian kanssa astmaatikoilla ja alttiilla henkilöillä voi esiintyä bronkospasmikriisejä ja mahdollisesti sokkia ja muita allergisia ilmiöitä.
04.5 Yhteisvaikutukset muiden lääkevalmisteiden kanssa sekä muut yhteisvaikutukset
YHDISTYKSET EI SUOSITTELE
Muut ei-steroidiset tulehduskipulääkkeet (mukaan lukien selektiiviset syklo-oksigenaasi-2-estäjät ) Ja salisylaatteja suurina annoksina : lisääntynyt ruoansulatuskanavan haavaumien ja verenvuotojen riski.
Antikoagulantit (hepariini ja varfariini) ja verihiutaleiden vastaiset aineet (esim. Tiklopidiini ja klopidogreeli) : lisääntynyt verenvuotoriski (ks. kohta 4.4). Jos samanaikaista käyttöä ei voida välttää, potilaita on seurattava tarkasti
Litium : riski plasman litiumpitoisuuksien noususta, joka voi joskus saavuttaa myrkyllisiä pitoisuuksia litiumin erittymisen vähentyessä munuaisten vuoksi. Tarvittaessa plasman litiumtasoja on seurattava mahdollisella annosmuutoksella NSAID -hoidon aikana ja sen jälkeen.
Metotreksaatti yli 15 mg / viikko annoksina: metotreksaatin aiheuttama hematologisen toksisuuden riski, erityisesti kun sitä annetaan suurina annoksina (> 15 mg / viikko); mahdollisesti johtuen metotreksaatin sitoutumisesta proteiineihin ja heikentyneestä munuaispuhdistumasta. Jos potilaalla on jo ketoprofeenihoito, hoito on lopetettava vähintään 12 tuntia ennen metotreksaatin antamista. Jos ketoprofeeni annetaan metotreksaattihoidon lopussa, on odotettava 12 tuntia ennen antamista.
VAROITUSTA KOSKEVAT YHDISTYKSET
Kortikosteroidit : lisääntynyt ruoansulatuskanavan haavaumien tai verenvuodon riski (ks. kohta 4.4).
Diureetit : potilailla, jotka käyttävät diureetteja, ja erityisesti dehydratoituneilla potilailla, on suuri riski sairastua munuaisten vajaatoimintaan sen seurauksena, että munuaisten verenkierto heikkenee prostaglandiinien estämisen vuoksi. Nämä potilaat on nesteytettävä ennen yhteiskäytön aloittamista ja munuaisten toimintaa on seurattava hoidon alussa (ks. kohta 4.4).
ACE: n estäjät ja angiotensiini II -antagonistit :
Potilailla, joilla on munuaisten vajaatoiminta (esim. Dehydratoituneet potilaat tai iäkkäät potilaat), ACE: n estäjän tai angiotensiini II -antagonistin ja syklo-oksigenaasijärjestelmää estävien aineiden samanaikainen käyttö voi johtaa munuaisten toiminnan heikkenemiseen, mukaan lukien mahdollinen akuutti munuaisten vajaatoiminta Nämä yhteisvaikutukset on otettava huomioon potilailla, jotka käyttävät Orudista samanaikaisesti ACE: n estäjien tai angiotensiini II -antagonistien kanssa. Siksi yhdistelmää on käytettävä varoen, erityisesti iäkkäillä potilailla.
Potilaiden tulee olla riittävästi nesteytettyjä ja munuaisten toimintaa on seurattava samanaikaisen hoidon aloittamisen jälkeen (ks. Kohta 4.4).
Metotreksaatti alle 15 mg / viikko annoksina: yhdistelmähoidon ensimmäisten viikkojen aikana on suoritettava viikoittainen verenkuva. Munuaisten vajaatoiminnan tai iäkkäiden potilaiden seurannan tulisi olla tiheämpää.
Pentoksifylliini : verenvuotoriski on lisääntynyt. Lähempi kliininen seuranta ja verenvuodon seuranta on tarpeen.
HUOMIOITAVAT YHDISTYKSET
Verenpainelääkkeet (beetasalpaajat, angiotensiinikonvertaasientsyymit, diureetit): verenpainetta alentavan riskin riski (tulehduskipulääkkeiden aiheuttama prostaglandiinien vasodilataation esto).
Trombolyytit: lisääntynyt verenvuotoriski.
Probenesidi: Probenesidin samanaikainen käyttö voi merkittävästi pienentää ketoprofeenin plasmapuhdistumaa.
Selektiiviset serotoniinin takaisinoton estäjät (SSRI) : lisääntynyt ruoansulatuskanavan verenvuodon riski (ks. kohta 4.4).
Gemeprost: gemeprostin tehon heikkeneminen.
Kohdunsisäiset ehkäisylaitteet (IUD): laitteen tehokkuus voi heikentyä, mikä johtaa raskauteen.
04.6 Raskaus ja imetys
Ketoprofeenin antoa ei suositella raskauden, imetyksen aikana eikä imeväisikäisenä, vaikka kokeellisesti ei havaittu alkio-sikiötoksisuutta, jos annostus on verrattavissa kliiniseen käyttöön.
Raskaus
Prostaglandiinisynteesin esto voi vaikuttaa haitallisesti raskauteen ja / tai alkion / sikiön kehitykseen.
Epidemiologisten tutkimusten tulokset osoittavat, että keskenmenon ja sydämen epämuodostumien ja mahalaukun riski kasvaa, kun prostaglandiinisynteesin estäjää on käytetty raskauden alkuvaiheessa. Sydämen epämuodostumien absoluuttinen riski kasvoi alle 1 prosentista noin 1,5 prosenttiin. Riski on arvioitu eläimillä prostaglandiinisynteesin estäjien antamisen on osoitettu aiheuttavan lisääntyneitä menetyksiä ennen ja jälkeen istutuksen sekä alkion ja sikiön kuolleisuutta.
Lisäksi eri epämuodostumien, mukaan lukien sydän- ja verisuonitaudit, esiintyvyyttä on raportoitu enemmän eläimillä, joille on annettu prostaglandiinisynteesin estäjiä organogeenisen jakson aikana.
Raskauden ensimmäisen ja toisen kolmanneksen aikana Orudista tulee käyttää vain tarpeen mukaan. Jos Orudis -valmistetta käyttävät naiset, jotka yrittävät saada lasta tai raskauden ensimmäisen ja toisen kolmanneksen aikana, annoksen tulee olla mahdollisimman pieni ja hoidon keston mahdollisimman lyhyt.
Raskauden kolmannen kolmanneksen aikana kaikki prostaglandiinisynteesin estäjät voivat altistaa sikiön:
• sydän- ja keuhkotoksisuus (valtimokanavan ennenaikainen sulkeminen ja keuhkoverenpainetauti);
• munuaisten vajaatoiminta, joka voi edetä munuaisten vajaatoimintaan oligo-hydroamniosilla;
äiti ja vastasyntynyt raskauden lopussa:
• mahdollinen verenvuodon pidentyminen ja verihiutaleiden vastainen vaikutus, joka voi ilmetä jopa hyvin pienillä annoksilla;
• kohdun supistusten esto, joka johtaa synnytyksen viivästymiseen tai pitkittymiseen.
Lääkkeen käyttö lähellä synnytystä voi aiheuttaa muutoksia syntymättömän lapsen pienen verenkierron hemodynamiikassa ja aiheuttaa vakavia seurauksia hengitykselle.
Siksi ketoprofeeni on vasta -aiheinen raskauden kolmannen kolmanneksen aikana.
Ruokinta-aika
Koska tietoja ketoprofeenin erittymisestä äidinmaitoon ei ole saatavilla, sen käyttöä imetyksen aikana ei suositella.
04.7 Vaikutus ajokykyyn ja koneiden käyttökykyyn
Potilaille on kerrottava uneliaisuuden, huimauksen tai kouristuskohtausten mahdollisuudesta, ja heidän tulee välttää ajamista tai toimintaa, joka vaatii erityistä valppautta, jos tällaisia oireita ilmenee.
04.8 Haittavaikutukset
Kuten kaikki lääkkeet, myös ORUDIS voi aiheuttaa haittavaikutuksia. Kaikki eivät kuitenkaan niitä saa.
Odotettujen esiintymistiheyksien luokittelu: hyvin yleinen (≥1 / 10), yleinen (≥1 / 100,
Seuraavia reaktioita on raportoitu ketoprofeenin käytön yhteydessä aikuisilla
Ruoansulatuselimistö
Yleisimmin havaitut haittavaikutukset ovat luonteeltaan ruoansulatuskanavaa.
Yleiset: dyspepsia, pahoinvointi, vatsakipu, oksentelu.
Melko harvinainen: ummetus, ripuli, ilmavaivat, gastriitti
Harvinainen: haavainen stomatiitti, peptiset haavaumat
Tuntematon: paksusuolentulehduksen ja Crohnin taudin paheneminen, ruoansulatuskanavan perforaatio tai verenvuoto, joskus kuolemaan johtava, erityisesti vanhuksilla (ks. Kohta 4.4). Melena, hematemesis.
Iho ja ihonalainen kudos:
Melko harvinainen: ihottuma, kutina
Tuntematon: valoherkkyys, hiustenlähtö, nokkosihottuma, angioedeema, rakkulaiset reaktiot, mukaan lukien Stevens-Johnsonin ja Lyellin oireyhtymä, ja toksinen epidermaalinen nekrolyysi (hyvin harvoin).
Hengityselinten rintakehä ja välikarsina:
Harvinainen: astmakohtaukset,
Tuntematon: bronkospasmi (erityisesti potilailla, joilla tiedetään olevan yliherkkyys asetyylisalisyylihappo -ASA: lle ja muille tulehduskipulääkkeille), nuha.
Hermosto:
Melko harvinainen: päänsärky, huimaus, uneliaisuus
Harvinainen: parestesia
Tuntematon: kouristukset, dysgeusia.
Silmän patologia:
Harvinainen: näön hämärtyminen (ks. Kohta 4.4).
Korvan ja labyrintin patologia:
Harvinainen: tinnitus.
Munuaiset ja virtsatiet:
Tuntematon: poikkeavuudet munuaisten toimintakokeissa, akuutti munuaisten vajaatoiminta, interstitiaalinen tubulaarinen nefriitti, nefroottinen oireyhtymä.
Maksa ja sappi:
Harvinainen: hepatiitti, kohonneet transaminaasiarvot, kohonnut seerumin bilirubiiniarvo maksasairauden vuoksi.
Veren ja imukudoksen häiriöt:
Harvinainen: verenvuodosta johtuva anemia
Tuntematon: agranulosytoosi, trombosytopenia, luuytimen aplasia.
Immuunijärjestelmän häiriöt:
Tuntematon: anafylaktiset reaktiot (shokki mukaan lukien).
Psyykkiset häiriöt:
Tuntematon: mielialan muutokset.
Sydämen patologiat:
Tuntematon: sydämen vajaatoiminta
Verisuonipatologiat:
Tuntematon: verenpaine, vasodilataatio.
Yleisoireet ja antopaikassa todettavat haitat:
Melko harvinainen: turvotus, väsymys
Diagnostiset testit:
Harvinainen: painonnousu
Kliiniset tutkimukset ja epidemiologiset tiedot viittaavat siihen, että joidenkin tulehduskipulääkkeiden (etenkin suurina annoksina ja pitkäaikaishoidossa) käyttö saattaa liittyä jonkin verran suurentuneeseen valtimotromboottisten tapahtumien (esim. Sydäninfarkti tai aivohalvaus) riskiin (ks. Kohta 4.4).
04.9 Yliannostus
Yliannostustapauksia on raportoitu enintään 2,5 g: n ketoprofeeniannoksilla. Useimmissa tapauksissa havaitut oireet olivat luonteeltaan hyvänlaatuisia ja rajoittuivat uneliaisuuteen, uneliaisuuteen, pahoinvointiin, oksenteluun ja vatsakipuun.
Ketoprofeenin yliannostukseen ei ole spesifistä vastalääkettä. Jos epäillään vakavaa yliannostusta, suositellaan mahahuuhtelua sekä tuki- ja oireenmukaista hoitoa kuivumisen kompensoimiseksi, munuaisten toiminnan seuraamiseksi ja asidoosin korjaamiseksi.
Munuaisten vajaatoiminnassa hemodialyysi voi olla hyödyllinen lääkkeen poistamiseksi verenkierrosta.
Koska Orudis-depotkapselit ovat säännelty take away -valmiste, on todennäköistä olettaa, että ketoprofeeni imeytyy edelleen 16 tunnin ajan sen ottamisesta.
Jos potilas viedään lääkärin vastaanotolle lyhyen ajan kuluessa liiallisten annosten ottamisesta, mahahuuhtelu on suoritettava, jotta mahassa olevat rakeet, jotka ovat tunnistettavissa mahalaukun sisällöstä, saadaan huuhdeltavaksi. Hoito on kuitenkin oireenmukaista ja tukevaa.
Aktiivihiilen antamista on myös harkittava yritettäessä vähentää hitaasti vapautuvan ketoprofeenin imeytymistä.
05.0 FARMAKOLOGISET OMINAISUUDET
05.1 Farmakodynaamiset ominaisuudet
Farmakoterapeuttinen ryhmä: ei-steroidiset tulehdus- ja reumalääkkeet.
ATC -koodi: M01AE03.
Ketoprofeeni on tulehdusta ja kipua lievittävä lääke, joka kuuluu tulehduskipulääkkeiden farmakoterapeuttiseen ryhmään.
Tulehdusta ehkäisevä vaikutus liittyy neljään hyvin dokumentoituun toimintamekanismiin: lysosomaalisen kalvon stabilointi; prostaglandiinisynteesin estäminen; antiradykiniiniaktiivisuus; verihiutaleiden toimintaa.
Eläimillä ja osittain myös terveillä vapaaehtoisilla tehdyt farmakologiset tutkimukset viittaavat siihen, että kipua lievittävä vaikutus on kaksinkertainen.
On itse asiassa todennäköistä, että nyt tunnetun perifeerisen aktiivisuuden ohella ketoprofeeni toimii myös kipua lievittävän vaikutuksensa keskusmekanismin kautta. ei-opioidi joissa on mukana supraspinaalisia rakenteita, kuten NMDA: n kaltaiset glutamaattireseptorit, jotka indusoivat keskusherkistymistä, johon osallistuvat erilaiset biokemialliset välittäjät, kuten aine P, 5-HT, keskushermostossa olevien prostaglandiinien lisäksi.
Tämä erikoinen kipulääkeprofiili selittäisi ketoprofeenin kipua lievittävän vaikutuksen nopeuden klinikalla eri akuuteissa kivuliaisissa olosuhteissa, mikä ei muuten olisi selitettävissä ainoalla tähän mennessä tunnetulla perifeerisellä mekanismilla.
05.2 Farmakokineettiset ominaisuudet
Orudis-depotkapselit ovat pH-säädellysti vapauttavia ketoprofeenivalmisteita, jotka on suunniteltu tarvittavan terapeuttisen annoksen antamiseen kerran päivässä.
Imeytyminen
Ketoprofeeni imeytyy nopeasti ja täydellisesti ruoansulatuskanavasta. Maksimipitoisuudet plasmassa saavutetaan 60-90 minuutin kuluessa oraalisen annon jälkeen (45-60 minuuttia peräsuolen annon jälkeen).
Kun sitä annetaan ruoan kanssa, imeytymisnopeus hidastuu siten, että huippupitoisuudet plasmassa (Cmax) ovat pienentyneet ja viivästyneet. kokonaisbiosaatavuus ei kuitenkaan muutu.
Depotkapselilla huippupitoisuus plasmassa saavutetaan 6-8 tunnin kuluttua. Biosaatavuus pieneni 13%, kun tätä formulaatiota annettiin korkeakaloristen elintarvikkeiden kanssa.
Jakelu
Lääke sitoutuu 99% plasman proteiineihin.
Ketoprofeeni leviää nivelnesteeseen ja nivelsisäiseen, kapseli-, nivel- ja jännekudokseen. Ketoprofeeni läpäisee veri -aivot ja istukan. Plasman eliminaation puoliintumisaika on noin 2 tuntia. Jakautumistilavuus on noin 7 litraa.
Pitkävaikutteinen formulaatio: Kun tasanko on saavutettu (viides ja kahdestoista tunti), ketoprofeenipitoisuudet laskevat ja näennäinen puoliintumisaika on 3-4 tuntia. Kerääntymistä ei havaittu toistuvan annon jälkeen.
Biotransformaatio
Ketoprofeenin biotransformaatiolle on tunnusomaista kaksi pääreittiä, hydroksylaatio ja konjugointi glukuronihapon kanssa, joista toinen on ihmisen tärkein reitti. Erittyminen muuttumattomassa muodossa on vähäistä (alle 1%). Lähes kaikki lääke erittyy muuttumattomana virtsa, 65-85% annetusta annoksesta on glukuronisoitu.
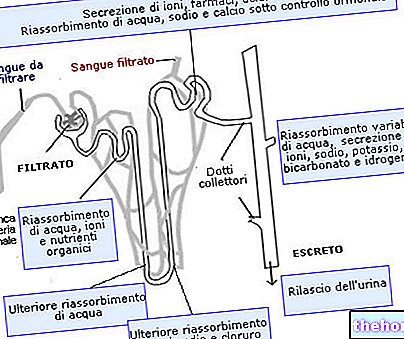
Erittyminen
50% annoksesta erittyy virtsaan 6 tunnin kuluessa annostelusta. Noin 75-90% annoksesta erittyy pääasiassa virtsaan 5 päivän kuluessa annostelusta. Eliminaatio on minimaalista (1-8%).
Erityisryhmät
Iäkkäät potilaat
Ketoprofeenin imeytyminen ei vaikuta; puoliintumisaika pidentyy (3 tuntia) ja munuaisten ja plasman puhdistuma vähenee.
Potilaat, joilla on munuaisten vajaatoiminta
Munuaisten ja plasman puhdistuma pienenee ja puoliintumisaika pitenee munuaisten vajaatoiminnan vakavuuden vuoksi.
Maksan vajaatoimintaa sairastavat potilaat
Plasman puhdistumassa ja eliminaation puoliintumisajassa ei ole merkittäviä muutoksia. Vapaa osuus on kuitenkin noin kaksinkertaistunut.
05.3 Prekliiniset tiedot turvallisuudesta
Toksikologiset testit ovat osoittaneet ketoprofeenin alhaisen toksisuuden ja korkean terapeuttisen indeksin: LD50 rotilla, per os, on 165 mg / kg, hiirillä eri antoreiteillä 365 - 662 mg / kg.
Prekliinisistä tiedoista ei ole muita lisätietoja kuin ne, jotka on jo raportoitu muualla tässä valmisteyhteenvedossa (ks. Kohta 4.6).
06.0 FARMASEUTTISET TIEDOT
06.1 Apuaineet
ORUDIS 50 mg kovat kapselit
Magnesiumstearaatti, laktoosi.
Kotelon osat: rautaoksidi (E172), titaanidioksidi (E171), gelatiini.
ORUDIS 100 mg depotkapselit
sakkaroosi, tärkkelys, kolloidinen piidioksidi, sellakka, etyyliselluloosa, talkki.
Kotelon osat: erytrosiini (E127), kiiltosininen V (E131), titaanidioksidi (E171), gelatiini.
ORUDIS 200 mg depotkapselit
sakkaroosi, tärkkelys, kolloidinen piidioksidi, sellakka, etyyliselluloosa, talkki.
Kotelon osat: erytrosiini (E127), titaanidioksidi (E171), gelatiini.
06.2 Yhteensopimattomuus
Ei raportoitu.
06.3 Voimassaoloaika
2 vuotta.
06.4 Säilytys
ORUDIS 50 mg kovat kapselit
Säilytä enintään 30 ° C: n lämpötilassa.
Säilytä ulkopakkauksessa.Suojaa lääke valolta.
ORUDIS 100 mg depotkapselit
ORUDIS 200 mg depotkapselit
Säilytä alkuperäispakkauksessa suojataksesi lääkettä valolta.
06.5 Välipakkauksen luonne ja pakkauksen sisältö
Alumiini / PVC -läpipainopakkaus
"50 mg kovat kapselit" 30 kapselia
"100 mg depotkapselit, kovat" 30 kapselia
"200 mg depotkapselit" 30 kapselia
06.6 Käyttö- ja käsittelyohjeet
Ei mitenkään erityisesti.
07.0 MYYNTILUVAN HALTIJA
Sanofi S.p.A. - Viale L.Bodio, 37 / B - Milano
08.0 MYYNTILUVAN NUMERO
50 mg kovat kapselit - 30 cps: A.I.C. n. 023183027
100 mg depotkapselit - 30 cps: A.I.C. n. 023183181
200 mg depotkapselit - 30 cps: A.I.C. n. 023183193
09.0 MYYNTILUVAN TAI UUDISTAMISPÄIVÄMÄÄRÄ
Ensimmäinen valtuutus:
kovat kapselit helmikuu 1979
Depottabletit, kovat kapselit kesäkuu 1998
Valtuutuksen uusiminen: kesäkuu 2010
10.0 TEKSTIN MUUTTAMISPÄIVÄMÄÄRÄ
Lokakuuta 2014