Mitä Rasilez HCT on?
Rasilez HCT on lääke, joka sisältää vaikuttavina aineina aliskireenia ja hydroklooritiatsidia. Sitä on saatavana soikeina tabletteina (valkoinen: 150 mg aliskireenia ja 12,5 mg hydroklooritiatsidia; kellertävä: 150 mg aliskireenia ja 25 mg hydroklooritiatsidia; vaaleanpunainen: 300 mg aliskireenia ja 12,5 mg hydroklooritiatsidia; keltainen kirkas: 300 mg aliskireenia ja 25 mg hydroklooritiatsidia ).
Mihin Rasilez HCT: tä käytetään?
Rasilez HCT on tarkoitettu essentiaalisen verenpaineen (korkean verenpaineen) hoitoon aikuisilla. Termi "välttämätön" tarkoittaa, että verenpaineen syy on tuntematon.
Rasilez HCT -valmistetta käytetään potilaille, joiden verenpainetta ei saada riittävästi hallintaan pelkästään aliskireenilla tai hydroklooritiatsidilla. Sitä voidaan käyttää myös potilailla, joiden verenpaine on riittävästi hallinnassa aliskireenin ja hydroklooritiatsidin kanssa erillisinä tabletteina korvaamaan samat annokset molempia vaikuttavia aineita.
Lääkettä saa vain reseptillä.
Miten Rasilez HCT: tä käytetään?
Suositeltu Rasilez HCT -annos on yksi tabletti vuorokaudessa. Lääke tulee ottaa kevyen aterian yhteydessä, mieluiten samaan aikaan joka päivä, välttäen sen ottamista greippimehun kanssa. Annos riippuu potilaan aiemmin ottamista aliskireenin ja / tai hydroklooritiatsidin annoksista.
Potilaiden, jotka ovat aikaisemmin käyttäneet vain aliskireenia tai hydroklooritiatsidia, on ehkä otettava nämä kaksi tablettia ja muutettava annosta ennen Rasilez HCT -hoitoon siirtymistä. Rasilez HCT: n ottamisen jälkeen 2–4 viikon ajan annosta voidaan suurentaa potilailla, joiden verenpaine pysyy hallinnassa.
Potilailla, joilla on riittävästi hoitoa kahdella vaikuttavalla aineella, Rasilez HCT -annoksen tulee sisältää samat aliskireenin ja hydroklooritiatsidin annokset kuin potilas on aiemmin käyttänyt.
Rasilez HCT -valmistetta on käytettävä varoen potilailla, joilla on maksavaivoja, eikä sitä saa käyttää potilailla, joilla on vakavia maksa- tai munuaisongelmia.
Miten Rasilez HCT vaikuttaa?
Rasilez HCT sisältää kahta vaikuttavaa ainetta, aliskireenia ja hydroklooritiatsidia.
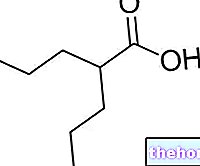
Aliskireeni on reniinin estäjä. Se estää reniini -nimisen ihmisen entsyymin toimintaa, joka osallistuu kehon angiotensiini I -nimisen aineen tuotantoon. Angiotensiini I muuttuu angiotensiini II -hormoniksi, joka on voimakas verisuonia supistava aine (
verisuonten supistuminen). Kun angiotensiini I: n tuotanto estyy, angiotensiini I- ja angiotensiini II -tasot laskevat. Tämä aiheuttaa verisuonten laajenemista (verisuonten laajenemista) ja siten verenpaineen laskua.
Hydroklooritiatsidi on diureetti, toinen verenpainelääkitys, joka lisää virtsaneritystä, vähentää nesteen määrää veressä ja alentaa siten verenpainetta.
Näiden kahden vaikuttavan aineen yhdistelmällä on lisävaikutus, joka alentaa verenpainetta enemmän kuin kaksi lääkettä erikseen. Alentamalla verenpainetta verenpaineen, kuten aivohalvauksen, riski pienenee.
Miten Rasilez HCT: tä on tutkittu?
Pelkästään Aliskirenille on myönnetty Euroopan unionin (EU) lisenssi elokuusta 2007 lähtien nimillä Rasilez, Enviage, Sprimeo, Tekturna ja Riprazo. Yhtiö esitti aliskireenin arvioinnissa käytetyt tiedot ja julkaistusta kirjallisuudesta Rasilez HCT -hakemuksen tueksi sekä lisätutkimuksista saadut tiedot.
Kaiken kaikkiaan yritys esitti yhdeksän päätutkimuksen tulokset, joihin osallistui noin 9 000 essentiaalista hypertensiota sairastavaa potilasta. Suurin osa tutkimuksista sisälsi potilaita, joilla oli lievä tai kohtalainen hypertensio, ja yksi tutkimus vaikeaa verenpainetta sairastavilla potilailla. Tutkimuksissa verrattiin aliskireenin ja hydroklooritiatsidin yhdistelmää lumelääkkeeseen (nukkehoito), aliskireenin tai hydroklooritiatsidin kanssa erikseen tai muiden verenpainelääkkeiden (valsartaani, irbesartaani, lisinopriili tai amlodipiini) kanssa. Tutkimusten kesto vaihteli kahdeksasta viikosta vuoteen, ja tehon pääasiallinen mitta oli verenpaineen muutos sykkeen lepovaiheessa (diastolinen paine) tai sydänontelojen supistusvaiheen aikana (systolinen paine).
Kolme lisätutkimusta suoritettiin osoittamaan, että vaikuttavat aineet imeytyivät elimistöön samalla tavalla kuin ne imeytyivät erillisinä tabletteina ja Rasilez HCT: n muodossa.
Mitä hyötyä Rasilez HCT: stä on havaittu tutkimuksissa?
Rasilez HCT alensi verenpainetta lumelääkettä tehokkaammin. Potilailla, joiden verenpainetta ei saatu riittävästi hallintaan pelkällä aliskireenilla tai hydroklooritiatsidilla, vaihtaminen yhdistelmään johti suurempiin verenpaineen laskuihin kuin pelkkä vaikuttava aine.
Mitä riskejä Rasilez HCT: hen liittyy?
Yleisin Rasilez HCT: n raportoitu sivuvaikutus (1–10 potilaalla 100: sta) on ripuli. Täydellinen luettelo Rasilez HCT: n ilmoitetuista sivuvaikutuksista on pakkausselosteessa.
Rasilez HCT -valmistetta ei saa antaa henkilöille, jotka voivat olla yliherkkiä (allergisia) aliskireenille, hydroklooritiatsidille tai jollekin muulle aineelle tai sulfonamideille. Sitä ei saa käyttää potilailla, joilla on angioedeema (ihon alla oleva turvotus) aliskireenin ottamisen jälkeen, joilla on vaikeita munuais- tai maksavaivoja tai joiden kaliumpitoisuus on liian alhainen tai kalsiumpitoisuus liian korkea. Sitä ei saa ottaa yhdessä siklosporiinin kanssa (immuunijärjestelmän toimintaa heikentävä lääke) tai muita lääkkeitä, jotka hidastavat aliskireenin aineenvaihduntaa kehossa, kuten kinidiini (käytetään epäsäännöllisen sydämenlyönnin korjaamiseen) tai verapamiili (käytetään sydänvaivojen hoitoon). naisilla, jotka ovat yli kolme kuukautta raskaana tai imettävät Sitä ei suositella raskauden kolmen ensimmäisen kuukauden aikana.
Miksi Rasilez HCT on hyväksytty?
Lääkevalmistekomitea (CHMP) katsoi, että Rasilez HCT: n hyödyt ovat sen riskejä suuremmat essentiaalisen verenpaineen hoidossa aikuisilla, joiden verenpainetta ei saada riittävästi hallintaan pelkällä aliskireenilla tai hydroklooritiatsidilla tai joka on riittävästi hallinnassa aliskireenilla ja hydroklooritiatsidilla Siksi komitea suositteli myyntiluvan myöntämistä Rasilez HCT: lle.
Lisätietoja Rasilez HCT: stä
Euroopan komissio myönsi 16. tammikuuta 2009 Novartis Europharm Limitedille Rasilez HCT: n myyntiluvan, joka on voimassa koko Euroopan unionin alueella.
Jos haluat nähdä Rasilez HCT EPAR -EPAR -version kokonaisuudessaan, napsauta tätä.
Tämän yhteenvedon viimeisin päivitys: 12-2008
Tällä sivulla julkaistut tiedot Rasilez HCT: stä voivat olla vanhentuneita tai puutteellisia. Jos haluat käyttää näitä tietoja oikein, katso Vastuuvapauslauseke ja hyödyllisiä tietoja -sivu.