Vaikuttavat aineet: fenobarbitaali
Luminale® 200 mg / ml injektioneste, liuos lihakseen
Luminale® 100 mg tabletit
Luminale -pakkausselosteita on saatavana seuraaville pakkauksille: - Luminale® 200 mg / ml injektioneste, liuos lihakseen, Luminale® 100 mg tabletit
- Luminale® 15 mg tabletit
Käyttöaiheet Miksi Luminalea käytetään? Mitä varten se on?
Farmakoterapeuttinen ryhmä
Barbituraatit
Terapeuttiset käyttöaiheet
Luminale® on tarkoitettu pääasiassa yleiseksi rauhoittavaksi lääkkeeksi, erityisesti epilepsiaan ja kaikkiin pitkäaikaista sedaatiota vaativiin tiloihin. Sitä voidaan käyttää unilääkkeenä ja kroonisen barbiturismin vieroituksessa.
Vasta -aiheet Kun Luminale -valmistetta ei tule käyttää
Yliherkkyys barbituraateille, porfyria, munuaisten ja maksan vajaatoiminta, vaikea sydänsairaus, akuutti alkoholimyrkytys, kipulääkkeet, unilääkkeet.
Käyttöä koskevat varotoimet Mitä sinun on tiedettävä, ennen kuin otat Luminale -valmistetta
Fenobarbitaali voi aiheuttaa riippuvuutta. Jatkuva hoito indusoi maksaentsyymien muodostumista, jotka nopeuttavat tiettyjen lääkkeiden, kuten antikoagulanttien, joidenkin antibioottien, lisämunuaisen steroidien, aineenvaihduntaa.
Hypericum perforatum -valmisteita ei tule käyttää samanaikaisesti fenobarbitaalia sisältävien lääkevalmisteiden kanssa, koska fenobarbitaalin plasmapitoisuuden alenemisen ja terapeuttisen tehon heikkenemisen riski on olemassa (ks. Yhteisvaikutukset).
Hoidon äkillinen lopettaminen epilepsiapotilailla voi aiheuttaa epileptisen tilan.
Potilaille, jotka voivat tulla raskaaksi tai ovat hedelmällisessä iässä, on annettava erikoisneuvontaa.
Epilepsialääkityksen tarve on arvioitava uudelleen, kun potilas suunnittelee raskautta.
Synnynnäisten vikojen riski kasvaa 2-3 kertaa epilepsialääkettä saaneiden äitien jälkeläisillä, joista yleisimmin raportoitu huulten halkeama, sydän- ja verisuonivirheet ja hermoputken viat.
Moniterapiaan epilepsialääkkeillä voi liittyä suurempi synnynnäisten epämuodostumien riski kuin monoterapiaan. Siksi on tärkeää, että monoterapiaa harjoitetaan aina kun mahdollista. Epilepsialääkityksen äkillistä lopettamista ei pidä harjoittaa, koska kouristusten uusiutuminen voi aiheuttaa vakavia seurauksia sekä äidille että vauvalle.
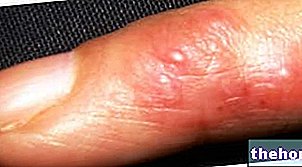
Hengenvaarallisia ihottumia (Stevens-Johnsonin oireyhtymä, toksinen epidermaalinen nekrolyysi) on raportoitu Luminalen käytön yhteydessä.Nämä näyttävät aluksi pyöreiltä punaisilta täpliltä tai pyöreiltä laastareilta, joihin liittyy usein rakkuloita rungon keskiosassa.
Muita huomioitavia merkkejä ovat haavaumat suussa, kurkussa, nenässä, sukupuolielimissä ja sidekalvotulehdus (punoittavat ja turvonneet silmät)
Näihin hengenvaarallisiin ihottumiin liittyy usein flunssan kaltaisia oireita. Ihottuma voi edetä laajojen rakkuloiden tai ihon kuorinnan kehittymiseen.
Suurin riski vakavista ihoreaktioista ilmenee ensimmäisten 8 hoitoviikon aikana.
Jos sinulle on kehittynyt Stevens-Johnsonin oireyhtymä tai myrkyllinen epidermaalinen nekrolyysi Luminalen käytön aikana, Luminale-valmistetta ei saa enää käyttää.
Jos sinulle kehittyy ihottumaa tai näitä iho -oireita, lopeta Luminalen käyttö, ota välittömästi yhteys lääkäriin ja kerro hänelle, että käytät tätä lääkettä.
Yhteisvaikutukset Mitkä lääkkeet tai elintarvikkeet voivat muuttaa Luminalen vaikutusta
Fenobarbitaalin teho voi heikentyä, jos samanaikaisesti annetaan Hypericum perforatum -pohjaisia valmisteita.Tämä johtuu siitä, että Hypericum perforatum -pohjaiset valmisteet indusoivat lääkkeiden aineenvaihdunnasta vastaavia entsyymejä, joten niitä ei pidä antaa samanaikaisesti fenobarbitaalin kanssa. Induktiovaikutus voi jatkua vähintään 2 viikon ajan Hypericum perforatum -valmisteen käytön lopettamisen jälkeen. Jos potilas käyttää Hypericum perforatum -valmisteita samanaikaisesti, veren fenobarbitaalipitoisuuksia on seurattava ja hoito Hypericum perforatum -valmisteilla lopetettava. Veren fenobarbitaalipitoisuudet voivat nousta, kun Hypericum perforatum lopetetaan. Fenobarbitaalin annostusta on ehkä muutettava.
Alkoholin vaikutus tehostuu ja alkoholijuomien nauttimista tulee rajoittaa Yhdistelmä muiden psykotrooppisten lääkkeiden ja antihistamiinien kanssa vaatii erityistä varovaisuutta ja valppautta lääkäriltä välttääkseen vuorovaikutuksen odottamattomia haittavaikutuksia.
Varoitukset On tärkeää tietää, että:
Fenobarbitaalihoito vähentää huomiota ja pidentää refleksien kestoa: potilaita on varoitettava tästä, jotta he eivät välttämättä aja autoa tai suorita toimintoja, jotka vaativat valppautta koskemattomuutensa vuoksi.
Pieni määrä potilaita, joita hoidetaan epilepsialääkkeillä, kuten Luminale, ovat kehittäneet ajatuksia itsensä vahingoittamisesta tai itsemurhasta. Aina kun tällaisia ajatuksia ilmenee, ota heti yhteys lääkäriisi.
Annostus ja käyttötapa Luminalen käyttö: Annostus
- LUMINALE® 200 mg / ml injektioneste, liuos, lihakseen, 200 mg / ml Fenobarbitaalin INJEKTIOPULLOT (219 mg natriumsuolan muodossa): ellei lääkäri toisin määrää, aikuisilla yksi ampulli päivässä lihakseen. Älä ylitä 400 mg 24 tunnissa. Lapsilla 10 mg 1 vuoden ikävuodesta alkaen.
- LUMINALE® 100 mg tabletit: rauhoittavana 50-100 mg (puoli / yksi tabletti) päivässä. Antikonvulsanttina aikuisilla 100-300 mg (1-3 tablettia) päivässä 2-3 kertaa. Lapsilla annoksia on pienennettävä (100 mg: sta 20 mg: aan) iän ja painon mukaan, ja Luminale® 15 mg -tabletit on tarkoitettu käytettäväksi.
Vaikeassa unettomuudessa 50-200 mg (puoli tai 2 tablettia) illalla, tunti ennen nukkumaanmenoa. Tabletit voidaan liuottaa pieneen veteen tai mahdollisesti lisätä ruokaan. Iäkkäiden potilaiden hoidossa annoksen on oltava huolellisesti lääkäri, jonka on arvioitava edellä mainittujen annosten mahdollinen pienentäminen.
Yliannostus Mitä tehdä, jos olet ottanut liikaa Luminalea
Akuutin barbituraattimyrkytyksen hoito edellyttää välitöntä mahahuuhtelua, jos potilaan tila sen sallii.
Jo imeytynyt lääke voidaan poistaa pakotetulla diureesilla ja virtsan alkalisoinnilla. Vaikeissa tapauksissa hemodialyysi on hyödyllinen ja hengitystä on ehkä ohjattava mekaanisesti Antibioottien antaminen on välttämätöntä keuhkojen komplikaatioiden välttämiseksi.
Sivuvaikutukset Mitkä ovat Luminalen sivuvaikutukset
Iho: harvinaisia allergisia iho -oireita. Harvinaisia multiformisen punoituksen, Stevens-Johnsonin oireyhtymän ja toksisen epidermaalisen nekrolyysin (Lyellin oireyhtymä) tapauksia on raportoitu.
Maksa ja sappi: harvinaisia toksisen hepatiitin tapauksia.
Hematologiset: harvinaiset leukopenia, agranulosytoosi, trombosytopenia ja purppura. Fenobarbitaalilla hoidettujen äitien vastasyntyneillä voi esiintyä K -vitamiinihoitoon vaikuttavaa hypotrombinemiaa. Kroonisten hoitojen aikana voi esiintyä folaattiherkkää megaloblastista anemiaa ja osteomalasiaa, joka reagoi D-vitamiinihoitoon.
Keskushermosto: joillakin potilailla niitä voi esiintyä harvoin: jännitystä, levottomuutta ja deliriumia. Lapsipotilailla voi esiintyä hyperaktiivisuuden ilmenemismuotoja. Sedaatio, ataksia, nystagmus ja henkinen sekavuus voivat ilmetä etenkin vanhuksilla suurien annosten jälkeen.
Luminalen käytön yhteydessä on raportoitu hengenvaarallisia ihottumia (Stevens-Johnsonin oireyhtymä, toksinen epidermaalinen nekrolyysi) .Esiintymistiheys: hyvin harvinainen
Luusairauksia, mukaan lukien osteopenia ja osteoporoosi (luiden oheneminen) ja murtumia, on raportoitu. Ota yhteys lääkäriisi tai apteekkiin, jos olet käyttänyt epilepsialääkettä pitkään tai jos sinulla on aiemmin ollut osteoporoosia tai jos käytät steroideja.
Potilasta kehotetaan ilmoittamaan hoitavalle lääkärille mahdollisista haittavaikutuksista, joita ei ole kuvattu.
Vanhentuminen ja säilyttäminen
Varoitus: älä käytä lääkettä pakkauksessa mainitun viimeisen käyttöpäivämäärän jälkeen.
Sävellys
1 injektiopullo sisältää:
Vaikuttava aine: fenobarbitaali (natriumsuolan muodossa 219 mg) 200 mg.
Apuaineet: propyleeniglykoli, etanoli, injektionesteisiin käytettävä vesi.
1 tabletti sisältää:
Vaikuttava aine: fenobarbitaali 100 mg.
Apuaineet: talkki, povidoni, steariinihappo, maissitärkkelys.
Lääkemuoto
- Laatikossa 10 ampullia
- 20 tabletin laatikko
Lähdepakkaus: AIFA (Italian lääkevirasto). Sisältö julkaistu tammikuussa 2016. Esitetyt tiedot eivät välttämättä ole ajan tasalla.
Jotta saat käyttöösi uusimman version, on suositeltavaa käyttää AIFA: n (Italian Medicines Agency) verkkosivustoa. Vastuuvapauslauseke ja hyödyllistä tietoa.
01.0 LÄÄKEVALMISTEEN NIMI
LUMINAALINEN
02.0 LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS
1 1 ml: n ampulli sisältää:
Vaikuttava aine: FENOBARBITAL (natriumsuolan muodossa 219 mg) 200 mg
Yksi 170 mg: n tabletti sisältää
Vaikuttava aine: FENOBARBITAL 100 mg
03.0 LÄÄKEMUOTO
- injektiopullot
- tabletit
04.0 KLIINISET TIEDOT
04.1 Käyttöaiheet
LUMINALE on tarkoitettu pääasiassa yleiseksi rauhoittavaksi lääkkeeksi, erityisesti epilepsiaan ja kaikkiin pitkäaikaista sedaatiota vaativiin tiloihin.
04.2 Annostus ja antotapa
Luminale -injektiopullot
Ellei lääkäri toisin määrää, 1 ampulli päivässä lihakseen aikuisille. Älä ylitä 400 mg 24 tunnissa.
Lapsilla 10 mg jokaista ikävuotta kohti ensimmäisestä vuodesta.
Luminale 100 mg tabletit
Rauhoittavana aineena 50-100 mg (1 / 2-1 tabletti) päivässä.
Kouristuksia ehkäisevänä aineena aikuisille 100-300 mg (1-3 tablettia) päivässä 2-3 kertaa. Lapsilla annoksia on pienennettävä (20 mg: sta 100 mg: aan) iän ja painon mukaan, ja Luminale 15 mg -tabletit on tarkoitettu.
Vaikeassa unettomuudessa 50-200 mg (1/2-2 tablettia) illalla tunti ennen nukkumaanmenoa. Tabletit voidaan liuottaa pieneen veteen tai mahdollisesti lisätä ruokaan. Iäkkäiden potilaiden hoidossa annoksen on oltava huolellisesti lääkäri, jonka on arvioitava edellä mainittujen annosten mahdollinen pienentäminen.
04.3 Vasta -aiheet
Yliherkkyys vaikuttavalle aineelle tai apuaineille.
Porfyria, munuaisten ja maksan vajaatoiminta, vaikea sydänsairaus, akuutti alkoholimyrkytys, kipulääkkeet, unilääkkeet.
04.4 Varoitukset ja käyttöön liittyvät varotoimet
Fenobarbitaali voi aiheuttaa riippuvuutta. Jatkuva hoito indusoi maksaentsyymien muodostumista, jotka nopeuttavat tiettyjen lääkkeiden, kuten antikoagulanttien, joidenkin antibioottien, lisämunuaisen steroidien, aineenvaihduntaa. Hypericum perforatum -valmisteita ei pidä käyttää samanaikaisesti fenobarbitaalia sisältävien lääkevalmisteiden kanssa, koska fenobarbitaalin plasman pitoisuuksien ja terapeuttisen tehon riski voi laskea (ks. Kohta Yhteisvaikutukset).
Alkoholin vaikutus tehostuu ja alkoholijuomien nauttimista tulee rajoittaa Yhdistelmä muiden psykotrooppisten lääkkeiden ja antihistamiinien kanssa vaatii erityistä varovaisuutta ja valppautta lääkäriltä välttääkseen vuorovaikutuksen odottamattomia haittavaikutuksia. Hoidon äkillinen lopettaminen epilepsiapotilailla voi aiheuttaa epileptisen tilan.
Itsemurha -ajatuksia ja -käyttäytymistä on raportoitu potilailla, jotka ovat saaneet epilepsialääkkeitä eri käyttöaiheissaan. Satunnaistettujen kliinisten tutkimusten meta-analyysi lumelääkettä vastaan korosti myös itsemurha-ajatusten ja -käyttäytymisen riskin vähäistä kasvua.
Tämän riskin mekanismia ei ole vahvistettu, eivätkä saatavilla olevat tiedot sulje pois mahdollisuutta lisätä riskiä Luminalen kanssa.
Siksi potilaita on seurattava itsetuhoajatuksen ja -käyttäytymisen merkkien varalta, ja asianmukaista hoitoa on harkittava, jos näin on. Potilaita (ja hoitajia) on neuvottava ilmoittamaan hoitavalle lääkärilleen, jos itsemurha -ajatuksia tai -käyttäytymistä ilmenee.
Seuraavia hengenvaarallisia ihoreaktioita on raportoitu Luminalen käytön yhteydessä: Stevens-Johnsonin oireyhtymä (SJS) ja toksinen epidermaalinen nekrolyysi (TEN).
Potilaille on ilmoitettava oireista ja heitä on seurattava tarkasti ihoreaktioiden varalta. Suurin riski SJS: n ja TEN: n kehittymiselle ilmenee ensimmäisten 8 hoitoviikon aikana.
Jos SJS: n tai TEN: n oireita tai merkkejä ilmenee (esim. Etenevä ihottuma, johon usein liittyy rakkuloita tai limakalvovaurioita), Luminale -hoito on lopetettava.
Parhaat tulokset SJS: n ja TEN: n hoidossa saadaan varhaisella diagnoosilla ja hoidon välittömällä lopettamisella minkä tahansa epäillyn lääkkeen kanssa.
Jos potilaalle on kehittynyt SJS tai TEN Luminalen käytön aikana, Luminale -valmistetta ei saa enää käyttää tällä potilaalla.
Ei lasten ulottuville eikä näkyville.
Katso myös kohdat 4.6 ja 4.7.
04.5 Yhteisvaikutukset muiden lääkevalmisteiden kanssa sekä muut yhteisvaikutukset
Fenobarbitaalin teho voi heikentyä, jos samanaikaisesti annetaan Hypericum perforatum -pohjaisia valmisteita.Tämä johtuu siitä, että Hypericum perforatum -pohjaiset valmisteet indusoivat lääkkeiden aineenvaihdunnasta vastaavia entsyymejä, joten niitä ei pidä antaa samanaikaisesti fenobarbitaalin kanssa. Induktiovaikutus voi jatkua vähintään 2 viikon ajan Hypericum perforatum -valmisteen käytön lopettamisen jälkeen. Jos potilas käyttää Hypericum perforatum -valmisteita samanaikaisesti, veren fenobarbitaalipitoisuuksia on seurattava ja hoito Hypericum perforatum -valmisteilla lopetettava. Veren fenobarbitaalipitoisuudet voivat nousta, kun Hypericum perforatum lopetetaan. Fenobarbitaalin annostusta on ehkä muutettava.
Katso kohta 4.4
04.6 Raskaus ja imetys
Potilaille, jotka voivat tulla raskaaksi tai ovat hedelmällisessä iässä, on annettava erikoisneuvontaa.
Epilepsialääkityksen tarve on arvioitava uudelleen, kun potilas suunnittelee raskautta.
Synnynnäisten vikojen riski kasvaa 2-3 kertaa epilepsialääkettä saaneiden äitien jälkeläisillä, joista yleisimmin raportoitu huulten halkeama, sydän- ja verisuonivirheet ja hermoputken viat.
Moniterapiaan epilepsialääkkeillä voi liittyä suurempi synnynnäisten epämuodostumien riski kuin monoterapiaan. Siksi on tärkeää, että monoterapiaa harjoitetaan aina kun mahdollista.
Epilepsialääkityksen äkillistä lopettamista ei pidä harjoittaa, koska kouristusten uusiutuminen voi aiheuttaa vakavia seurauksia sekä äidille että vauvalle.
04.7 Vaikutus ajokykyyn ja koneiden käyttökykyyn
Fenobarbitaalihoito vähentää huomiota ja pidentää refleksien kestoa: potilaita on varoitettava tästä, jotta he eivät välttämättä aja autoa tai suorita toimintoja, jotka vaativat valppautta koskemattomuutensa vuoksi.
04.8 Haittavaikutukset
Iho: harvinaisia allergisia iho -oireita. Harvinaisia multiformisen punoituksen, Stevens-Johnsonin oireyhtymän ja toksisen epidermaalisen nekrolyysin (Lyellin oireyhtymä) tapauksia on raportoitu.
Maksa ja sappi: harvinaisia toksisen hepatiitin tapauksia.
Hematologiset: harvinaiset leukopenia, agranulosytoosi, trombosytopenia ja purppura. Fenobarbitaalilla hoidettujen äitien vastasyntyneillä voi esiintyä K -vitamiinihoitoon vaikuttavaa hypotrombinemiaa.
Kroonisten hoitojen aikana voi esiintyä folaattiherkkää megaloblastista anemiaa ja osteomalasiaa, joka reagoi D-vitamiinihoitoon.
Keskushermosto: joillakin potilailla niitä voi esiintyä harvoin: jännitystä, levottomuutta ja deliriumia. Lapsipotilailla voi esiintyä hyperaktiivisuuden ilmenemismuotoja.
Sedaatio, ataksia, nystagmus ja henkinen sekavuus voivat ilmetä etenkin vanhuksilla suurien annosten jälkeen.
Luminalen käytön yhteydessä on raportoitu vakavia ihon haittavaikutuksia, kuten Steven-Johnosonin oireyhtymää (SJS) ja toksista epidermaalista nekrolyysiä (TEN).
Esiintymistiheys: hyvin harvinainen
Pitkäaikaista Luminale-hoitoa saavilla potilailla on raportoitu luun mineraalitiheyden vähenemisestä, osteopeniasta, osteoporoosista ja murtumista. Mekanismia, jolla Luminale vaikuttaa luun aineenvaihduntaan, ei ole tunnistettu.
Katso myös kohdat 4.4 - 4.6 ja 4.7
04.9 Yliannostus
Akuutin barbituraattimyrkytyksen hoito edellyttää välitöntä mahahuuhtelua, jos potilaan olosuhteet sen sallivat. Jo imeytynyt lääke voidaan poistaa pakotetulla diureesilla ja virtsan alkalisoinnilla. Vakavimmissa tapauksissa on hyödyllistä käyttää "hemodialyysiä ja voi olla tarpeen hallita hengitystä mekaanisesti. Antibioottien antaminen on välttämätöntä keuhkokomplikaatioiden alkamisen välttämiseksi.
05.0 FARMAKOLOGISET OMINAISUUDET
05.1 Farmakodynaamiset ominaisuudet
Fenobarbitaali on tehokas hypnoottinen-rauhoittava aine, joka vaikuttaa pääasiassa aivokuoreen, erityisesti moottorikeskuksiin, nostaa herkkyysrajaa ja myös aivorungon neurovegetatiivisia keskuksia. Sillä on myös spasmolyyttisiä ominaisuuksia, jotka mahdollistavat sen käytön yleensä spastisissa tiloissa.
05.2 Farmakokineettiset ominaisuudet
Fenobarbitaalin imeytyminen suun kautta on täydellinen, mutta hidas; huippupitoisuudet plasmassa määritetään useita tunteja kerta-annoksen jälkeen. Jakautumistilavuus on noin 0,9 1 / kg. Yli 25% fenobarbitaalia eliminoituu pH: sta riippuvaisella munuaisten kautta. Jäännösmäärä inaktivoidaan maksan mikrosomaalisilla entsyymeillä. Päämetaboliitti, parahydroksifenyylijohdannainen, on inaktiivinen ja erittyy virtsa osittain sulfaattikonjugaattina. Fenobarbitaalin puoliintumisaika plasmassa on noin 90 tuntia aikuisilla ja hieman lyhyempi lapsilla.
05.3 Prekliiniset tiedot turvallisuudesta
Rotan oraalinen LD50 on 660 mg / kg, mikä on yli 100 kertaa suositeltu terapeuttinen annos.
06.0 FARMASEUTTISET TIEDOT
06.1 Apuaineet
Luminale 200 mg injektioneste, liuos lihakseen
Apuaineet: propyleeniglykoli, etanoli, vesi pp.
Luminale -tabletit
Apuaineet: talkki, povidoni, steariinihappo, maissitärkkelys
06.2 Yhteensopimattomuus
Ei tiedossa.
06.3 Voimassaoloaika
Luminale 200 mg / ml injektioneste, liuos lihakseen:
Voimassaolo: 2 vuotta.
Luminale -tabletit
Voimassaolo: 5 vuotta.
06.4 Säilytys
Pidä poissa valolta.
Viimeinen käyttöpäivämäärä viittaa tuotteeseen ehjässä pakkauksessa, oikein varastoituna.
06.5 Välipakkauksen luonne ja pakkauksen sisältö
- 1 ml: n ampullit: tyypin I väritön lasi F.U. IX toim. 10 injektiopullon laatikko
Tabletit: läpipainopakkaus (PVC-alumiini kytketty) läpinäkymätön. 20 tabletin laatikko
06.6 Käyttö- ja käsittelyohjeet
Ei mitään raportoitavaa.
07.0 MYYNTILUVAN HALTIJA
BRACCO S.p.A. E.Follin kautta, 50 - Milano
08.0 MYYNTILUVAN NUMERO
Luminale 200 mg / ml injektioneste, liuos lihakseen - AIC 002860017
Luminale -tabletit - AIC 002860031
09.0 MYYNTILUVAN TAI UUDISTAMISPÄIVÄMÄÄRÄ
Luminale 200 mg / ml injektioneste, liuos lihakseen 12.07.1950 / 01.06.2005
Luminale -tabletit - 16.10.1967 / 01.06.2010
10.0 TEKSTIN MUUTTAMISPÄIVÄMÄÄRÄ
Kesäkuuta 2012