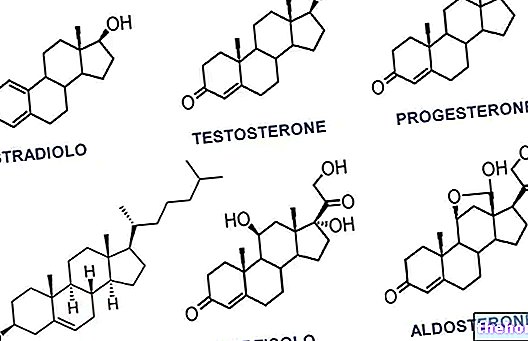
Proteiinien alkuaineanalyysi antaa seuraavat keskiarvot: 55% hiiltä, 7% vetyä ja 16% typpeä; on selvää, että proteiinit eroavat toisistaan, mutta niiden keskimääräinen alkuaineiden koostumus eroaa vähän yllä olevista arvoista .
Periaatteessa proteiinit ovat makromolekyylejä, jotka on muodostettu luonnollisista a-aminohapoista; aminohapot liittyvät amidisidoksen kautta, joka saadaan aikaan reaktiolla a-aminohapon aminoryhmän ja toisen a-aminohapon karboksyylin välillä.
Tätä sidosta (-CO-NH-) kutsutaan myös peptidisidokseksi, koska se sitoutuu peptideihin (aminohapot yhdessä):
yksi on dipeptidi, koska se koostuu kahdesta aminohaposta. Koska dipeptidi sisältää vapaan aminoryhmän toisessa päässä (NH2) ja karboksyylin toisessa päässä (COOH), se voi reagoida yhden tai useamman aminohapon kanssa ja pidentää ketjua sekä oikealta että vasemmalta samalla reaktiolla yllä nähty.
Reaktioiden sarja (jotka eivät muuten ole oikeastaan niin yksinkertaisia) voi jatkua loputtomiin: kunnes on olemassa ns. polypeptidi tai proteiinia. Ero peptidien ja proteiinien välillä liittyy molekyylipainoon: yleensä yli 10000 molekyylipainolla puhutaan proteiineista.
Aminohappojen sitominen yhteen jopa pienien proteiinien saamiseksi on vaikea tehtävä, vaikka viime aikoina on kehitetty automaattinen menetelmä proteiinien tuottamiseksi aminohapoista, mikä antaa erinomaisia tuloksia.
Yksinkertaisin proteiini koostuu siis kahdesta aminohaposta: kansainvälisen sopimuksen mukaan aminohappojen järjestetty numerointi proteiinirakenteessa alkaa aminohaposta, jossa on vapaa a-aminoryhmä.
koodaavat tätä proteiinia), jolla on merkityksettömiä kemiallisia vaikeuksia.
Oli mahdollista määrittää järjestetty aminohapposekvenssi Edman-hajoamisen kautta: proteiini reagoi fenyyli-isotiosyanaatin (FITC) kanssa; aluksi a-amino-typpidubletti hyökkää fenyyli-isotiosyanaattiin, joka muodostaa tiokarbamyylijohdannaisen; sen jälkeen saatu tuote syklisoituu, jolloin saadaan fenyylitiohydantoiinijohdannainen, joka on fluoresoiva.
Edman on kehittänyt sekvensseriksi kutsutun koneen, joka säätää automaattisesti parametrit (aika, reagenssit, pH jne.) Hajoamista varten ja tarjoaa proteiinien ensisijaisen rakenteen (tästä hän sai Nobelin palkinnon).
Ensisijainen rakenne ei riitä täysin tulkitsemaan proteiinimolekyylien ominaisuuksia; uskotaan, että nämä ominaisuudet riippuvat olennaisesti tilakokoonpanosta, jonka proteiinimolekyylit pyrkivät omaksumaan, taittuen eri tavoin: eli olettaen, mikä on määritelty proteiinien toissijaiseksi rakenteeksi.
Proteiinien toissijainen rakenne välkkyy, toisin sanoen sillä on taipumus hajota kuumennettaessa; sitten proteiinit denaturoivat itsensä menettäen monet ominaisominaisuuksistaan. Sen lisäksi, että lämmitys yli 70 ° C, denaturointi voi johtua myös säteilytyksestä tai reagenssien vaikutuksesta (esimerkiksi vahvoista hapoista).
Proteiinien denaturoituminen lämpövaikutuksen vuoksi havaitaan esimerkiksi kuumentamalla munanvalkuaista: sen nähdään menettävän hyytelömäisen ulkonäkönsä ja muuttuvan liukenemattomaksi valkoiseksi aineeksi. Proteiinien denaturointi johtaa kuitenkin niiden toissijaisen rakenteen tuhoutumiseen, mutta jättää niiden primaarisen rakenteen muuttamatta (eri aminohappojen ketjutus).
Proteiinit ottavat tertiäärisen rakenteen, kun niiden ketju, vaikka se on edelleen joustava toissijaisen rakenteen taivutuksesta huolimatta, taittuu siten, että muodostuu vääntynyt kolmiulotteinen järjestely kiinteän kappaleen muotoon. Tertiaarisesta rakenteesta ovat vastuussa ennen kaikkea disulfidisidokset, jotka voidaan muodostaa molekyyliä pitkin hajallaan olevan kysteiini-SH: n väliin.
Kvaternaarinen rakenne sen sijaan kuuluu vain kahden tai useamman alayksikön muodostamiin proteiineihin. Esimerkiksi hemoglobiini koostuu kahdesta parista proteiineja (eli kaikissa neljässä proteiiniketjussa), jotka sijaitsevat tetraedrin kärjissä siten, että muodostuu pallomainen rakenne; neljä proteiiniketjua pidetään yhdessä ionisten ja ei-kovalenttiset sidokset.
Toinen esimerkki kvaternaarisesta rakenteesta on insuliini, joka näyttää koostuvan jopa kuudesta proteiinin alayksiköstä, jotka on järjestetty pareittain kolmion kärkiin, joiden keskellä on kaksi sinkkiatomia.
Kuituiset proteiinit
Ne ovat proteiineja, joilla on tietty jäykkyys ja joilla on paljon pidempi akseli kuin toisella; kuituproteiini, jota on enemmän luonnossa, on kollageeni (tai kollageeni).
Kuituproteiini voi olettaa erilaisia sekundaarisia rakenteita: a-heliksi, β-arkki ja kollageenin tapauksessa kolmoiskierre; α-helix on vakain rakenne, jota seuraa β-arkki, kun taas vähiten vakaa kolmesta on kolmoiskierre.
oikein jos päärungon jälkeen (suunnattu alhaalta ylöspäin) suoritetaan oikeanpuoleisen ruuvin ruuvaamisen kaltainen liike; kun kierre on vasen käsi jos liike on analoginen vasemmanpuoleisen ruuvin ruuvaamisen kanssa. käsi a -helikes -R -substituentit ovat sisäänpäin. Oikeakätiset a-kierukat ovat vakaampia kuin vasenkätiset, koska vati -R c ": n välillä on vähemmän vuorovaikutusta ja vähemmän steerisiä esteitä.
Α-heliksin rakenne stabiloidaan vetysidoksilla (vetysillat), jotka muodostuvat kunkin aminohapon karboksyyliryhmän (-C = O) ja neljän ryhmän jälkeen löydetyn aminoryhmän (-NH) väliin lineaarinen sekvenssi.
Esimerkki proteiinista, jolla on a-helix-rakenne, on hiusten keratiini.
Pidentämällä a-helix-rakennetta siirrytään a-helixistä β-arkkiin; myös lämpö tai mekaaninen rasitus sallivat kulkea a-kierukasta β-levyrakenteeseen.
Yleensä proteiinissa β-arkkirakenteet ovat lähellä toisiaan, koska ketjun väliset vetysidokset voidaan muodostaa itse proteiinin osien väliin.
Kuituproteiineissa suurin osa proteiinirakenteesta on järjestetty a-heliksi- tai β-arkkiin.
Globulaariset proteiinit
Niillä on lähes pallomainen tilarakenne (johtuen polypeptidiketjun lukuisista suunnanmuutoksista); jotkut olemisen osat voidaan jäljittää α-helix- tai β-arkkirakenteeseen, ja muut osat eivät sen sijaan johdu näistä muodoista: järjestely ei ole satunnainen, vaan järjestetty ja toistuva.
Tähän mennessä mainitut proteiinit ovat aineita, joilla on täysin homogeeninen rakenne: toisin sanoen yhdistettyjen aminohappojen puhtaat sekvenssit; sellaisia proteiineja sanotaan yksinkertainen; on proteiineja, jotka koostuvat proteiiniosasta ja ei-proteiiniosasta (eturauhasryhmä), joita kutsutaan proteiineiksi konjugaatti.
, kynsissä, sarveiskalvossa ja silmän linssissä, joidenkin elinten (esim. maksan) välitilojen välissä ja niin edelleen.
Sen rakenne antaa sille erityisiä mekaanisia ominaisuuksia; sillä on suuri mekaaninen lujuus, joka liittyy korkeaan joustavuuteen (esim. jänteissä) tai korkeaan jäykkyyteen (esim. luissa) sen tehtävän mukaan.
Yksi kollageenin mielenkiintoisimmista ominaisuuksista on sen yksinkertainen yksinkertaisuus: se koostuu noin 30% proliinista ja noin 30% glysiinistä; muiden 18 aminohapon on vain jaettava loput 40% proteiinirakenteesta. Kollageenin aminohapposekvenssi on huomattavan säännöllinen: jokaista kolmea tähdettä kohden kolmas on glysiini.
Proliini on syklinen aminohappo, jossa R-ryhmä sitoutuu a-amino-typpiin ja antaa sille tietyn jäykkyyden.
Lopullinen rakenne on toistuva ketju, jonka muoto on "kierre"; kollageeniketjun sisällä ei ole vetysidoksia. Kollageeni on "vasemman käden kierre, jonka nousu (pituus vastaa kierukan yhtä kierrosta)" a-kierukkaa suurempi; kollageenikierukka on niin löysä, että kolme proteiiniketjua kykenee kietoutumaan toistensa ympärille muodostaen " yksi köysi: kolminkertainen kierrerakenne.
Kolmogeenin kolminkertainen kierre on kuitenkin vähemmän vakaa kuin sekä a-heliksi että β-arkkirakenne.
Katsotaanpa nyt mekanismi, jolla kollageenia tuotetaan; Ajattele esimerkiksi verisuonen repeämistä: tähän repeämään liittyy lukemattomia signaaleja, joiden tarkoituksena on sulkea verisuoni ja muodostaa siten hyytymä.
Koagulaatio vaatii vähintään kolmekymmentä erikoistunutta entsyymiä. Hyytymän jälkeen on tarpeen jatkaa kudoksen korjaamista; haavan lähellä olevat solut tuottavat myös kollageenia. Tätä varten indusoidaan ensin geenin ilmentyminen, eli eliöt, jotka geenin tiedoista alkaen kykenevät tuottamaan proteiinia (geneettinen tieto transkriboidaan mRNA: han, joka lähtee ytimestä ja saavuttaa ribosomit sytoplasmassa, jossa geneettinen informaatio muunnetaan proteiiniksi.) Sitten kollageeni syntetisoidaan ribosomeissa (se näyttää vasemman käden kierukalta, joka koostuu noin 1200 aminohaposta ja jonka molekyylipaino on noin 150 000 d) ja sitten kerääntyy luumeniin siitä tulee substraatti entsyymeille, jotka kykenevät suorittamaan translaation jälkeisiä muutoksia ("mRNA: n kääntämän kielen muutokset"); kollageenissa nämä muutokset koostuvat joidenkin sivuketjujen, erityisesti proliinin ja lysiinin, hydroksylaatiosta.
Näihin muutoksiin johtavien entsyymien toimintahäiriöt aiheuttavat keripukkia: se on sairaus, joka aiheuttaa aluksi verisuonten rikkoutumisen, hampaiden rikkoutumisen, jota voivat seurata suoliston väliset verenvuodot ja kuolema; se voi johtua pitkäikäisen ruoan jatkuvasta käytöstä.
Myöhemmin muiden entsyymien vaikutuksesta tapahtuu muita muutoksia, jotka koostuvat proliinin ja lysiinin hydroksyyliryhmien glykosidaatiosta (sokeri sitoutuu OH: n happeen); Näitä entsyymejä esiintyy muilla alueilla kuin ontelossa, joten proteiini kulkee muutosten aikana endoplasmisen verkkokalvon sisään päätyäkseen pusseihin (rakkuloihin), jotka sulkeutuvat ja irrottavat verkkokalvon: niiden sisällä on glykosidoitu pro -kollageenimonomeeri; jälkimmäinen saavuttaa Golgi-laitteen, jossa tietyt entsyymit tunnistavat kysteiinin, joka on läsnä glykosidoidun pro-kollageenin karboksipääteosassa, ja saavat eri ketjut lähestymään toisiaan ja muodostamaan disulfidisiltoja: tällä tavalla kolme ketjua glykosidoitu pro-kollageeni saadaan yhteen kytkettynä, ja tästä lähtökohdasta kolme ketjua, jotka tunkeutuvat toisiinsa, synnyttävät sitten spontaanisti kolminkertaisen kierukan. tukehtuen itseensä, irrottautuu Golgi -laitteesta ja kuljettaa kolme ketjua kohti solun reunaa, jossa sulakkeen kautta ionin kanssa plasmamembraanissa, trimetri poistetaan solusta.
Solun ylimääräisessä tilassa on erityisiä entsyymejä, pro-kollageenipeptidaaseja, jotka poistavat solusta karkotetuista lajeista, kolme fragmenttia (yksi kutakin heliksiä kohden), 300 aminohappoa l "yksi, terminaalisesta karboksiosasta ja kolme fragmentit (yksi kutakin kierretä kohden), joissa kussakin on noin 100 aminohappoa, aminoterminaalisesta osasta: jäljellä on kolmoiskierre, joka koostuu noin 800 aminohaposta per kierre, joka tunnetaan nimellä tropokollageeni.
Tropokollageenilla on melko jäykkä sauva; erilaiset trimmerit yhdistyvät kovalenttisiin sidoksiin, jolloin saadaan suurempia rakenteita: mikrokuituja. Mikrokuiduissa eri trimmerit on järjestetty porrastetusti; monet mikrokuidut muodostavat tropokollageeninippuja.
Luissa, kollageenikuitujen välissä, on välitiloja, joihin kalsiumin ja magnesiumin sulfaatit ja fosfaatit kerääntyvät: nämä suolat peittävät myös kaikki kuidut; tämä tekee luista jäykkiä.
Jänteissä välivälit ovat vähemmän kiteitä kuin luut, kun taas pienempiä proteiineja on läsnä kuin tropokollageenissa: tämä antaa jänteille joustavuutta.
Osteoporoosi on sairaus, joka johtuu kalsiumin ja magnesiumin puutteesta, mikä tekee mahdottomaksi kiinnittää suoloja tropokollageenikuitujen välisiin alueisiin.