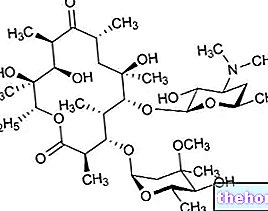
Vaikuttavat aineet: Retinoli (retinoliasetaatti)
VIT A N "25.000UI / 100 g oftalmologinen voide" 5 g: n putki
Käyttöaiheet Miksi Vit A N: ää käytetään? Mitä varten se on?
Farmakoterapeuttinen ryhmä: Epiteeli eutrofinen. Antixerophthalmic.
Käyttöaiheet
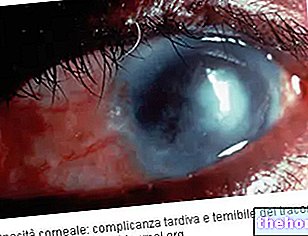
Blefariitti, imukudoksen keratokonjunktiviitti, kseroftalmia, keratiitti, sarveiskalvon haavaumat.
Vasta -aiheet, kun Vit A N: ää ei tule käyttää
Yliherkkyys mille tahansa valmisteen aineosalle.
Käytön varotoimet Mitä sinun on tiedettävä, ennen kuin otat Vit A N
Ei mitään
Yhteisvaikutukset Mitkä lääkkeet tai elintarvikkeet voivat muuttaa Vit A N: n vaikutusta
Ei mitään
Varoitukset On tärkeää tietää, että:
Pidä tämä lääke poissa lasten ulottuvilta
Annos, antotapa ja antamisaika Vit A N: n käyttö: Annostus
2-3 käyttökertaa päivässä sidekalvopussiin, ellei toisin määrätä.
Sivuvaikutukset Mitkä ovat Vit A N: n sivuvaikutukset
Joissakin tapauksissa voi tuntua lievä ja ohimenevä silmän polttamisen tunne.
Vanhentuminen ja säilyttäminen
Varoitus: älä käytä lääkettä pakkauksessa mainitun viimeisen käyttöpäivämäärän jälkeen.
Potilasta kehotetaan ilmoittamaan lääkärille tai apteekkihenkilökunnalle kaikista haittavaikutuksista, joita ei ole kuvattu tässä pakkausselosteessa.
Pakkaus: 5 g putki.
Sävellys
100 g sisältää: Retinolia (asetaattina) 25000 IU
Apuaineet: p. Metyylihydroksibentsoaatti; s. Propyylihydroksibentsoaatti; Nestemäinen parafiini; Valkoinen vaseliini
Alkuperäinen pakkausseloste: AIFA (Italian lääkevirasto). Sisältö julkaistu tammikuussa 2016. Esitetyt tiedot eivät välttämättä ole ajan tasalla.
Jotta saat käyttöösi uusimman version, on suositeltavaa käyttää AIFA: n (Italian Medicines Agency) verkkosivustoa. Vastuuvapauslauseke ja hyödyllistä tietoa.
01.0 LÄÄKEVALMISTEEN NIMI
VITAN
02.0 LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS
100 g sisältää: Retinolia (asetaattina) 25000 IU
03.0 LÄÄKEMUOTO
"25.000UI / 100 g oftalmologinen voide" 5 g: n putki
04.0 KLIINISET TIEDOT
04.1 Käyttöaiheet
Blefariitti. Lymfaattinen keratokonjunktiviitti. Kseroftalmia. Keratiitti. Sarveiskalvon haavaumat.
04.2 Annostus ja antotapa
2-3 käyttökertaa päivässä sidekalvopussiin, ellei toisin määrätä.
04.3 Vasta -aiheet
Tunnettu yksilöllinen yliherkkyys mille tahansa tuotteen osalle.
04.4 Varoitukset ja käyttöön liittyvät varotoimet
Ei mitään.
Pidä tämä lääke poissa lasten ulottuvilta.
04.5 Yhteisvaikutukset muiden lääkevalmisteiden kanssa sekä muut yhteisvaikutukset
Ei mitään.
04.6 Raskaus ja imetys
Vasta -aiheita ei tunneta.
04.7 Vaikutus ajokykyyn ja koneiden käyttökykyyn
Vaikutuksia ei ole kuvattu.
04.8 Haittavaikutukset
Joissakin tapauksissa voi tuntua lievä ja ohimenevä silmän polttamisen tunne.
04.9 Yliannostus
Yliannostusreaktioita ei ole koskaan raportoitu.
05.0 FARMAKOLOGISET OMINAISUUDET
05.1 Farmakodynaamiset ominaisuudet
A -vitamiini on välttämätön epiteelisolujen kasvulle ja normaalille erilaistumiselle. Sen puute johtaa solujen lukumäärän vähenemiseen ja keratinisoitumiseen kaikissa epiteelissä, mukaan lukien sarveiskalvo. Erityisesti tällä viimeisellä alueella tyypillisen kuivan silmän (kseroftalmian) rinnalla A -vitamiinin puute voi aiheuttaa vakavia muutoksia sarveiskalvon parenkyymissä, kuten keratomalasiaa ja sarveiskalvon haavaumia.
05,2 "Farmakokineettiset ominaisuudet
Paikallisesti kanin silmään annettu retinoli metaboloituu retinoiinihapoksi, joka on aktiivinen osa A -vitamiinimolekyyliä.
05.3 Prekliiniset tiedot turvallisuudesta
A -vitamiinin myrkyllisyys on hyvin alhainen tai käytännössä ei lainkaan. Ihmisellä havaitaan ensimmäiset toksisuuden merkit akuutin oraalisen tai parenteraalisen annon jälkeen, kun annokset ovat 10 000 kertaa suurempia (15 g) kuin normaalin päivittäisen tarpeen (5000 IU) annokset. ) kuin tarvitaan päivittäin fysiologisissa olosuhteissa.
06.0 FARMASEUTTISET TIEDOT
06.1 Apuaineet
p. metyylihydroksibentsoaatti; s. Propyylihydroksibentsoaatti; Nestemäinen parafiini; Valkoinen vaseliini
06.2 Yhteensopimattomuus
Yhteensopimattomuuksia muiden lääkkeiden kanssa ei tunneta.
06.3 Voimassaoloaika
3 vuotta ehjässä pakkauksessa.
06.4 Säilytys
Ei mitään.
06.5 Välipakkauksen luonne ja pakkauksen sisältö
5 g maalattua alumiiniputkea.
06.6 Käyttö- ja käsittelyohjeet
Ei mitään.
07.0 MYYNTILUVAN HALTIJA
FARMIGEA ITALIA S.r.l., Centro Direzionale Milano Fiori Strada 4 SNC - 20090 Assago (MI)
08.0 MYYNTILUVAN NUMERO
A.I.C. n. 009896010
09.0 MYYNTILUVAN TAI UUDISTAMISPÄIVÄMÄÄRÄ
08.04.1955 /01.06.10
10.0 TEKSTIN MUUTTAMISPÄIVÄMÄÄRÄ
AIFA -määritys 9. huhtikuuta 2014