Vaikuttavat aineet: Cetrorelix (Cetrorelix -asetaatti)
Cetrotide 0,25 mg injektiokuiva -aine ja liuotin, liuosta varten
Käyttöaiheet Miksi Cetrotidea käytetään? Mitä varten se on?
Mikä on Cetrotide
Cetrotide sisältää vaikuttavaa ainetta, nimeltään "cetroreliksiasetaatti". Tämä lääke estää munasolun vapautumisen munasarjasta (ovulaation) kuukautiskierron aikana.
Mihin Cetrotidea käytetään
Cetrotide on yksi lääkkeistä, joita käytetään "avustettujen lisääntymismenetelmien" aikana raskauden edistämiseksi. Se estää munasolujen välittömän vapautumisen, koska jos munasolut vapautuvat liian aikaisin (ennenaikainen ovulaatio), lääkäri ei voi ottaa niitä.
Miten Cetrotide toimii
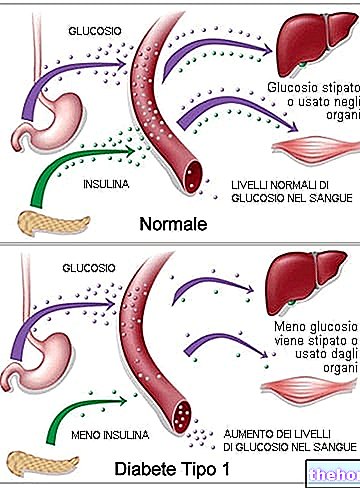
Cetrotide estää elimistössä olevan luonnollisen hormonin LHRH (luteinisoivaa hormonia vapauttava hormoni).
- LHRH kontrolloi toista hormonia, nimeltään LH ("luteinisoiva hormoni").
- LH stimuloi ovulaatiota kuukautiskierron aikana.
Tämä tarkoittaa sitä, että Cetrotide estää tapahtumaketjun, joka johtaa munasolun vapautumiseen munasarjassa. Kun munasolut ovat valmiita kerättäväksi, sinulle annetaan toinen lääke, joka indusoi munasolujen vapautumisen (ovulaation induktio).
Vasta -aiheet Kun Cetrotidea ei tule käyttää
Älä käytä Cetrotidea
- jos olet allerginen setroreliksiasetaatille tai tämän lääkkeen jollekin muulle aineelle (lueteltu kohdassa 6)
- jos olet allerginen Cetrotiden kaltaisille lääkkeille (muille peptidihormoneille)
- jos olet raskaana tai imetät
- jos olet jo vaihdevuodet
- jos sinulla on kohtalainen tai vaikea munuais- tai maksasairaus.
Älä käytä Cetrotidea, jos jokin yllä olevista koskee sinua. Jos olet epävarma, ota yhteys lääkäriisi ennen tämän lääkkeen käyttöä.
Käyttöön liittyvät varotoimet Mitä sinun on tiedettävä, ennen kuin otat Cetrotidea
Allergiat
Jos sinulla on aktiivinen allergia tai sinulla on ollut allergioita aiemmin, kerro siitä lääkärillesi ennen Cetrotide -valmisteen ottamista.
Munasarjojen hyperstimulaatio-oireyhtymä (OHSS)
Cetrotidea käytetään yhdessä muiden lääkkeiden kanssa, jotka stimuloivat munasarjoja tuottamaan enemmän vapautuvia munia. Munasarjojen hyperstimulaatio -oireyhtymää (OHSS) voi ilmetä näiden lääkkeiden käytön aikana tai sen jälkeen. Tämä tapahtuu, kun munarakkulat kasvavat ja muuttuvat suuriksi kystiksi. Mahdolliset vaikutukset, joita on tarkkailtava ja mitä tehdä, jos sinulle kehittyy, katso kohta 4 "Mahdolliset haittavaikutukset" .
Yhteisvaikutukset Mitkä lääkkeet tai elintarvikkeet voivat muuttaa Cetrotiden vaikutusta
Kerro lääkärille, jos parhaillaan käytät, olet äskettäin käyttänyt tai saatat käyttää muita lääkkeitä.
Varoitukset On tärkeää tietää, että:
Cetrotiden käyttö useamman kuin yhden syklin ajan
Kokemus Cetrotiden käytöstä useamman kuin yhden syklin aikana on rajallinen. Jos sinun on otettava Cetrotideä useamman kuin yhden syklin ajan, lääkäri arvioi huolellisesti hyödyt ja riskit.
Lapset ja nuoret
Cetrotiden käyttöä ei ole tarkoitettu lapsille ja nuorille.
Raskaus ja imetys
Älä käytä Cetrotidea, jos olet jo raskaana tai epäilet olevasi raskaana tai jos imetät. Kysy lääkäriltä tai apteekista neuvoa ennen minkään lääkkeen käyttöä.
Ajaminen ja koneiden käyttö
Cetrotiden käytön ei odoteta vaikuttavan ajokykyyn tai koneiden käyttökykyyn.
Annos, menetelmä ja antotapa Cetrotiden käyttö: Annostus
Käytä tätä lääkettä juuri sen verran kuin lääkäri on määrännyt. Jos olet epävarma, ota yhteys lääkäriisi.
Tämän lääkkeen käyttö
Tämä lääke on tarkoitettu vain vatsan injektioon juuri ihon pinnan alapuolelle (ihon alle). Ihon ärsytyksen välttämiseksi valitse eri vatsa -alue joka päivä.
- Ensimmäinen annos tulee antaa lääkärisi valvonnassa. Lääkäri tai sairaanhoitaja näyttää sinulle, miten lääke valmistetaan ja pistetään.
- Voit suorittaa seuraavat annokset sen jälkeen, kun lääkäri on ilmoittanut sinulle oireista, jotka voivat viitata allergioihin, sekä mahdollisista vakavista tai hengenvaarallisista seurauksista, jotka tarvitsevat välitöntä hoitoa (ks. Kohta 4 "Mahdolliset haittavaikutukset").
- Lue huolellisesti ja noudata ohjeita, jotka on kuvattu tämän pakkausselosteen lopussa olevassa kohdassa "Cetrotiden sekoittaminen ja pistäminen".
- Hoidon ensimmäinen päivä alkaa käyttää toista lääkettä. Aloitat Cetrotiden käytön muutamaa päivää myöhemmin. (Katso kohta "Kuinka paljon lääkettä käytetään".)
Kuinka paljon lääkettä käytetään
Pistä yhden injektiopullon (0,25 mg Cetrotide) sisältö kerran päivässä. On suositeltavaa käyttää lääkettä samaan aikaan joka päivä 24 tunnin välein yhden annoksen ja seuraavan välillä.
Voit valita pistoksen joka aamu tai ilta.
- Jos valitset aamuannoksen, aloita injektiot hoitojakson päivänä 5 tai 6. Lääkärisi kertoo sinulle tarkan päivämäärän ja kellonajan.Jatkat tämän lääkkeen käyttöä munien noutopäivään asti (ovulaation induktio).
TAI
- Jos olet valinnut iltaisin annostelun: aloita injektiot hoitojakson päivänä 5. Lääkärisi kertoo sinulle tarkan päivämäärän ja kellonajan.Jatkat tämän lääkkeen käyttöä iltaan ennen munasolun ottamista (ovulaation induktio).
Jos unohdat käyttää Cetrotidea
- Jos unohdat annoksen, pistä se heti kun huomaat sen ja kerro siitä lääkärillesi.
- Älä pistä kaksinkertaista annosta korvataksesi unohtamasi annoksen.
Jos sinulla on kysymyksiä tämän lääkkeen käytöstä, käänny lääkärin tai apteekkihenkilökunnan puoleen.
Yliannostus Mitä tehdä, jos olet ottanut yliannoksen Cetrotidea
Vakavia vaikutuksia ei odoteta, jos pistät vahingossa enemmän tätä lääkettä kuin odotettiin. Lääkkeen vaikutus kestää kauemmin, joten erityistoimenpiteitä ei yleensä tarvita.
Sivuvaikutukset Mitkä ovat Cetrotiden sivuvaikutukset?
Kuten kaikki lääkkeet, tämäkin lääke voi aiheuttaa haittavaikutuksia. Kaikki eivät kuitenkaan niitä saa.
Allergiset reaktiot
- Lämpö, ihon punoitus, kutina (usein nivusissa tai kainaloissa), punainen, kutiava, kohonnut alue (nokkosihottuma), vuotava nenä, nopea tai epäsäännöllinen sykkiminen, kielen ja kurkun turpoaminen, aivastelu, hengityksen vinkuminen tai vaikea hengitysvaikeus tai huimaus Saatat kokea vakavan tai hengenvaarallisen allergisen reaktion lääkkeelle Tämä reaktio on melko harvinainen (esiintyy alle 1%: lla naisista).
Jos huomaat jonkin näistä haittavaikutuksista, lopeta Cetrotide -valmisteen käyttö ja kerro siitä heti lääkärille Munasarjojen hyperstimulaatio -oireyhtymä (OHSS) Tämä voi johtua muista munasarjojen stimulointiin käytetyistä lääkkeistä.
- Munasarjojen hyperstimulaatio -oireyhtymän (OHSS) oireita voivat olla alavatsan kipu, johon liittyy pahoinvointi (pahoinvointi) tai todellinen epämukavuus (oksentelu) .Tämä voi tarkoittaa sitä, että munasarjat ovat reagoineet liikaa hoitoon ja että niille on kehittynyt suuria munasarjakystoja Tämä tapahtuma on yleinen ( voi esiintyä enintään 1 naisella 10: stä).
- OHSS voi muuttua vakavaksi merkittävästi suurentuneiden munasarjojen, vähentyneen virtsanerityksen, painonnousun, hengitysvaikeuksien tai nesteen vuoksi vatsassa tai rinnassa. Tämä tapahtuma on melko harvinainen (voi esiintyä enintään 1 naisella 100: sta).
Jos huomaat jonkin näistä haittavaikutuksista, kerro siitä heti lääkärillesi.
Muut haittavaikutukset
Yleiset (voi esiintyä enintään 1 naisella 10: stä):
- Pistoskohdassa voi esiintyä lievää ja lyhytaikaista ihoärsytystä, kuten punoitusta, kutinaa tai turvotusta.
Melko harvinaiset (voi esiintyä enintään 1 naisella 100: sta):
- Pahoinvointi
- Päänsärky.
Sivuvaikutusten ilmoittaminen
Jos havaitset haittavaikutuksia, käänny lääkärin tai apteekkihenkilökunnan puoleen, mukaan lukien mahdolliset haittavaikutukset, joita ei ole mainittu tässä pakkausselosteessa. Voit ilmoittaa haittavaikutuksista myös suoraan liitteessä V luetellun kansallisen ilmoitusjärjestelmän kautta. Ilmoittamalla haittavaikutuksista voit auttaa saamaan enemmän tietoa tämän lääkkeen turvallisuudesta.
Vanhentuminen ja säilyttäminen
Ei lasten ulottuville eikä näkyville.
Älä käytä tätä lääkettä injektiopullossa mainitun viimeisen käyttöpäivämäärän (EXP) jälkeen. Viimeinen käyttöpäivämäärä tarkoittaa kuukauden viimeistä päivää.
Injektiopullossa olevan Cetrotide-jauheen ja esitäytetyn ruiskun steriilin veden (liuotin) viimeinen käyttöpäivämäärä on sama.Tämä on ilmoitettu tarroissa ja pakkauksessa.
Säilytä alle 25 ° C.
Pidä injektiopullo ulkopakkauksessa suojataksesi lääkettä valolta.
Liuos on käytettävä heti valmistuksen jälkeen.
Älä käytä tätä lääkettä, jos huomaat, että injektiopullon valkoinen rae on muuttunut ulkonäöltään. Älä käytä sitä, jos injektiopullossa valmistettu liuos ei ole kirkas ja väritön tai sisältää hiukkasia.
Älä heitä lääkkeitä viemäriin tai talousjätteisiin. Kysy apteekista, kuinka heittää pois lääkkeet, joita et enää käytä. Tämä auttaa suojelemaan ympäristöä.
Jos sinulla on kysyttävää, käänny lääkärin tai apteekkihenkilökunnan puoleen.
Määräaika "> Muut tiedot
Mitä Cetrotide sisältää
- Vaikuttava aine on setroreliksiasetaatti. Yksi injektiopullo sisältää 0,25 mg setroreliksiasetaattia.
- Toinen aine on mannitoli.
- Liuotin on steriili injektionesteisiin käytettävä vesi.
Lääkevalmisteen kuvaus ja pakkaus
Cetrotide on valkoinen injektiokuiva -aine, liuosta varten lasisessa injektiopullossa, jossa on kumitulppa. Sitä on saatavana yhden tai seitsemän injektiopullon pakkauksissa (kaikkia pakkauskokoja ei välttämättä ole myynnissä).
Lisäksi pakkaukset sisältävät jokaisen injektiopullon
- esitäytetty ruisku, jossa on steriiliä injektionesteisiin käytettävää vettä (liuotin). Tätä vettä käytetään jauheen sekoittamiseen injektiopullossa
- keltaisella merkitty injektioneula steriilin veden ruiskuttamiseen injektiopulloon ja valmistetun lääkkeen ottamiseksi injektiopullosta
- harmaalla merkitty injektioneula lääkkeen pistämiseksi vatsaan
- kaksi alkoholipyyhettä desinfiointia varten.
CETROTIDEN SEKOITTAMINEN JA PISTÄMINEN
- Tässä osassa kuvataan, miten jauhe sekoitetaan steriiliin veteen (liuotin) ja pistetään lääke.
- Ennen kuin aloitat tämän lääkkeen käytön, lue nämä ohjeet kokonaan ja huolellisesti.
- Tämä lääke on tarkoitettu vain sinulle, kukaan muu ei saa käyttää sitä.
- Neula, injektiopullo ja ruisku ovat kertakäyttöisiä.
Ennen aloittamista
- Käsien pesuun
- On tärkeää, että kätesi ja kaikki käytetyt esineet ovat mahdollisimman puhtaita.
- Aseta kaikki tarvittava puhtaalle pinnalle:
- injektiopullo jauhetta
- esitäytetty ruisku steriilillä vedellä (liuotin)
- neula, jossa on keltainen merkki, steriilin veden ruiskuttamiseksi injektiopulloon ja valmistetun lääkkeen ottaminen pois
- neula harmaalla merkillä lääkkeen pistämiseksi vatsaan
- kaksi alkoholipyyhettä.
Jauheen sekoittaminen steriiliin veteen lääkkeen valmistamiseksi
- Poista muovikorkki injektiopullosta
- Alla on kumitulppa, pidä se injektiopullossa.
- Puhdista kumitulppa ja metallirengas ensimmäisellä alkoholipyyhkeellä.
- Veden lisääminen esitäytetystä ruiskusta injektiopullossa olevaan jauheeseen
- Ota keltainen merkki sisältävä neula pakkauksesta.
- Irrota esitäytetyn ruiskun korkki ja ruuvaa keltainen neula siihen ja poista neulan suojus.
- Työnnä keltainen neula injektiopullon kumitulpan keskikohdan läpi.
- Ruiskuta vesi injektiopulloon painamalla hitaasti ruiskun mäntää. Älä käytä muuta vettä.
- Jätä ruisku kumitulppaan.
- Jauhe sekoitetaan injektiopullon veteen
- Pidä ruiskusta ja injektiopullosta varovasti kiinni ja pyöritä niitä varovasti, jotta jauhe sekoittuu veteen.
- Älä ravista, jotta lääkkeessä ei ole rakkuloita.
- Täytä ruisku uudelleen lääkepullosta
- Käännä injektiopullo ylösalaisin.
- Vedä mäntä ulos vetääksesi lääke injektiopullosta ruiskuun.
- Jos osa lääkkeestä jää injektiopullon sisään, vedä keltainen neula hitaasti sisään, kunnes sen pää on kumitulpan sisällä.Jos katsot sivuttain raon läpi, voit tarkistaa neulan ja liuoksen liikkeet.
- Varmista, että olet ottanut kaikki lääkkeet injektiopullosta.
- Laita korkki takaisin keltaiseen neulaan.Ruuvaa keltainen neula irti ruiskusta ja aseta ruisku pinnalle.
Pistoskohdan valmistelu ja lääkkeen pistäminen
- Ilmakuplien poisto
- Ota harmaa neula pakkauksesta, ruuvaa harmaa neula ruiskuun ja poista neulan suojus.
- Pidä ruiskua harmaa neula ylöspäin ja tarkista ilmakuplat.
- Poista kuplia napauttamalla ruiskua varovasti, kunnes kaikki ilmakuplat kerääntyvät yläosaan, ja paina sitten mäntää varovasti irrottaaksesi ne ruiskusta.
- Älä koske harmaaseen neulaan äläkä anna harmaan neulan joutua kosketuksiin minkään pinnan kanssa.
- Pistoskohdan puhdistaminen
- Valitse pistoskohta vatsaan, mieluiten napaan.
- Puhdista iho valitulla pistoskohdalla käyttämällä toista alkoholilla kostutettua kudosta pyöreiden liikkeiden jälkeen.
- Ihon puhkeaminen
- Pidä ruiskua toisessa kädessä, ikään kuin se olisi lyijykynä.
- Purista kevyesti toisella kädellä ihoa pistoskohdan ympäriltä ja pidä siitä lujasti kiinni.
- Työnnä harmaa neula hitaasti iholle 45-90 asteen kulmassa ja vapauta iho.
- Lääkkeen pistäminen
- Vedä ruiskun mäntä varovasti sisään. Jos verta tulee, jatka vaiheen 5 mukaisesti.
- Jos verta ei tule näkyviin, paina mäntää hitaasti pistääksesi lääkkeen.
- Kun ruisku on tyhjä, vedä harmaa neula hitaasti ulos samasta kulmasta.
- Kun olet lopettanut injektion, paina pistoskohtaa kevyesti toisella alkoholipyyhkeellä.
- Jos verta tulee:
- vedä harmaa neula hitaasti ulos samasta kulmasta
- paina pistoskohtaa kevyesti toisella alkoholipyyhkeellä
- tyhjennä lääke astiaan ja jatka kohdan 6 mukaisesti
- pese kätesi ja aloita alusta uudella injektiopullolla ja uudella esitäytetyllä ruiskulla.
- Hävittäminen
- Neula, injektiopullo ja ruisku ovat kertakäyttöisiä.
- Aseta neulansuojus takaisin neulojen päälle, jotta ne voidaan hävittää turvallisesti.
- Kysy apteekista, kuinka hävittää käytetyt neulat, injektiopullot ja ruiskut turvallisesti.
Alkuperäinen pakkausseloste: AIFA (Italian lääkevirasto). Sisältö julkaistu tammikuussa 2016. Esitetyt tiedot eivät välttämättä ole ajan tasalla.
Jotta saat käyttöösi uusimman version, on suositeltavaa käyttää AIFA: n (Italian Medicines Agency) verkkosivustoa. Vastuuvapauslauseke ja hyödyllistä tietoa.
01.0 LÄÄKEVALMISTEEN NIMI -
CETROTITE 0,25 MG Jauhe ja liuotin, liuosta varten
02.0 LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS -
Yksi injektiopullo sisältää 0,25 mg setroreliksiä (asetaattina).
Käyttövalmiiksi saattamisen jälkeen mukana toimitettu liuotin, jokainen ml liuosta sisältää 0,25 mg setroreliksiä.
Täydellinen apuaineluettelo, katso kohta 6.1.
03.0 LÄÄKEMUOTO -
Injektiokuiva -aine ja liuotin, liuosta varten.
Jauheen ulkonäkö: valkoinen kylmäkuivattu
Liuottimen ulkonäkö: kirkas ja väritön liuos
Käyttövalmiiksi saatetun liuoksen pH on 4,0-6,0.
04.0 KLIINISET TIEDOT -
04.1 Käyttöaiheet -
Ennenaikaisen ovulaation ehkäisy potilailla, joille tehdään kontrolloitu munasarjojen stimulaatio, jota seuraa munasolujen haku ja avustavat lisääntymismenetelmät.
Cetrotidea on käytetty kliinisissä tutkimuksissa ihmisen vaihdevuodet ohittavan gonadotropiinin (HMG) kanssa, mutta rajallinen kokemus rekombinantista follikkelia stimuloivasta hormonista (FSH) on osoittanut samanlaisen tehon.
04.2 Annostus ja antotapa -
Cetrotiden saa määrätä vain alan asiantuntija.
Annostus
Ensimmäinen Cetrotide-hoito on annettava lääkärin valvonnassa ja olosuhteissa, jotka mahdollistavat allergisten / pseudoallergisten reaktioiden (mukaan lukien hengenvaaralliset anafylaktiset reaktiot) välittömän hoidon. sen jälkeen, kun hän on ilmoittanut hänelle oireista, jotka voivat viitata yliherkkyysreaktioihin, tällaisten reaktioiden seurauksista ja tarpeen välittömästä lääkärin toimenpiteestä, jos niitä ilmenee.
Yhden injektiopullon sisältö (0,25 mg setroreliksiä) tulee antaa kerran vuorokaudessa 24 tunnin välein joko aamulla tai illalla. Ensimmäisen annon jälkeen on suositeltavaa pitää potilas lääkärin seurannassa 30 minuutin ajan, jotta varmistetaan, ettei injektion jälkeen esiinny allergisia / pseudoallergisia reaktioita.
Iäkkäät väestöt
Ei ole viitteitä Cetrotiden erityisestä käytöstä iäkkäillä potilailla.
Pediatriset potilaat
Ei ole viitteitä Cetrotiden erityisestä käytöstä lapsipotilailla.
Antotapa
Cetrotide annetaan ihonalaisena injektiona vatsan alaosiin.
Pistoskohdan reaktioita voidaan vähentää vaihtamalla pistoskohtia vuorotellen, viivyttämällä injektioita samaan kohtaan ja pistämällä lääke hitaasti helpottamaan imeytymistä.
Aamuhallinto : Cetrotide -hoito tulee aloittaa 5. tai 6. päivänä munasarjojen stimulaatiolla virtsa- tai yhdistelmä -gonadotropiineilla (noin 96-120 tuntia munasarjojen stimulaation aloittamisesta) ja sitä on jatkettava koko gonadotropiinihoidon ajan, mukaan lukien "indusoidun ovulaation päivä".
Tarjoilu illalla : Cetrotide -hoito on aloitettava virtsa- tai yhdistelmä -gonadotropiineilla saadun munasarjojen stimulaation viidentenä päivänä (noin 96–108 tuntia munasarjojen stimulaation aloittamisen jälkeen), ja sitä on jatkettava koko hoitojakson ajan ennen indusoidun ovulaation päivää.
Ohjeet lääkkeen käyttövalmiiksi saattamisesta ennen antoa, ks. Kohta 6.6.
04.3 Vasta -aiheet -
Cetrorelixiä ei tule käyttää, jos jokin seuraavista tiloista on olemassa:
• Yliherkkyys vaikuttavalle aineelle tai gonadotropiinia vapauttavan hormonin (GnRH) rakenteellisille analogeille, ulkoisille peptidihormoneille tai kohdassa 6.1 mainituille apuaineille.
• Raskauden ja imetyksen aikana.
• Potilaat, joilla on vaikea munuaisten vajaatoiminta.
04.4 Varoitukset ja käyttöön liittyvät varotoimet -
Allergiset olosuhteet
Ensimmäisen annoksen yhteydessä on raportoitu allergisia / pseudoallergisia reaktioita, mukaan lukien hengenvaarallisia anafylaktisia reaktioita (ks. Kohta 4.8).
Erityistä huomiota on kiinnitettävä naisiin, joilla on allergisten tilojen merkkejä ja oireita tai joilla on tunnettu allergia -alttius. Cetrotide -hoitoa ei suositella naisille, joilla on vaikea allerginen sairaus.
Munasarjojen hyperstimulaatio -oireyhtymä (Munasarjojen hyperstimulaatio-oireyhtymä, OHSS)
Munasarjojen hyperstimulaatio -oireyhtymää voi esiintyä munasarjojen stimulaation aikana tai sen jälkeen. Tätä mahdollisuutta on pidettävä gonadotropiinin stimulaatiotekniikoiden sisäisenä riskinä.
Munasarjojen hyperstimulaatio -oireyhtymää tulee hoitaa oireenmukaisesti, ts. Levossa, elektrolyyttejä / kolloideja suonensisäisesti ja hepariinihoitoa.
Luteaalinen tukivaihe on suoritettava lisääntymisterveyskeskusten menettelyjen mukaisesti.
Toistuva munasarjojen stimulaatiomenettely
Tähän mennessä on vain vähän kokemusta setroreliksin antamisesta toistuvan munasarjojen stimulaatiotoimenpiteen aikana. Siksi setroreliksiä tulee käyttää vain toistuvina sykleinä huolellisen riskin / hyödyn arvioinnin jälkeen.
Synnynnäisiä poikkeavuuksia
Synnynnäisten poikkeavuuksien esiintyvyys avusteisen lisääntymismenetelmän käytön jälkeen (avustettu lisääntymistekniikka, ART) GnRH -antagonisteilla tai ilman niitä voi olla hieman korkeampi kuin spontaanin hedelmöityksen jälkeen havaittu, mutta ei tiedetä, johtuuko tämä parin hedelmättömyyteen tai ART -toimenpiteisiin liittyvistä tekijöistä. seuranta, 316 imeväisellä, jotka saivat hedelmättömyyden hoitoon setroreliksiä, viittaa siihen, että setroreliksi ei lisää synnynnäisten poikkeavuuksien riskiä jälkeläisissä.
Maksan vajaatoiminta
Cetroreliksiä ei ole tutkittu potilailla, joilla on maksan vajaatoiminta, joten varovaisuutta on noudatettava.
Munuaisten vajaatoiminta
Cetroreliksiä ei ole tutkittu munuaisten vajaatoimintaa sairastavilla potilailla, joten varovaisuutta on noudatettava.
Cetrorelix on vasta -aiheinen potilaille, joilla on vaikea munuaisten vajaatoiminta (ks. Kohta 4.3).
04.5 Yhteisvaikutukset muiden lääkevalmisteiden kanssa sekä muut yhteisvaikutukset -
Muodollisia yhteisvaikutustutkimuksia setroreliksin kanssa ei ole tehty in vitro ovat osoittaneet, että yhteisvaikutukset sellaisten lääkevalmisteiden kanssa, jotka metaboloituvat sytokromi P450: n tai glukuronidaattien avulla tai konjugoidaan jollakin muulla tavalla, ovat epätodennäköisiä. Yhteisvaikutusten mahdollisuutta gonadotropiinien tai lääkkeiden kanssa, jotka voivat aiheuttaa histamiinin vapautumista herkillä yksilöillä, ei kuitenkaan voida täysin sulkea pois.
04.6 Raskaus ja imetys -
Raskaus ja imetys
Cetrotidea ei tule käyttää raskauden ja imetyksen aikana (ks. Kohta 4.3).
Hedelmällisyys
Kokeelliset eläinkokeet osoittavat, että setroreliksillä on annoksesta riippuvainen vaikutus hedelmällisyyteen, lisääntymistoimintaan ja raskauteen. Kun lääkettä annettiin herkällä raskausjaksolla, teratogeenisiä vaikutuksia ei havaittu.
04.7 Vaikutus ajokykyyn ja koneiden käyttökykyyn -
Cetrotide -valmisteella ei ole haitallista vaikutusta ajokykyyn ja koneiden käyttökykyyn.
04.8 Haittavaikutukset -
Yhteenveto turvallisuusprofiilista
Yleisimmin havaitut haittavaikutukset ovat paikalliset pistoskohdan reaktiot, kuten punoitus, turvotus ja kutina, jotka ovat yleensä ohimeneviä ja lieviä. Kliinisissä tutkimuksissa näitä vaikutuksia havaittiin 9,4%: n taajuudella Cetrotide 0,25 mg: n useiden injektioiden jälkeen.
Lievää tai kohtalaista munasarjojen hyperstimulaatio -oireyhtymää (OHSS) (WHO: n luokka I tai II) on havaittu yleisesti, ja sitä on pidettävä tahdistusmenettelyn luontaisena riskinä. Sitä vastoin vaikea OHSS on edelleen harvinainen tapahtuma.
Melko harvinaisia yliherkkyysreaktioita, mukaan lukien pseudoallergiset / anafylaktoidiset reaktiot, on havaittu.
Luettelo haittavaikutuksista
Alla luetellut haittavaikutukset on luokiteltu esiintymistiheyden mukaan: hyvin yleinen (≥1 / 10), yleinen (≥1 / 100,
Immuunijärjestelmän häiriöt
Melko harvinainen: Systeemiset allergiset / pseudoallergiset reaktiot, mukaan lukien hengenvaaralliset anafylaktiset reaktiot.
Hermosto
Melko harvinainen: päänsärky
Ruoansulatuselimistö
Melko harvinainen: pahoinvointi
Lisääntymisjärjestelmän ja rintojen sairaudet
Yleinen: Lievää tai kohtalaista munasarjojen hyperstimulaatio -oireyhtymää (WHO: n luokka I tai II) voi esiintyä, mikä on tahdistusmenettelyn luontainen riski (ks. Kohta 4.4).
Melko harvinainen: Vaikea munasarjojen hyperstimulaatio -oireyhtymä (WHO: n luokka III)
Yleisoireet ja antopaikassa todettavat haitat
Yleinen: Pistoskohdan paikallisia reaktioita, kuten punoitusta, turvotusta ja kutinaa, on havaittu.
Epäillyistä haittavaikutuksista ilmoittaminen
Ilmoittaminen epäillyistä haittavaikutuksista, jotka ilmenevät lääkkeen myyntiluvan myöntämisen jälkeen, on tärkeä, koska se mahdollistaa lääkkeen hyöty -riskisuhteen jatkuvan seurannan. Terveydenhuollon ammattilaisia pyydetään ilmoittamaan kaikista epäillyistä haittavaikutuksista Italian lääkeviraston kautta. , verkkosivusto: http://www.agenziafarmaco.gov.it/it/responsabili.
04.9 Yliannostus -
Ihmisillä yliannostus voi pidentää vaikutuksen kestoa, mutta siihen ei todennäköisesti liity akuutteja toksisia vaikutuksia.
Jyrsijöillä tehdyissä akuutin toksisuuden kokeissa havaittiin epäspesifisiä toksisia oireita setroreliksin intraperitoneaalisen annon jälkeen, kun annokset olivat yli 200 kertaa suurempia kuin ihon alle annettavat farmakologisesti tehokkaat annokset.
05.0 FARMAKOLOGISET OMINAISUUDET -
05,1 "Farmakodynaamiset ominaisuudet -
Farmakoterapeuttinen ryhmä: gonadotropiinia vapauttavat hormonit, ATC-koodi: H01CC02
Toimintamekanismi
Cetrorelix on luteinisoivan hormonin vapauttavan hormonin (LHRH) antagonisti. LHRH sitoutuu aivolisäkkeen kalvoreseptoreihin. Cetroreliksi kilpailee endogeenisen LHRH: n sitoutumisesta LHRH -reseptoreihin Tämän toimintamekanismin ansiosta setroreliksi kontrolloi gonadotropiinien (LH ja FSH) eritystä.
Cetrorelix estää LH: n ja FSH: n aivolisäkkeen eritystä annoksesta riippuvaisella mekanismilla. Suppressio alkaa käytännössä välittömästi ja pysyy muuttumattomana jatkuvassa hoidossa ilman alkavaa stimulaatiovaikutusta.
Kliininen teho ja turvallisuus
Naisilla setroreliksi viivästyttää LH -erityksen alkamista ja siten ovulaatiota. Munasarjojen stimulaatiota saavilla naisilla setroreliksin vaikutuksen kesto riippuu annoksesta.Setroreliksin vaikutus säilyy toistuvilla injektioilla 24 tunnin välein 0,25 mg: n annoksella.
Sekä eläimillä että ihmisillä setroreliksin hormoniantagonistivaikutukset ovat täysin palautuvia hoidon lopettamisen jälkeen.
05,2 "Farmakokineettiset ominaisuudet -
Imeytyminen
Setrolixin absoluuttinen hyötyosuus ihonalaisen annon jälkeen on noin 85%.
Jakelu
Jakautumistilavuus (Vd) on 1,1 l x kg-1.
Eliminaatio
Plasman kokonaispuhdistuma ja munuaispuhdistuma ovat vastaavasti 1,2 ml x min-1x kg-1 ja 0,1 ml x min-1x kg-1.
Keskimääräiset terminaaliset puoliintumisajat laskimonsisäisen ja ihonalaisen annon jälkeen ovat noin 12 ja 30 tuntia, mikä vahvistaa injektiokohdan imeytymisprosessien tehokkuuden.
Lineaarisuus
Kerta -annoksen (0,25 mg - 3 mg setroreliksi) ihon alle antaminen sekä päivittäinen anto yli 14 päivän ajan osoittavat lineaarisen kinetiikan.
05.3 Prekliiniset tiedot turvallisuudesta -
Ei-kliiniset tiedot osoittavat, että tavanomaiset tutkimukset eivät viittaa erityiseen vaaraan ihmisille farmakologinen turvallisuus, toistuvan annoksen toksisuus, genotoksisuus, karsinogeenisuus, lisääntymistoksisuus.
Kokeellisissa tutkimuksissa, jotka koskivat akuuttia, subakuuttia tai kroonista toksisuutta hiirillä ja koirilla, setroreliksin ihon alle annettuna ei havaittu kohde -elintoksisuutta. Koiralle ei annettu merkkejä paikallisesta ärsytyksestä tai yhteensopimattomuudesta, kun sitä annettiin laskimonsisäisen, valtimonsisäisen ja laskimoon annetun injektion jälkeen, vaikka setroreliksiä annettiin paljon suurempia annoksia kuin ihmisille kliinisessä käytössä vahvistetut annokset.
Cetrorelix ei osoittanut mahdollisia mutageenisia tai klastogeenisiä vaikutuksia geeni- ja kromosomimutaatiotutkimuksissa.
06.0 FARMASEUTTISET TIEDOT -
06.1 Apuaineet -
Pöly:
Mannitoli
Liuotin:
Injektionesteisiin käytettävä vesi
06.2 Yhteensopimattomuus "-
Tätä lääkevalmistetta ei saa sekoittaa muiden lääkevalmisteiden kanssa, lukuun ottamatta niitä, jotka on mainittu kohdassa 6.6.
06.3 Voimassaoloaika "-
2 vuotta.
Liuos on käytettävä heti valmistuksen jälkeen.
06.4 Säilytystä koskevat erityiset varotoimet -
Säilytä alle 25 ° C.
Pidä injektiopullo (t) ulkopakkauksessa suojataksesi lääkettä valolta.
06.5 Välipakkauksen luonne ja pakkauksen sisältö -
Pakkaus, jossa on 1 tai 7 tyypin I lasipulloa suljettuna kumitulpalla.
Lisäksi pakkaus sisältää jokaiselle injektiopullolle:
1 esitäytetty ruisku (tyypin I lasipatruuna suljettuna kumitulpalla) ja 1 ml liuotinta parenteraaliseen käyttöön
1 injektioneula (20 gauge)
1 injektioneula (27 gauge)
2 alkoholipyyhettä.
Kaikkia pakkauskokoja ei välttämättä ole myynnissä.
06.6 Käyttö- ja käsittelyohjeet -
Cetrotide voidaan sekoittaa käyttövalmiiksi vain mukana tulevalla liuottimella ravistamalla injektiopulloa varovasti.
Vältä voimakkaita liikkeitä, jotka voivat johtaa kuplien muodostumiseen.
Käyttövalmis liuos on kirkas eikä siinä ole hiukkasia. Älä käytä, jos liuos sisältää hiukkasia tai ei ole kirkas.
Vedä koko injektiopullon sisältö, mikä varmistaa, että potilaalle annetaan vähintään 0,23 mg setroreliksiannosta.
Liuos on käytettävä heti käyttövalmiiksi saattamisen jälkeen.
Käyttämätön lääke ja tästä lääkkeestä syntyvät jätteet on hävitettävä paikallisten määräysten mukaisesti.
07.0 "MYYNTILUVAN HALTIJA" -
Merck Serono Europe Limited
56, Marsh Wall
Lontoo E14 9TP
Iso -Britannia
08.0 MYYNTILUVAN NUMERO -
EU/1/99/100/001
EU/1/99/100/002
034419010
034419022
09.0 MYYNTILUVAN MYYNTILUVAN TAI UUDISTAMISPÄIVÄMÄÄRÄ -
Myyntiluvan myöntämisen päivämäärä: 13. huhtikuuta 1999
Ensimmäisen uudistamispäivämäärä: 15. huhtikuuta 2004
Viimeisimmän uudistamisen päivämäärä: 13. huhtikuuta 2009
10.0 TEKSTIN MUUTTAMISPÄIVÄMÄÄRÄ -
04/2016
















.jpg)










