Mitä Extavia on?
Extavia on injektiokuiva -aine ja liuotin, liuosta varten.Sisältää 250 mikrogrammaa (8 miljoonaa kansainvälistä yksikköä, MIU) millilitraa kohden vaikuttavaa ainetta beeta-1b-interferonia.
Lääke on samanlainen kuin Betaferon, jolla on jo myyntilupa Euroopan unionissa (B).
Mihin Extaviaa käytetään?
Extaviaa käytetään multippeliskleroosia (MS) sairastavien aikuispotilaiden hoitoon. Multippeliskleroosi on tulehduksellinen sairaus, joka vaikuttaa keskushermostoon ja tapahtuu tuhoamalla hermosoluja suojaava vaippa. Tätä prosessia kutsutaan "demyelinaatioksi".
Extavia on tarkoitettu seuraavien sairauksien hoitoon:
• potilaat, joilla on ensimmäistä kertaa multippeliskleroosin (demyelinisoiva tapahtuma) merkkejä ja joiden oireet ovat riittävän vakavia, jotta kortikosteroidihoito (tulehduskipulääkkeet) olisi perusteltua. sairastua multippeliskleroosiin Ennen lääkärin määräämistä lääkärisi on suljettava pois oireiden muut syyt.
• potilaat, joilla on "relapsing-remitting" -tyyppinen multippeliskleroosi, jolle on tunnusomaista hyökkäykset (uusiutumiset) vuorotellen oireettomien kuukausien (remissioiden) kanssa, potilailla, joilla on vähintään kaksi uusiutumista kahden viime vuoden aikana;
• potilaat, joilla on sekundaarisesti etenevä multippeliskleroosi (MS-tauti, joka esiintyy uusiutuvan-remittisen multippeliskleroosin jälkeen), joilla on aktiivinen sairaus.
Lääkettä saa vain reseptillä.
Miten Extaviaa käytetään?
Extavia -hoidon saa aloittaa lääkäri, jolla on kokemusta multippeliskleroosin hoidosta. On suositeltavaa aloittaa 62,5 mikrogrammalla (neljäsosa annoksesta) joka toinen päivä ja lisätä määrää hitaasti 19 päivän aikana, jotta saavutetaan suositeltu annos 250 mikrogrammaa (8 MIU) joka päivä. Extavia annetaan injektiona ihon alle ( Potilas voi pistää lääkkeen itse saatuaan asianmukaiset ohjeet Extavia -hoito on lopetettava, jos potilas ei reagoi hoitoon.
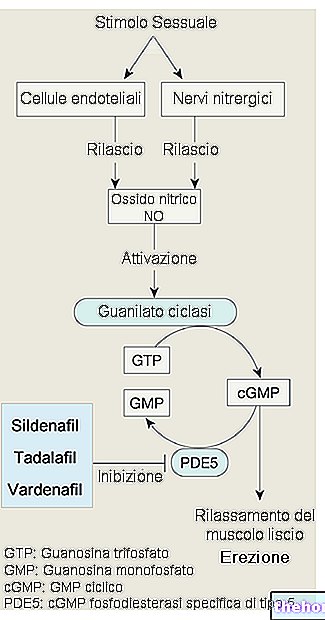
Miten Extavia vaikuttaa?
Extavian vaikuttava aine, beeta-1b-interferoni, kuuluu interferonien ryhmään. Interferonit ovat luonnollisia aineita, joita elimistö tuottaa auttaakseen selviytymään hyökkäyksistä, kuten virusinfektioista. Extavian vaikutusmekanismi multippeliskleroosin hoidossa ei ole vielä tiedossa, mutta näyttää siltä, että beetainterferoni pystyy säätelemään immuunijärjestelmää ( interferoni beeta-1b valmistetaan menetelmällä, joka tunnetaan nimellä "rekombinantti-DNA-tekniikka": eli se on saatu bakteerista, jossa se on A-geeni (DNA) Analoginen beeta-1b-interferoni toimii samalla tavalla kuin luonnollinen beeta-interferoni.
Miten Extaviaa on tutkittu?
Extaviaa tutkittiin 2 vuoden ajan 338 potilaalla, joilla oli uusiutuva-remittinen multippeliskleroosi ja jotka pystyivät kävelemään ilman apua, verraten sen tehoa lumelääkkeeseen (nukkehoito).
Extaviaa testattiin myös 1657 potilaalla kahdessa tutkimuksessa potilailla, joilla oli sekundaarisesti etenevä multippeliskleroosi ja jotka pystyivät kävelemään; näissä tutkimuksissa lääkettä verrattiin lumelääkkeeseen.
Extavia -tutkimuksessa potilailla, joilla oli yksi demyelinaatiotapahtuma, osallistui 487 potilasta, jotka saivat Extaviaa tai lumelääkettä kahden vuoden ajan. Tutkimuksessa mitattiin ajanjakso ennen multippeliskleroosin kliinisesti määritellyn muodon puhkeamista.
Mitä hyötyä Extaviasta on havaittu tutkimuksissa?
Potilailla, joilla oli uusiutuva-remittinen multippeliskleroosi, Extavia pienensi uusiutumisten määrää lumelääkettä tehokkaammin: lääkkeellä hoidetuilla potilailla esiintyi keskimäärin 0,84 uusiutumista vuodessa ja lumelääkettä saaneilla 1,27.
Yhdessä kahdesta tutkimuksesta, jotka tehtiin potilailla, joilla oli toissijainen etenevä multippeliskleroosi, havaittiin merkittävä viivästyminen vamman etenemisessä (31%: n riskin pieneneminen Extavian ansiosta) ja pidennys ennen aikaa, jolloin potilas on pakko "käyttää pyörätuolia (39%). Toisessa tutkimuksessa ei havaittu viivettä vamman etenemisessä. Molemmissa tutkimuksissa Extavia havaitsi kliinisten uusiutumisten määrän vähenevän (30%).
Tutkimuksessa, jossa potilailla oli yksi demyelinisoiva tapahtuma, Extavian osoitettiin vähentävän kliinisesti määritellyn multippeliskleroosin riskiä: 28%: lla Extavia -hoitoa saaneista potilaista kehittyi multippeliskleroosi verrattuna 45%: iin lumelääkettä saaneista potilaista.
Mitä riskejä Extaviaan liittyy?
Yleisimmät Extavian käytön yhteydessä havaitut sivuvaikutukset (useammalla kuin yhdellä potilaalla kymmenestä) olivat: flunssan oireet, kuume, vilunväristykset ja pistoskohdan reaktiot (kipu ja tulehdus). Pakkausselosteessa on luettelo kaikista Extavian ilmoitetuista sivuvaikutuksista.Extaviaa ei saa käyttää potilaille, joilla on aiemmin ollut yliherkkyyttä (allergiaa) luonnolliselle tai yhdistelmä -interferonibeetalle, ihmisen albumiinille tai jollekin muulle aineelle. Extavia -hoitoa ei saa aloittaa raskauden aikana. Potilaiden, jotka tulevat raskaaksi hoidon aikana, on neuvoteltava lääkärin kanssa. Lisäksi Extavia -valmistetta ei saa antaa potilaille, joilla on vaikea masennus ja / tai itsemurha -ajatuksia. Extaviaa ei ole tarkoitettu potilaille, joilla on dekompensoitu maksasairaus (jossa maksa ei pysty toimimaan normaalisti).
Miksi Extavia on hyväksytty?
Ihmisille tarkoitettuja lääkkeitä käsittelevä komitea (CHMP) katsoi, että Extavian hyödyt potilaiden hoidossa, joilla on yksi demyelinaatiotapahtuma, jos tämä tapahtuma on riittävän vakava, jotta se vaatii laskimonsisäisen kortikosteroidihoidon, potilaille, joilla on uusiutuva-remittinen multippeliskleroosipotilaita ja potilaat, joilla on sekundaarisesti etenevä multippeliskleroosi ja joilla on aktiivinen sairaus. Siksi CHMP suositteli myyntiluvan myöntämistä Extavialle.
Muita tietoja Extaviasta:
Euroopan komissio myönsi 20. toukokuuta 2008 Novartis Europharm Limitedille Extavian myyntiluvan, joka on voimassa koko Euroopan unionin alueella..
Extavian EPAR -arviointilausunnon täydellinen versio on täällä.
Tämän yhteenvedon viimeisin päivitys: 4-2008
Tällä sivulla julkaistut tiedot Extavia - interferoni beeta -1b: stä voivat olla vanhentuneita tai puutteellisia. Jos haluat käyttää näitä tietoja oikein, katso Vastuuvapauslauseke ja hyödyllisiä tietoja -sivu.










.jpg)