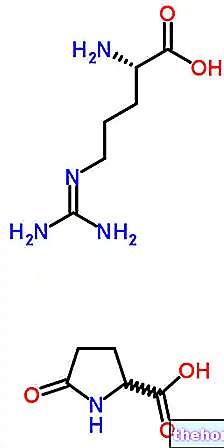
Vaikuttavat aineet: Darbepoetiini alfa
Aranesp 10 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
Aranesp 15 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
Aranesp 20 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
Aranesp 30 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
Aranesp 40 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
Aranesp 50 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
Aranesp 60 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
Aranesp 80 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
Aranesp 100 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
Aranesp 130 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
Aranesp 150 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
Aranesp 300 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
Aranesp 500 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
Aranesp -pakkausselosteita on saatavana seuraaviin pakkauskokoihin: - Aranesp 10 mikrogrammaa injektioneste, liuos esitäytetyssä ruiskussa, Aranesp 15 mikrogramman injektioneste, liuos esitäytetyssä ruiskussa, Aranesp 20 mikrogramman injektioneste, liuos esitäytetyssä ruiskussa, Aranesp 30 mikrogramman injektioneste, liuos esitäytetyssä ruiskussa, Aranesp 40 mikrogrammaa injektioneste, liuos 50 mikrogrammaa injektionestettä, Aranesp 40 mikrogrammaa injektioneste, liuos 50 mikrogrammaa injektioneste, liuos esitäytetyssä ruiskussa, Aranesp 60 mikrogramman injektioneste, liuos esitäytetyssä ruiskussa, Aranesp 80 mikrogramman injektioneste, liuos esitäytetyssä ruiskussa täytetty ruisku, Aranesp 100 mikrogrammaa injektioneste, liuos esitäytetyssä ruiskussa, Aranesp 130 mikrogrammaa injektioneste, liuos esitäytetyssä ruiskussa, Aranesp 150 mikrogrammaa injektioneste, liuos esitäytetyssä ruiskussa , Aranesp 150 mikrogrammaa injektioneste, liuos, esitäytetty ruisku 300 mikrogrammaa injektioneste, liuos esitäytetyssä ruiskussa
- Aranesp 10 mikrogramman injektioneste, liuos, esitäytetty kynä (SureClick), Aranesp 15 mikrogramman injektioneste, liuos, esitäytetty kynä (SureClick), Aranesp 20 mikrogramman injektioneste, liuos, esitäytetty kynä (SureClick), Aranesp 30 mikrogramman liuos injektio esitäytetyssä kynässä (SureClick), Aranesp 40 mikrogrammaa injektioneste, liuos, esitäytetty kynä (SureClick), Aranesp 50 mikrogrammaa injektioneste, esitäytetty kynä (SureClick), Aranesp 60 mikrogrammaa injektioneste, liuos, esitäytetty kynä (SureClick), Aranesp 80 mikrogrammaa injektioneste, liuos, esitäytetty kynä (SureClick), Aranesp 100 mikrogrammaa injektioneste, liuos, esitäytetty kynä (SureClick), Aranesp 130 mikrogramman injektioneste, liuos, esitäytetty kynä (SureClick), Aranesp 150 mikrogrammaa injektioneste, liuos, esitäytetty kynä (SureClick), Aranesp 300 mikrogrammaa injektioneste, liuos, esitäytetty kynä (SureClick), Aranesp 500 mikrogrammaa injektioneste, liuos esitäytetty kynä (SureClick
- Aranesp 25 mikrogrammaa injektioneste, liuos injektiopullossa, Aranesp 40 mikrogramman injektioneste, liuos injektiopullossa, Aranesp 60 mikrogramman injektioneste, liuos injektiopullossa, Aranesp 100 mikrogramman injektioneste, liuos injektiopullossa, Aranesp 200 mikrogramman injektioneste, liuos injektiopullossa, Aranesp 300 mikrogramman liuos injektio injektiopullossa
Miksi Aranespia käytetään? Mitä varten se on?
Lääkäri määräsi Aranespia (anemian vastaista ainetta) anemiansa hoitoon. Sinulla on anemia, kun veressä ei ole riittävästi punasoluja ja anemian oireita voivat olla uupumus, heikkous ja hengenahdistus.
Aranesp toimii täsmälleen samalla tavalla kuin luonnollinen erytropoietiinihormoni Erytropoietiinia tuottaa munuaiset ja se stimuloi luuytimen tuottamaan enemmän punasoluja. Aranespin vaikuttava aine on darbepoetiini alfa, joka on tuotettu geenitekniikalla kiinalaisen hamsterin munasarjasoluissa (CHO-K1).
Jos sinulla on krooninen munuaisten vajaatoiminta
Aranespia käytetään krooniseen munuaisten vajaatoimintaan liittyvän oireisen anemian hoitoon aikuisilla ja lapsilla.Munuaisten vajaatoiminnassa munuaiset eivät tuota tarpeeksi luonnollista erytropoietiinihormonia, mikä voi usein aiheuttaa anemiaa.
Kehosi kestää jonkin aikaa saada lisää punasoluja, ja sitten kestää noin neljä viikkoa, ennen kuin huomaat mitään vaikutuksia. Normaali dialyysi ei vaikuta Aranespin kykyyn hoitaa anemiaa.
Jos saat kemoterapiaa
Aranesp-valmistetta käytetään oireisen anemian hoitoon solunsalpaajahoitoa saavilla aikuispotilailla, joilla on ei-luuytimen kasvaimia (ei-myelooisia maligniteetteja).
Yksi kemoterapian tärkeimmistä sivuvaikutuksista on se, että se estää luuytimen tuottamasta tarpeeksi verisoluja. Kemoterapiahoidon loppupuolella, etenkin jos olet saanut paljon kemoterapiaa, punasolujen määrä voi laskea ja tehdä sinusta aneeminen.
Vasta -aiheet Milloin Aranespia ei saa käyttää
Älä käytä Aranesp -valmistetta
- jos olet allerginen darbepoetiini alfalle tai tämän lääkkeen jollekin muulle aineelle (lueteltu kohdassa 6).
- jos sinulla on diagnosoitu korkea verenpaine, joka ei ole tällä hetkellä hallinnassa muilla lääkärisi määräämillä lääkkeillä
Käyttöä koskevat varotoimet Mitä sinun on tiedettävä, ennen kuin otat Aranesp -valmistetta
Keskustele lääkärin, apteekkihenkilökunnan tai sairaanhoitajan kanssa ennen kuin käytät Aranesp -valmistetta.
Kerro lääkärillesi, jos sinulla on tai on ollut:
- korkea verenpaine, joka on tällä hetkellä hallinnassa lääkärin määräämillä lääkkeillä
- sirppisoluanemia;
- kouristukset (kouristukset)
- kouristukset (kohtaukset)
- maksasairaus;
- merkittävä vasteen puute anemian hoitoon käytettäville lääkkeille;
- allergia lateksille (esitäytetyn ruiskun neulansuojus sisältää lateksin johdannaista); tai
- hepatiitti C.
Erityisvaroitukset:
- Jos sinulla on oireita, kuten epätavallista väsymystä ja voimakkuuden laskua, sinulla voi olla puhdas punasoluaplasia (PRCA), jota on raportoitu potilailla. PRCA tarkoittaa, että elimistö lopettaa punasolujen tuotannon tai vähentää sen tuotantoa, mikä aiheuttaa vakavan anemian.Jos sinulla ilmenee näitä oireita, kerro niistä lääkärillesi, joka päättää parhaasta anemian hoitostrategiasta.
- Ole erityisen varovainen käyttäessäsi muita lääkkeitä, jotka stimuloivat punasolujen tuotantoa: Aranesp kuuluu valmisteryhmään, joka stimuloi punasolujen ja ihmisen erytropoietiinin tuotantoa. Terveydenhuollon ammattilaisen on aina tallennettava käyttämäsi lääkkeen oikea nimi.
- Lääkärisi tulee yrittää pitää hemoglobiinisi 10–12 g / dl. sydäninfarktin, aivohalvauksen ja kuoleman riski.
- Jos sinulla on krooninen munuaisten vajaatoiminta, vakavien sydän- tai verisuoniongelmien (sydän- ja verisuonitapahtumat) riski kasvaa, jos hemoglobiini pidetään liian korkeana.
- Jos sinulla on oireita, joihin kuuluu voimakasta päänsärkyä, uneliaisuutta, sekavuutta, näköongelmia, pahoinvointia, oksentelua tai kohtauksia, se voi tarkoittaa, että sinulla on erittäin korkea verenpaine. Jos koet näitä oireita, ota yhteys lääkäriisi.
- Jos sinulla on syöpä, sinun tulee olla tietoinen siitä, että Aranesp voi toimia verisolujen kasvutekijänä ja että se voi joissakin olosuhteissa vaikuttaa negatiivisesti syöpään. Tilanteesta riippuen verensiirto voi olla parempi. Keskustele tästä lääkärisi kanssa.
- Virheellinen käyttö terveillä koehenkilöillä voi aiheuttaa sydän- ja verisuoniongelmia, jotka asettavat tutkittavan välittömään hengenvaaraan.
Yhteisvaikutukset Mitkä lääkkeet tai elintarvikkeet voivat muuttaa Aranesp -valmisteen vaikutusta?
Muut lääkevalmisteet ja Aranesp
Kerro lääkärille tai apteekkihenkilökunnalle, jos parhaillaan käytät, olet äskettäin käyttänyt tai saatat käyttää muita lääkkeitä.
Punasolujen määrä voi vaikuttaa lääkkeisiin siklosporiiniin ja takrolimuusiin (immuunijärjestelmää lamaavat lääkkeet). On tärkeää, että kerrot lääkärillesi, jos käytät jotakin näistä lääkkeistä.
Aranesp ruuan ja juoman kanssa
Ruoka ja juoma eivät vaikuta Aranespiin.
Varoitukset On tärkeää tietää, että:
Raskaus ja imetys
Jos olet raskaana tai imetät, epäilet olevasi raskaana tai jos suunnittelet lapsen hankkimista, kysy lääkäriltä tai apteekista neuvoa ennen tämän lääkkeen käyttöä.
Aranespia ei ole testattu raskaana olevilla naisilla. On tärkeää kertoa lääkärille, jos:
- ovat raskaana;
- epäilet olevasi raskaana; tai
- suunnittelee raskautta.
Ei tiedetä, erittyykö darbepoetiini alfa äidinmaitoon. Jos käytät Aranesp -valmistetta, imetys on lopetettava.
Ajaminen ja koneiden käyttö
Aranespin ei odoteta rajoittavan ajokykyä tai koneiden käyttökykyä.
Aranesp sisältää natriumia
Tämä lääkevalmiste sisältää alle 1 mmol natriumia (23 mg) per annos, eli se on käytännössä natriumiton.
Annos, antotapa ja antamisaika Aranespin käyttö: Annostus
Käytä tätä lääkettä juuri siten kuin lääkäri tai apteekki on määrännyt. Jos olet epävarma, käänny lääkärin tai apteekkihenkilökunnan puoleen.
Lääkärisi on joidenkin verikokeiden perusteella päättänyt, että tarvitset Aranesp -valmistetta, koska hemoglobiinipitoisuutesi on 10 g / dl tai vähemmän. g / dl. Tämä voi vaihdella sen mukaan, onko kyseessä aikuinen vai lapsi.
Kuinka pistää itsellesi Aranesp
Lääkärisi voi päättää, että sinun tai hoitajasi on parasta pistää Aranesp. Lääkärisi, sairaanhoitajasi tai apteekkihenkilökunta näyttää sinulle, miten pistät itsellesi esitäytetyn ruiskun. Älä yritä pistää itseäsi, jos sinulle ei ole kerrottu, kuinka tehdä se. Älä koskaan pistä Aranespia itse laskimoon.
Jos sinulla on krooninen munuaisten vajaatoiminta
Kaikille ≥ 11 -vuotiaille aikuisille ja lapsipotilaille, joilla on krooninen munuaisten vajaatoiminta, Aranesp annetaan kerta -annoksena ihon alle (ihon alle) tai laskimoon (laskimonsisäisesti).
Aranespin aloitusannos painokiloa kohti anemian korjaamiseksi on:
- 0,75 mikrogrammaa kahden viikon välein tai
- 0,45 mikrogrammaa kerran viikossa.
Aikuispotilaille, jotka eivät ole dialyysihoidossa, voidaan käyttää myös 1,5 mikrogrammaa / kg kerran kuukaudessa aloitusannoksena.
Kaikki ≥ 11 -vuotiaat aikuispotilaat ja lapsipotilaat, joilla on krooninen munuaisten vajaatoiminta, kun heidän anemiansa on korjattu, saavat edelleen Aranesp -pistoksen kerta -annoksena joko kerran viikossa tai kahden viikon välein.Jos et ole dialyysissä, Aranesp voi myös pistoksena kerran kuukaudessa.
Lääkärisi käy säännöllisesti verikokeissa anemian vasteen tarkistamiseksi ja voi tarvittaessa muuttaa annostasi neljän viikon välein.
Kun anemia on korjattu, lääkärisi jatkaa säännöllisiä verikokeita ja annosta voidaan edelleen säätää anemian pitkäaikaisen hallinnan ylläpitämiseksi. Lääkäri ilmoittaa sinulle, jos annostusta muutetaan.
Verenpaineesi tarkistetaan myös säännöllisesti, erityisesti hoidon alussa.
Joissakin tapauksissa lääkäri voi ehdottaa, että otat raudan lisäravinteita.
Lääkärisi voi päättää muuttaa injektiotapaa (joko ihon alle tai laskimoon). verikokeita sen varmistamiseksi, että anemiaa hoidetaan aina oikein.
Jos lääkäri on päättänyt muuttaa hoitosi r-HuEPO: sta (geneettisellä tekniikalla tuotetusta erytropoietiinista) Aranesp-hoitoon, hän päättää myös, kuinka usein Aranesp-valmistetta tulee antaa kerran viikossa tai joka toinen viikko. r-HuEPO-hoitoon, mutta lääkäri kertoo sinulle, kuinka paljon ja milloin ottaa, ja voi tarvittaessa muuttaa annosta.
Jos saat kemoterapiaa
Aranesp annetaan kerran viikossa tai kerran kolmessa viikossa yhtenä pistoksena ihon alle.
Aloitusannos anemian korjaamiseksi on:
- 500 mikrogrammaa kerran kolmessa viikossa (6,75 mikrogrammaa Aranespia painokiloa kohti) tai
- 2,25 mikrogrammaa (kerran viikossa) Aranespia painokiloa kohti.
Lääkärisi käy säännöllisesti verikokeissa anemian vasteen tarkistamiseksi ja voi muuttaa annosta tarpeen mukaan. Hoitoa jatketaan noin neljän viikon ajan solunsalpaajahoidon päättymisen jälkeen. Aranesp.
Joissakin tapauksissa lääkäri voi ehdottaa, että otat raudan lisäravinteita.
Ohjeet itsesi pistämiseen esitäytetyllä Aranesp-ruiskulla
Tämä osio sisältää tietoja Aranesp -pistoksen pistämisestä itse. On tärkeää, ettet yritä pistää itseäsi, jos lääkäri, sairaanhoitaja tai apteekki ei ole kertonut sinulle, miten pistät pistoksen. Jos sinulla on kysyttävää pistoksesta, kysy lääkäriltäsi, sairaanhoitajalta tai apteekista.
Aranespin käyttö esitäytetyssä ruiskussa sinun tai pistoksen antavan henkilön toimesta
Lääkärisi on määrännyt Aranesp-injektionestettä esitäytetyssä ruiskussa injektoitavaksi välittömästi ihon alle.
Mitä tarvitaan:
Pistoksen antamiseksi tarvitset:
- uusi Aranesp-esitäytetty ruisku; Ja
- alkoholipyyhkeitä tai vastaavia desinfiointiaineita.
Mitä minun pitäisi tehdä ennen kuin annan itselleni "ihonalaisen Aranesp -injektion"?
- Ota esitäytetty ruisku jääkaapista. Jätä esitäytetty ruisku huoneenlämpöön noin 30 minuutiksi. Tämä tekee injektiosta mukavampaa.Älä lämmitä Aranesp -laitetta millään muulla tavalla (kuten mikroaaltouunissa tai kuumassa vedessä) Älä myöskään jätä ruiskua suoraan auringonvaloon.
- Älä ravista esitäytettyä ruiskua.
- Älä poista neulan korkkia ruiskusta ennen kuin olet valmis pistämään.
- Tarkista, että annos on sama kuin lääkärisi määräämä.
- Tarkista viimeinen käyttöpäivämäärä esitäytetyn ruiskun etiketistä (EXP) .Älä käytä sitä, jos se on kuukauden viimeisen päivän jälkeen.
- Tarkista Aranespin ulkonäkö. Sen on oltava kirkas, väritön tai hieman opaalinhohtoinen neste. Jos se on sameaa tai siinä näkyy hiukkasia, älä käytä sitä.
- Pese kädet huolellisesti.
- Löydä mukava, hyvin valaistu, puhdas pinta ja pidä kaikki tarvitsemasi lähellä.
Miten valmistan Aranesp -injektion?
Ennen kuin pistät Aranesp -pistoksen, sinun on toimittava seuraavasti: 1. Vältä neulan taittuminen irrottamalla neulansuojus varovasti kiertämättä sitä kuvien 1 ja 2 mukaisesti. 2. Älä koske neulaan äläkä työnnä mäntää. 3. Saatat huomata pienen ilmakuplan esitäytetyssä ruiskussa. Älä poista ilmakuplaa ennen pistämistä. Liuoksen pistäminen ilmakuplilla on vaaratonta. 4. Voit nyt käyttää esitäytettyä ruiskua.
Mistä pistos annetaan?
Parhaat pistoskohdat ovat reidet ja vatsa. Jos joku muu antaa sinulle pistoksen, voit käyttää myös käsivarsiasi.
Vaihda pistoskohtaa, jos huomaat, että alue on punainen tai kipeä.
Miten pistän pistoksen itselleni?
- Desinfioi iho alkoholipyyhkeellä ja nosta iho peukalon ja etusormen väliin (puristamatta sitä).
- Työnnä neula kokonaan ihoon lääkärin, sairaanhoitajan tai apteekin osoittamalla tavalla.
- Pistä määrätty annos ihon alle lääkärin, sairaanhoitajan tai apteekkihenkilökunnan ohjeiden mukaan.
- Paina mäntää hitaasti, tasaisesti ja pidä iho aina puristettuna, kunnes ruisku on tyhjä.
- Vedä neula ulos ja päästä iholta.
- Jos huomaat veripisteen, voit painaa puuvillapalloa tai sideharsoa varovasti pistoskohtaan. Älä hiero pistoskohtaa. Tarvittaessa voit peittää pistoskohdan teipillä.
- Käytä jokaista ruiskua vain yhteen pistokseen. Älä käytä ruiskuun jäänyttä Aranesp -valmistetta uudelleen.
Muista: Jos sinulla on ongelmia, älä epäröi kysyä neuvoa lääkäriltäsi tai sairaanhoitajalta.
Käytettyjen ruiskujen hävittäminen
- Älä laita korkkia takaisin käytettyjen neulojen päälle, sillä voit pistää vahingossa itsesi.
- Pidä käytetyt ruiskut poissa lasten ulottuvilta ja näkyviltä.
- Käytetyt esitäytetyt ruiskut on hävitettävä paikallisten vaatimusten mukaisesti. Kysy apteekista, miten heität pois lääkkeet, joita et enää käytä. Tämä auttaa suojelemaan ympäristöä.
Yliannostus Mitä tehdä, jos olet ottanut liian paljon Aranesp -valmistetta?
Jos käytät enemmän Aranesp -valmistetta kuin sinun pitäisi
Sinulla voi olla vakavia ongelmia, jos otat enemmän Aranesp -valmistetta kuin tarvitset, kuten erittäin korkea verenpaine. Jos näin käy, ota yhteys lääkäriisi, sairaanhoitajaasi tai apteekkiin.Jos tunnet olosi huonoksi, ota välittömästi yhteys lääkäriin, sairaanhoitajaan tai apteekkiin.
Jos unohdat käyttää Aranespia
Älä ota kaksinkertaista annosta korvataksesi unohtamasi annoksen.
Jos olet unohtanut Aranesp -annoksen, ota yhteys lääkäriisi selvittääksesi, milloin sinun tulee ottaa seuraava pistos.
Jos lopetat Aranespin käytön
Jos haluat lopettaa Aranespin käytön, keskustele asiasta ensin lääkärisi kanssa.
Sivuvaikutukset Mitkä ovat Aranespin sivuvaikutukset?
Kuten kaikki lääkkeet, tämäkin lääke voi aiheuttaa haittavaikutuksia. Kaikki eivät kuitenkaan niitä saa.
Aranesp -hoidon jälkeen joillakin potilailla esiintyi seuraavia haittavaikutuksia:
Potilaat, joilla on krooninen munuaisten vajaatoiminta
Hyvin yleinen: voi esiintyä useammalla kuin yhdellä potilaalla 10: stä
- Korkea verenpaine (hypertensio)
- Allergiset reaktiot
Yleinen: voi esiintyä enintään 1 käyttäjällä 10: stä
- Aivohalvaus
- Kipu pistoskohdassa
- Ihottuma ja / tai ihon punoitus
Melko harvinainen: voi esiintyä enintään 1 käyttäjällä 100: sta
- Veritulpat (tromboosi)
- Kouristukset (kohtaukset)
Tuntematon: esiintymistiheyttä ei voida arvioida saatavilla olevien tietojen perusteella
- Puhdas punasoluaplasia (PRCA) - (anemia, epätavallinen väsymys, voiman menetys)
Syöpäpotilaat
Hyvin yleinen: voi esiintyä useammalla kuin yhdellä potilaalla 10: stä
- Allergiset reaktiot
- Nesteen kertyminen (turvotus)
Yleinen: voi esiintyä enintään 1 käyttäjällä 10: stä
- Korkea verenpaine (hypertensio)
- Veritulpat (tromboosi)
- Kipu pistoskohdassa
- Ihottuma ja / tai ihon punoitus
Melko harvinainen: voi esiintyä enintään 1 käyttäjällä 100: sta
- Kouristukset (kohtaukset)
Kaikki potilaat
Tuntematon: esiintymistiheyttä ei voida arvioida saatavilla olevien tietojen perusteella
Vakavat allergiset reaktiot, joihin voi kuulua:
- Äkilliset allergiset reaktiot, jotka voivat olla hengenvaarallisia (anafylaksia)
- Kasvojen, huulten, suun, kielen tai kurkun turvotus, joka voi vaikeuttaa nielemistä tai hengittämistä (angioedeema)
- Hengenahdistus (allerginen bronkospasmi)
- Ihottumia
- Nokkosihottuma
Jos havaitset haittavaikutuksia, käänny lääkärin tai apteekkihenkilökunnan puoleen, mukaan lukien mahdolliset haittavaikutukset, joita ei ole mainittu tässä pakkausselosteessa.
Vanhentuminen ja säilyttäminen
Ei lasten ulottuville eikä näkyville.
Älä käytä tätä lääkettä pakkauksessa ja esitäytetyn ruiskun etiketissä mainitun viimeisen käyttöpäivämäärän (EXP) jälkeen. Viimeinen käyttöpäivämäärä on kuukauden viimeinen päivä.
Säilytä jääkaapissa (2 ° C - 8 ° C). Ei saa jäätyä. Älä käytä Aranesp -valmistetta, jos se on mielestäsi jäätynyt.
Pidä esitäytetty ruisku ulkopakkauksessa suojataksesi lääkettä valolta.
Kun ruisku on otettu pois jääkaapista ja jätetty huoneenlämpöön noin 30 minuutiksi ennen injektiota, se on joko käytettävä 7 päivän kuluessa tai hävitettävä.
Älä käytä tätä lääkettä, jos huomaat, että esitäytetyn ruiskun sisältö on sameaa tai siinä on näkyviä hiukkasia.
Älä heitä lääkkeitä viemäriin tai talousjätteisiin. Kysy apteekista, kuinka heittää pois lääkkeet, joita et enää käytä. Tämä auttaa suojelemaan ympäristöä.
Koostumus ja lääkemuoto
Mitä Aranesp sisältää
- Vaikuttava aine on darbepoetiini alfa, r-HuEPO (geenitekniikalla tuotettu erytropoietiini). Esitäytetty ruisku sisältää 10, 15, 20, 30, 40, 50, 60, 80, 100, 130, 150, 300 tai 500 mikrogrammaa darbepoetiini alfaa.
- Muut aineet ovat yksiemäksinen natriumfosfaatti, kaksiemäksinen natriumfosfaatti, natriumkloridi, polysorbaatti 80 ja injektionesteisiin käytettävä vesi.
Lääkevalmisteen kuvaus ja pakkaus
Aranesp on kirkas, väritön tai hieman opalisoiva injektioneste, liuos esitäytetyssä ruiskussa.
Aranesp on saatavana 1 tai 4 esitäytetyn ruiskun pakkauksissa. Ruiskut on pakattu läpipainopakkauksiin (1 tai 4 ruiskun pakkaukset) tai ilman rakkuloita (1 ruiskun pakkaukset). Kaikkia pakkauskokoja ei välttämättä ole myynnissä.
Lähdepakkaus: AIFA (Italian lääkevirasto). Sisältö julkaistu tammikuussa 2016. Esitetyt tiedot eivät välttämättä ole ajan tasalla.
Jotta saat käyttöösi uusimman version, on suositeltavaa käyttää AIFA: n (Italian Medicines Agency) verkkosivustoa. Vastuuvapauslauseke ja hyödyllistä tietoa.
01.0 LÄÄKEVALMISTEEN NIMI
ARANESP
02.0 LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS
Aranesp 10 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
Yksi esitäytetty ruisku sisältää 10 mikrogrammaa darbepoetiini alfaa 0,4 ml: ssa (25 mikrogrammaa / ml).
Aranesp 15 mikrogrammaa injektioneste, liuos, esitäytetty ruiskuYksi esitäytetty ruisku sisältää 15 mcg darbepoetiini alfaa 0,375 ml: ssa (40 mcg / ml).
Aranesp 20 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
Yksi esitäytetty ruisku sisältää 20 mikrogrammaa darbepoetiini alfaa 0,5 ml: ssa (40 mikrogrammaa / ml).
Aranesp 30 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
Yksi esitäytetty ruisku sisältää 30 mikrogrammaa darbepoetiini alfaa 0,3 ml: ssa (100 mikrogrammaa / ml).
Aranesp 40 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
Yksi esitäytetty ruisku sisältää 40 mcg darbepoetiini alfaa 0,4 ml: ssa (100 mcg / ml).
Aranesp 50 mcg injektioneste, liuos esitäytetyssä ruiskussaYksi esitäytetty ruisku sisältää 50 mcg darbepoetiini alfaa 0,5 ml: ssa (100 mcg / ml).
Aranesp 60 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
Yksi esitäytetty ruisku sisältää 60 mcg darbepoetiini alfaa 0,3 ml: ssa (200 mcg / ml).
Aranesp 80 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
Yksi esitäytetty ruisku sisältää 80 mikrogrammaa darbepoetiini alfaa 0,4 ml: ssa (200 mcg / ml).
Aranesp 100 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
Yksi esitäytetty ruisku sisältää 100 mcg darbepoetiini alfaa 0,5 ml: ssa (200 mcg / ml).
Aranesp 130 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
Yksi esitäytetty ruisku sisältää 130 mikrogrammaa darbepoetiini alfaa 0,65 ml: ssa (200 mikrog / ml).
Aranesp 150 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
Yksi esitäytetty ruisku sisältää 150 mcg darbepoetiini alfaa 0,3 ml: ssa (500 mcg / ml).
Aranesp 300 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
Yksi esitäytetty ruisku sisältää 300 mcg darbepoetiini alfaa 0,6 ml: ssa (500 mcg / ml).
Aranesp 500 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
Yksi esitäytetty ruisku sisältää 500 mcg darbepoetiini alfaa 1 ml: ssa (500 mcg / ml).
Aranesp 10 mikrogrammaa injektioneste, liuos, esitäytetty kynä
Yksi esitäytetty kynä sisältää 10 mikrogrammaa darbepoetiini alfaa 0,4 ml: ssa (25 mikrogrammaa / ml).
Aranesp 15 mikrogrammaa injektioneste, liuos, esitäytetty kynä
Yksi esitäytetty kynä sisältää 15 mikrogrammaa darbepoetiini alfaa 0,375 ml: ssa (40 mcg / ml).
Aranesp 20 mikrogrammaa injektioneste, liuos, esitäytetty kynä
Yksi esitäytetty kynä sisältää 20 mikrogrammaa darbepoetiini alfaa 0,5 ml: ssa (40 mikrogrammaa / ml).
Aranesp 30 mikrogrammaa injektioneste, liuos, esitäytetty kynä
Yksi esitäytetty kynä sisältää 30 mikrogrammaa darbepoetiini alfaa 0,3 ml: ssa (100 mikrogrammaa / ml).
Aranesp 40 mikrogrammaa injektioneste, liuos, esitäytetty kynä
Yksi esitäytetty kynä sisältää 40 mikrogrammaa darbepoetiini alfaa 0,4 ml: ssa (100 mikrogrammaa / ml).
Aranesp 50 mcg injektioneste, liuos, esitäytetty kynä
Yksi esitäytetty kynä sisältää 50 mikrogrammaa darbepoetiini alfaa 0,5 ml: ssa (100 mikrogrammaa / ml).
Aranesp 60 mikrogrammaa injektioneste, liuos, esitäytetty kynä
Yksi esitäytetty kynä sisältää 60 mikrogrammaa darbepoetiini alfaa 0,3 ml: ssa (200 mikrogrammaa / ml).
Aranesp 80 mikrogrammaa injektioneste, liuos, esitäytetty kynä
Yksi esitäytetty kynä sisältää 80 mikrogrammaa darbepoetiini alfaa 0,4 ml: ssa (200 mikrogrammaa / ml).
Aranesp 100 mcg injektioneste, liuos, esitäytetty kynä
Yksi esitäytetty kynä sisältää 100 mikrogrammaa darbepoetiini alfaa 0,5 ml: ssa (200 mikrog / ml).
Aranesp 130 mcg injektioneste, liuos, esitäytetty kynä
Yksi esitäytetty kynä sisältää 130 mikrogrammaa darbepoetiini alfaa 0,65 ml: ssa (200 mcg / ml).
Aranesp 150 mikrogrammaa injektioneste, liuos, esitäytetty kynä
Yksi esitäytetty kynä sisältää 150 mcg darbepoetiini alfaa 0,3 ml: ssa (500 mcg / ml).
Aranesp 300 mcg injektioneste, liuos, esitäytetty kynä
Yksi esitäytetty kynä sisältää 300 mcg darbepoetiini alfaa 0,6 ml: ssa (500 mcg / ml).
Aranesp 500 mcg injektioneste, liuos, esitäytetty kynä
Yksi esitäytetty kynä sisältää 500 mcg darbepoetiini alfaa 1 ml: ssa (500 mcg / ml).
Aranesp 25 mcg injektioneste, liuos injektiopullossa
Yksi injektiopullo sisältää 25 mikrogrammaa darbepoetiini alfaa 1 ml: ssa (25 mikrogrammaa / ml).
Aranesp 40 mcg injektioneste, liuos injektiopullossa
Jokainen injektiopullo sisältää 40 mcg darbepoetiini alfaa 1 ml: ssa (40 mcg / ml).
Aranesp 60 mcg injektioneste, liuos injektiopullossa
Yksi injektiopullo sisältää 60 mcg darbepoetiini alfaa 1 ml: ssa (60 mcg / ml).
Aranesp 100 mcg injektioneste, liuos injektiopullossa
Yksi injektiopullo sisältää 100 mcg darbepoetiini alfaa 1 ml: ssa (100 mcg / ml).
Aranesp 200 mcg injektioneste, liuos injektiopullossa
Yksi injektiopullo sisältää 200 mcg darbepoetiini alfaa 1 ml: ssa (200 mcg / ml).
Aranesp 300 mcg injektioneste, liuos, injektiopullo
Yksi injektiopullo sisältää 300 mcg darbepoetiini alfaa 1 ml: ssa (300 mcg / ml).
Darbepoetiini alfa tuotetaan geenitekniikalla kiinalaisen hamsterin munasarjasoluissa (CHO-K1).
Apuaine, jolla on tunnettuja vaikutuksia:
Aranesp 10 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
Yksi esitäytetty ruisku sisältää 1,52 mg natriumia 0,4 ml: ssa.
Aranesp 15 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
Yksi esitäytetty ruisku sisältää 1,42 mg natriumia 0,375 ml: ssa.
Aranesp 20 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
Yksi esitäytetty ruisku sisältää 1,90 mg natriumia 0,5 ml: ssa.
Aranesp 30 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
Yksi esitäytetty ruisku sisältää 1,14 mg natriumia 0,3 ml: ssa.
Aranesp 40 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
Yksi esitäytetty ruisku sisältää 1,52 mg natriumia 0,4 ml: ssa.
Aranesp 50 mcg injektioneste, liuos esitäytetyssä ruiskussa
Yksi esitäytetty ruisku sisältää 1,90 mg natriumia 0,5 ml: ssa.
Aranesp 60 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
Yksi esitäytetty ruisku sisältää 1,14 mg natriumia 0,3 ml: ssa.
Aranesp 80 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
Yksi esitäytetty ruisku sisältää 1,52 mg natriumia 0,4 ml: ssa.
Aranesp 100 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
Yksi esitäytetty ruisku sisältää 1,90 mg natriumia 0,5 ml: ssa.
Aranesp 130 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
Yksi esitäytetty ruisku sisältää 2,46 mg natriumia 0,65 ml: ssa.
Aranesp 150 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
Yksi esitäytetty ruisku sisältää 1,14 mg natriumia 0,3 ml: ssa.
Aranesp 300 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
Yksi esitäytetty ruisku sisältää 2,27 mg natriumia 0,6 ml: ssa.
Aranesp 500 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
Yksi esitäytetty ruisku sisältää 3,79 mg natriumia 1 ml: ssa.
Aranesp 10 mikrogrammaa injektioneste, liuos, esitäytetty kynä
Yksi esitäytetty kynä sisältää 1,52 mg natriumia 0,4 ml: ssa.
Aranesp 15 mikrogrammaa injektioneste, liuos, esitäytetty kynä
Yksi esitäytetty kynä sisältää 1,42 mg natriumia 0,375 ml: ssa.
Aranesp 20 mikrogrammaa injektioneste, liuos, esitäytetty kynä
Yksi esitäytetty kynä sisältää 1,90 mg natriumia 0,5 ml: ssa.
Aranesp 30 mikrogrammaa injektioneste, liuos, esitäytetty kynä
Yksi esitäytetty kynä sisältää 1,14 mg natriumia 0,3 ml: ssa.
Aranesp 40 mikrogrammaa injektioneste, liuos, esitäytetty kynä
Yksi esitäytetty kynä sisältää 1,52 mg natriumia 0,4 ml: ssa.
Aranesp 50 mcg injektioneste, liuos, esitäytetty kynä
Yksi esitäytetty kynä sisältää 1,90 mg natriumia 0,5 ml: ssa.
Aranesp 60 mikrogrammaa injektioneste, liuos, esitäytetty kynä
Yksi esitäytetty kynä sisältää 1,14 mg natriumia 0,3 ml: ssa.
Aranesp 80 mikrogrammaa injektioneste, liuos, esitäytetty kynä
Yksi esitäytetty kynä sisältää 1,52 mg natriumia 0,4 ml: ssa.
Aranesp 100 mcg injektioneste, liuos, esitäytetty kynä
Yksi esitäytetty kynä sisältää 1,90 mg natriumia 0,5 ml: ssa.
Aranesp 130 mcg injektioneste, liuos, esitäytetty kynä
Yksi esitäytetty kynä sisältää 2,46 mg natriumia 0,65 ml: ssa.
Aranesp 150 mikrogrammaa injektioneste, liuos, esitäytetty kynä
Yksi esitäytetty kynä sisältää 1,14 mg natriumia 0,3 ml: ssa.
Aranesp 300 mcg injektioneste, liuos, esitäytetty kynä
Yksi esitäytetty kynä sisältää 2,27 mg natriumia 0,6 ml: ssa.
Aranesp 500 mcg injektioneste, liuos, esitäytetty kynä
Yksi esitäytetty kynä sisältää 3,79 mg natriumia 1 ml: ssa.
Aranesp 25 mcg injektioneste, liuos injektiopullossa
Yksi injektiopullo sisältää 3,79 mg natriumia.
Aranesp 40 mcg injektioneste, liuos injektiopullossa
Yksi injektiopullo sisältää 3,79 mg natriumia.
Aranesp 60 mcg injektioneste, liuos injektiopullossa
Yksi injektiopullo sisältää 3,79 mg natriumia.
Aranesp 100 mcg injektioneste, liuos injektiopullossa
Yksi injektiopullo sisältää 3,79 mg natriumia.
Aranesp 200 mcg injektioneste, liuos injektiopullossa
Yksi injektiopullo sisältää 3,79 mg natriumia.
Aranesp 300 mcg injektioneste, liuos injektiopullossa
Yksi injektiopullo sisältää 3,79 mg natriumia.
Täydellinen apuaineluettelo, katso kohta 6.1.
03.0 LÄÄKEMUOTO
Injektioneste (injektio) esitäytetyssä ruiskussa.
Injektioneste (injektio) esitäytetyssä kynässä (SureClick).
Injektioneste (injektio) injektiopullossa.
Kirkas, väritön liuos.
04.0 KLIINISET TIEDOT
04.1 Käyttöaiheet
Krooniseen munuaisten vajaatoimintaan (CRI) liittyvän oireisen anemian hoito aikuisilla ja lapsipotilailla (ks. Kohta 4.2).
Oireisen anemian hoito solunsalpaajahoitoa saavilla aikuispotilailla, joilla on ei-myelooinen maligniteetti.
04.2 Annostus ja antotapa
Aranesp -hoidon saa aloittaa edellä mainittuihin käyttöaiheisiin perehtynyt lääkäri.
Annostus
Oireisen anemian hoito aikuisilla ja lapsipotilailla, joilla on krooninen munuaisten vajaatoiminta
Anemian oireet ja seuraukset voivat vaihdella iän, sukupuolen ja sairauden yleisen vakavuuden mukaan; siksi on välttämätöntä, että lääkäri arvioi kunkin yksittäisen potilaan kliinisen kulun ja olosuhteet. Aranesp on annettava ihon alle tai laskimoon hemoglobiinipitoisuuden nostamiseksi enintään 12 g / dl (7,5 mmol / l). Ihonalainen käyttö on suositeltavaa potilaille, joille ei suoriteta hemodialyysiä, perifeeristen laskimoiden puhkeamisen välttämiseksi.
Potilaita on seurattava tarkasti anemian oireiden riittävän hallinnan saavuttamiseksi käyttämällä pienintä hyväksyttyä Aranesp -annosta samalla, kun hemoglobiinipitoisuus pidetään alle tai yhtä suuri kuin 12 g / dl (7,5 mmol / l). Varovaisuutta on noudatettava suurentavilla Aranesp -annoksilla potilailla, joilla on krooninen munuaisten vajaatoiminta.
Jos potilaalla on heikko hemoglobiinivaste Aranesp -hoitoon, tulee harkita huonon vasteen vaihtoehtoisia syitä (ks. Kohdat 4.4 ja 5.1).
Potilaan sisäisen vaihtelun vuoksi yksittäisellä hemoglobiiniarvolla voidaan toisinaan havaita haluttua hemoglobiinitasoa korkeammalla ja alhaisemmalla tasolla. Hemoglobiinin vaihtelua tulee hallita annosta säätämällä ottaen huomioon hemoglobiinin tavoitealue, joka on 10 g / dl (6,2 mmol / l) - 12 g / dl (7,5 mmol / l). g / dl (7,5 mmol / l) tulee välttää; alla on ohjeet asianmukaisen annoksen säätämisestä hemoglobiiniarvoille, jotka ovat yli 12 g / dl (7,5 mmol / l). mmol / l) 4 viikon aikana tulisi myös välttää. Jos näin käy, annosta on muutettava.
Aranesp -hoito on jaettu kahteen vaiheeseen, korjausvaiheeseen ja ylläpitovaiheeseen. Ohjeet annetaan erikseen aikuisille ja lapsipotilaille.
Aikuiset potilaat, joilla on krooninen munuaisten vajaatoiminta
Korjausvaihe:
Ihon alle tai laskimoon annettavan aloitusannoksen on 0,45 mcg painokiloa kohti kertainjektiona kerran viikossa. Vaihtoehtoisesti seuraavat aloitusannokset voidaan antaa myös ihon alle kerta -annoksena potilaille, jotka eivät ole dialyysihoidossa: 0,75 mcg / kg kahden viikon välein tai 1,5 mcg / kg kerran kuukaudessa. Jos hemoglobiinin nousu on riittämätön (alle 1 g / dl (0,6 mmol / l) neljän viikon aikana), annosta on lisättävä noin 25%. Annosta ei saa nostaa useammin kuin kerran 4 viikossa.
Jos hemoglobiinin nousu on yli 2 g / dl (1,25 mmol / l) neljän viikon aikana, annosta on pienennettävä noin 25%.Jos hemoglobiiniarvo on yli 12 g / dl (7,5 mmol / l), annoksen pienentämistä on harkittava. Jos hemoglobiini jatkaa nousuaan, annosta on pienennettävä noin 25%.Jos hemoglobiiniarvo kasvaa edelleen annoksen pienentämisen jälkeen, anto on keskeytettävä väliaikaisesti, kunnes annosta pienennetään. " annoksella, joka on noin 25% pienempi kuin edellinen annos.
Hemoglobiini on mitattava 1-2 viikon välein, kunnes se on vakiintunut, ja sen jälkeen hemoglobiini voidaan mitata pitemmillä aikaväleillä.
Huoltovaihe:
Dialyysipotilailla Aranesp -valmistetta voidaan jatkaa kerta -annoksena kerran viikossa tai kerran kahdessa viikossa. Dialyysipotilaiden, jotka siirtyvät kerran viikossa Aranesp -valmisteesta kahden viikon välein, tulee aluksi saada annos, joka vastaa kaksi kertaa edellistä viikoittaista annosta.
Potilaille, jotka eivät saa dialyysihoitoa, Aranesp -valmistetta voidaan jatkaa kerta -annoksena kerran viikossa tai kerran kahdessa viikossa tai kerran kuukaudessa. Aranesp -hoitoa saaville potilaille kerran kahdessa viikossa hemoglobiinipitoisuuden saavuttamisen jälkeen Aranesp voidaan antaa ihonalaisena injektiona kerran kuukaudessa.
Annosta on titrattava tarpeen mukaan hemoglobiinin tavoitepitoisuuden ylläpitämiseksi.
Jos annoksen muuttaminen on tarpeen hemoglobiinin pitämiseksi halutulla tasolla, on suositeltavaa muuttaa annosta noin 25%.
Jos hemoglobiinin nousu on yli 2 g / dl (1,25 mmol / l) neljän viikon aikana, annosta on pienennettävä noin 25%nousun nopeudesta riippuen. On suurempi kuin 12 g / dl (7,5 mmol) Jos hemoglobiini jatkaa nousuaan, annosta on pienennettävä noin 25%. Jos hemoglobiiniarvo jatkaa nousuaan annoksen pienentämisen jälkeen, anto on keskeytettävä väliaikaisesti, kunnes hemoglobiiniarvo laskee, jolloin hoito aloitetaan uudelleen noin 25% pienemmällä annoksella kuin edellinen.
Kun annosta tai annosteluohjelmaa on muutettu, hemoglobiini on tarkistettava 1-2 viikon välein.Hoitovaiheen annosta ei saa muuttaa useammin kuin kerran kahdessa viikossa.
Kun antoreittiä muutetaan, on käytettävä samaa annosta ja hemoglobiini on tarkistettava 1-2 viikon välein, jotta annosta voidaan muuttaa niin, että hemoglobiini pysyy halutulla tasolla.
Kliiniset tutkimukset ovat osoittaneet, että aikuispotilaat, jotka saavat r-HuEPO-valmistetta kerran, kahdesti tai kolme kertaa viikossa, voivat vaihtaa Aranesp-hoitoon kerran viikossa tai joka toinen viikko. Aranespin viikoittainen aloitusannos (mcg / viikko) voidaan laskea jakamalla r-HuEPO: n viikoittainen kokonaisannos (IU / viikko) 200: lla. Kahden viikon välein annettavan Aranespin aloitusannos (mcg kahden viikon ajan) voidaan laskea jakamalla kahden viikon jakson aikana annetun r-HuEPO: n kokonaisannos 200: lla. Yksilöllisen vaihtelun vuoksi odotetaan, että annosta on muutettava yksilöllisen potilaan optimaalisen terapeuttisen annoksen määrittämiseksi. Kun r-HuEPO korvataan Aranespilla, hemoglobiini on tarkistettava 1-2 viikon välein ja samaa antotapaa on käytettävä.
Pediatriset potilaat, joilla on krooninen munuaisten vajaatoiminta
Ei ole tietoja alle 1 -vuotiaiden lapsipotilaiden hoidosta satunnaistetuissa kliinisissä tutkimuksissa (ks. Kohta 5.1).
Korjausvaihe:
≥ 1 -vuotiaille potilaille ihon alle tai laskimoon annettavan aloitusannoksen on 0,45 mcg painokiloa kohden kertainjektiona kerran viikossa. Vaihtoehtoisesti potilaille, jotka eivät saa dialyysihoitoa, voidaan antaa aloitusannos 0,75 mcg / kg kerta -annoksena ihon alle kahden viikon välein. Jos hemoglobiinin nousu on riittämätön (alle 1 g / dl (0,6 mmol / l) neljän viikon aikana), annosta on lisättävä noin 25%. Annosta ei saa nostaa useammin kuin kerran neljässä viikossa.
Jos hemoglobiinin nousu on yli 2 g / dl (1,25 mmol / l) neljän viikon aikana, annosta on pienennettävä noin 25%riippuen nousun nopeudesta. On yli 12 g / dl (7,5 mmol) Jos hemoglobiini jatkaa nousuaan, annosta on pienennettävä noin 25%. Jos hemoglobiiniarvo jatkaa nousuaan annoksen pienentämisen jälkeen, anto on keskeytettävä väliaikaisesti, kunnes hemoglobiiniarvo laskee, jolloin hoito aloitetaan uudelleen noin 25% pienemmällä annoksella kuin edellinen.
Hemoglobiini on mitattava 1-2 viikon välein, kunnes se on vakiintunut, ja sen jälkeen hemoglobiini voidaan mitata pidemmillä aikaväleillä.
Anemian korjaamista Aranespilla kerran kuukaudessa ei ole tutkittu lapsipotilailla.
Huoltovaihe:
≥ 1 -vuotiaille lapsipotilaille Aranesp -hoitoa voidaan jatkaa ylläpitovaiheen aikana kerta -annoksena kerran viikossa tai kerran kahdessa viikossa. Potilaat ikääntyneet hemoglobiinitasot verrattuna vanhempiin potilaisiin. Dialyysipotilaiden, jotka siirtyvät kerran viikossa Aranesp -valmisteesta kahden viikon välein, tulee aluksi saada annos, joka vastaa kaksi kertaa edellistä viikoittaista annosta.
Kun dialyysipotilaat ovat 3–11-vuotiaita, kun hemoglobiinin tavoitepitoisuus on saavutettu kerran kahdessa viikossa, Aranesp voidaan antaa ihonalaisena injektiona kerran kuukaudessa alkaen kahdesti aiemmin annetusta annoksesta kerran kahdessa viikossa.
Kliiniset tiedot pediatrisista potilaista ovat osoittaneet, että potilaat, jotka saavat r-HuEPO: ta kaksi tai kolme kertaa viikossa, voidaan vaihtaa kerran viikossa Aranespiin ja potilaat, jotka saavat r-HuEPO: ta kerran viikossa, voivat siirtyä kerran viikossa annettavaan r-HuEPO-valmisteeseen. kaksi viikkoa. Aranesp-valmisteen aloitusviikkoannos lapsille (mcg / viikko) voidaan laskea jakamalla r-HuEPO: n viikoittainen kokonaisannos (IU / viikko) 240: llä. Kahden viikon välein aloitettava Aranesp-annos (mcg / kahden viikon välein) voidaan laskea jakamalla kahden viikon aikana annetun r-HuEPO: n kumulatiivinen kokonaisannos 240: llä. potilaalle optimaalinen terapeuttinen annos Kun r-HuEPO korvataan Aranespilla, hemoglobiini on tarkistettava 1-2 viikon välein ja samaa antotapaa on käytettävä.
Annosta on titrattava tarpeen mukaan hemoglobiinin tavoitepitoisuuden ylläpitämiseksi.
Jos annoksen muuttaminen on tarpeen hemoglobiinin pitämiseksi halutulla tasolla, on suositeltavaa muuttaa annosta noin 25%.
Jos hemoglobiinin nousu on yli 2 g / dl (1,25 mmol / l) neljän viikon aikana, annosta on pienennettävä noin 25%riippuen nousun nopeudesta. On yli 12 g / dl (7,5 mmol) Jos hemoglobiiniarvo kasvaa edelleen, annosta on pienennettävä noin 25%. annoksen pienentäminen, hemoglobiiniarvon nousu jatkuu, anto on keskeytettävä väliaikaisesti. kunnes hemoglobiiniarvo laskee, ja aloita sitten hoito uudelleen noin 25% pienemmällä annoksella kuin edellinen annos.
Potilaita, jotka aloittavat dialyysin Aranesp -hoidon aikana, tulee seurata tarkasti hemoglobiinipitoisuuksiensa asianmukaisen hallinnan varmistamiseksi.
Kun annosta tai annosteluaikataulua on muutettu, hemoglobiini on tarkistettava 1-2 viikon välein.Hoitovaiheen annosta ei saa muuttaa useammin kuin kerran kahdessa viikossa.
Kun antoreittiä muutetaan, on käytettävä samaa annosta ja hemoglobiini on tarkistettava 1-2 viikon välein annoksen säätämiseksi, jotta hemoglobiini pysyy halutulla tasolla.
Kemoterapian aiheuttaman oireisen anemian hoito syöpäpotilailla
Aranesp on annettava ihon alle aneemisille potilaille (esim. Hemoglobiinipitoisuus ≤ 10 g / dl (6,2 mmol / l), jotta hemoglobiiniarvo voidaan nostaa enintään 12 g / dl (7,5 mmol / l)). voi vaihdella iän, sukupuolen ja sairauden yleisen vakavuuden mukaan, joten on välttämätöntä, että lääkäri arvioi kunkin potilaan kliinisen kulun ja tilan.
Potilaan sisäisen vaihtelun vuoksi yksittäisellä hemoglobiiniarvolla voidaan toisinaan havaita haluttua hemoglobiinitasoa korkeammalla ja alhaisemmalla tasolla. Hemoglobiinin vaihtelua tulee hallita annosta säätämällä ottaen huomioon hemoglobiinin tavoitealue, joka on 10 g / dl (6,2 mmol / l) - 12 g / dl (7,5 mmol / l). Yli 12 g / dl (7,5 mmol / l); alla on ohjeet asianmukaisen annoksen muuttamisesta, jos hemoglobiiniarvot ovat yli 12 g / dl (7, 5 mmol / l).
Suositeltu aloitusannos on 500 mikrogrammaa (6,75 mikrogrammaa / kg) kerran kolmessa viikossa tai 2,25 mikrogrammaa / painokilo kerran viikossa. Jos potilaan kliininen vaste (väsymys, hemoglobiinivaste) on riittämätön yhdeksän viikon kuluttua, hoidon jatkaminen ei ehkä ole tehokasta.
Aranesp -hoito on lopetettava noin 4 viikon kuluttua solunsalpaajahoidon päättymisestä.
Kun yksittäisen potilaan hoitotavoite on saavutettu, annosta on pienennettävä 25-50%, jotta varmistetaan, että pienintä hyväksyttyä Aranesp-annosta käytetään pitämään hemoglobiini tasolla, joka hallitsee anemian oireet. mcg, 300 mcg ja 150 mcg tulee harkita.
Potilaita tulee seurata tarkasti ja pienentää annosta noin 25-50%, jos hemoglobiini ylittää 12 g / dl (7,5 mmol / l). Jos hemoglobiinipitoisuus ylittää 13 g / dl (8, 1 mmol / l), Aranesp-hoitoa tulee Hoito on aloitettava uudelleen annoksella, joka on noin 25% pienempi kuin edellinen annos, kun hemoglobiinitaso on laskenut 12: een tai alle g / dl (7,5 mmol / l).
Jos hemoglobiinin nousu on yli 2 g / dl (1,25 mmol / l) 4 viikon aikana, annosta on pienennettävä 25-50%.
Antotapa
Aranesp 10, 15, 20, 30, 40, 50, 60, 80, 100, 130, 150, 300, 500 mcg injektioneste, esitäytetty ruisku
Aranesp annetaan ihon alle tai suonensisäisesti annostelun mukaisesti.
Vaihda pistoskohdat ja pistä hitaasti pistoskohdan epämukavuuden minimoimiseksi. Aranesp toimitetaan käyttövalmiina esitäytetyissä ruiskuissa.
Aranesp 10, 15, 20, 30, 40, 50, 60, 80, 100, 130, 150, 300, 500 mcg injektioneste, esitäytetty kynä
Aranesp esitäytetyssä kynässä annetaan vain ihon alle.
Vaihda pistoskohdat epämukavuuden minimoimiseksi pistoskohdassa.
Aranesp toimitetaan käyttövalmiina esitäytetyssä kynässä.
Aranesp 25, 40, 60, 100, 200, 300 mcg injektioneste, liuos injektiopullossa
Aranesp annetaan ihon alle tai suonensisäisesti annostuksen mukaisesti.
Vaihda pistoskohdat ja pistä hitaasti pistoskohdan epämukavuuden minimoimiseksi.
Aranesp toimitetaan käyttövalmiina injektiopullossa.
Käyttö-, käsittely- ja hävittämisohjeet on annettu kohdassa 6.6.
04.3 Vasta -aiheet
Yliherkkyys vaikuttavalle aineelle tai kohdassa 6.1 mainituille apuaineille.
Hallitsematon verenpaine.
04.4 Varoitukset ja käyttöön liittyvät varotoimet
Yleistä
Erytropoieesiä stimuloivien aineiden (ESA) jäljitettävyyden parantamiseksi annetun ESA: n kauppanimi on merkittävä selvästi (tai ilmoitettava) potilastietueeseen.
Kaikkien potilaiden verenpainetta on seurattava erityisesti Aranesp -hoidon aloittamisen aikana.Jos verenpainetta on vaikea hallita asianmukaisilla toimenpiteillä, hemoglobiiniarvoa voidaan alentaa pienentämällä tai lopettamalla Aranesp -valmisteen käyttö (ks. Kohta 4.2). Vaikeaa hypertensiotapauksia, mukaan lukien hypertensiivinen kriisi, hypertensiivinen enkefalopatia ja kohtaus, on havaittu Aranesp -hoitoa saaneilla CRF -potilailla.
Tehokkaan erytropoieesin varmistamiseksi kaikkien potilaiden rautavarastot on tarkistettava ennen hoitoa ja sen aikana, ja lisärautahoitoa voidaan tarvita.
Jos Aranesp -hoitoon ei saada vastetta, sen pitäisi johtaa syy -tekijöiden tutkimiseen.Rautan, foolihapon tai B12 -vitamiinin puutteet heikentävät ESA: n tehoa ja ne on siksi korjattava. Samanaikaiset infektiot, tulehdus- tai traumaattiset jaksot, piilevä verenhukka, hemolyysi, vaikea alumiinimyrkytys, taustalla olevat hematologiset sairaudet tai luuydinfibroosi voivat heikentää erytropoieettista vastetta. Retikulosyyttien määrää on pidettävä osana arviointia. Jos tyypillisiä vasteen syitä on suljettu pois ja potilaalla on retikulosytopenia, luuydintutkimusta on harkittava.Jos luuydin on yhteensopiva PRCA -diagnoosin kanssa, on suoritettava vasta -ainetestit -erytropoietiini.
Erytropoietiinia neutraloivien vasta -aineiden aiheuttamaa puhdasta punasoluaplasiaa on raportoitu ESA -hoidon yhteydessä, mukaan lukien Aranesp. Tämä havainto on raportoitu pääasiassa potilailla, joilla on krooninen munuaisten vajaatoiminta (CRI) ihon alle. Näiden vasta-aineiden on osoitettu ristireagoivan kaikkien erytropoieettisten proteiinien kanssa, eikä potilaita, joiden epäillään tai todetaan olevan neutraloivia vasta-aineita erytropoietiinille, ei tule aloittaa Aranesp-hoidon aloittamisesta (ks. Kohta 4.8).
Paradoksaalisen hemoglobiinipitoisuuden alenemisen ja matalan retikulosyyttimäärään liittyvän vaikean anemian puhkeamisen pitäisi johtaa epoetiinihoidon välittömään keskeyttämiseen ja erytropoietiinivasta-ainetestin suorittamiseen. Tapauksia on raportoitu interferonia ja ribaviriinia saaneilla hepatiitti C -potilailla, kun epoetiinia käytettiin samanaikaisesti. Epoetiinia ei ole hyväksytty hepatiitti C: hen liittyvän anemian hoitoon.
Aktiivinen maksasairaus oli poissulkukriteeri kaikissa Aranesp -tutkimuksissa, joten tietoja potilaista, joilla on maksan vajaatoiminta, ei ole saatavilla. Koska maksan uskotaan olevan darbepoetiini alfan ja r-HuEPO: n tärkein eliminaatioreitti, Aranesp-valmistetta on käytettävä varoen maksasairautta sairastavilla potilailla.
Aranespia tulee käyttää varoen potilailla, joilla on sirppisoluanemia.
Aranespin väärinkäyttö terveillä henkilöillä voi aiheuttaa liiallisen hematokriitin nousun. Tämä voi liittyä sydän- ja verisuonikomplikaatioihin, jotka asettavat kohteen välittömään hengenvaaraan.
Esitäytetyn ruiskun tai esitäytetyn kynän neulansuojus sisältää kuivaa luonnonkumia (lateksin johdannainen), joka voi aiheuttaa allergisia reaktioita.
Aranespia tulee käyttää varoen epilepsiapotilailla. Kouristuksia on raportoitu Aranesp -hoitoa saavilla potilailla.
Tämä lääkevalmiste sisältää alle 1 mmol natriumia (23 mg) per annos, eli se on käytännössä natriumiton.
Potilaat, joilla on krooninen munuaisten vajaatoiminta
Potilailla, joilla on krooninen munuaisten vajaatoiminta, hemoglobiini on pidettävä tasolla, joka ei ylitä kohdassa 4.2 suositellun hemoglobiinin tavoitepitoisuuden ylärajaa. Kliinisissä tutkimuksissa on havaittu lisääntynyttä kuoleman, vakavien sydän- ja verisuonitapahtumien riskiä. mukaan lukien aivohalvaus ja verisuonitukosten tromboosi, jos annetaan ESA: ta, jonka tavoitteena on saavuttaa yli 12 g / dl (7,5 mmol / l) hemoglobiiniarvo.
Varovaisuutta on noudatettava Aranesp -annosten suurentamisessa potilailla, joilla on krooninen munuaisten vajaatoiminta, koska kumulatiiviset suuret epoetiiniannokset voivat liittyä kuolleisuuden, vakavien sydän- ja aivoverisuonitapahtumien riskin lisääntymiseen. vaihtoehtoisia syitä huonoon vasteeseen on otettava huomioon (ks. kohdat 4.2 ja 5.1).
Kontrolloidut kliiniset tutkimukset eivät ole osoittaneet epoetiinien antamisesta johtuvaa merkittävää hyötyä, kun hemoglobiinipitoisuus on noussut anemian oireiden hallintaan ja verensiirtojen välttämiseen tarvittavan tason yli.
Lisärautahoitoa suositellaan kaikille potilaille, joiden seerumin ferritiiniarvot ovat alle 100 mcg / l tai transferriinisaturaatio alle 20%.
Seerumin kaliumpitoisuuksia on seurattava säännöllisesti Aranesp -hoidon aikana. Joillakin Aranesp -hoitoa saaneilla potilailla on raportoitu kaliumpitoisuuden nousua, vaikka korrelaatiota hoitoon ei ole osoitettu. Jos kaliumpitoisuudet ovat kohonneet tai nousevat, Aranesp -hoidon lopettamista on harkittava, kunnes tämä taso korjaantuu.
Syöpäpotilaat
Vaikutus kasvaimen etenemiseen
Epoetiinit ovat kasvutekijöitä, jotka ensisijaisesti stimuloivat punasolujen tuotantoa. Erytropoietiinireseptoreita voidaan ekspressoida eri syöpäsolujen pinnalla, kuten kaikkien kasvutekijöiden kohdalla, on huolestuttavaa, että epoetiinit voivat stimuloida kasvainten kasvua. Useissa kontrolloiduissa kliinisissä tutkimuksissa epoetiinien ei ole osoitettu parantavan kokonaiseloonjäämistä tai vähentävän kasvaimen etenemisen riskiä potilailla, joilla on pahanlaatuisiin kasvaimiin liittyvä anemia.
Kontrolloiduissa kliinisissä tutkimuksissa, joissa annettiin Aranesp ja muita ESA -lääkkeitä, on osoitettu seuraavaa:
• Kasvaimen etenemiseen kuluvan ajan lyhentäminen potilailla, joilla on pitkälle edennyt pään ja kaulan syöpä ja jotka ovat saaneet sädehoitoa, kun ESA -lääkkeitä on annettu hemoglobiinin tavoitearvon saavuttamiseksi yli 14 g / dl (8,7 mmol / l); ESA: n käyttöä ei ole tarkoitettu tähän potilasryhmään.
• Kokonaiseloonjäämisen väheneminen ja taudin etenemiseen liittyvien kuolemien lisääntyminen 4 kuukauden kohdalla potilailla, joilla on metastaattinen rintasyöpä ja jotka ovat saaneet solunsalpaajahoitoa, kun niitä annetaan hemoglobiinitavoitteen 12-14 g / dl (7,5-8,7 mmol / l) saavuttamiseksi.
• Lisääntynyt kuolemanriski annostuksella, jonka tavoitteena on saavuttaa 12 g / dl (7,5 mmol / l) potilailla, joilla on aktiivisia pahanlaatuisia kasvaimia ja joita ei hoideta kemoterapialla tai sädehoidolla. ESA: n käyttöä ei ole indikoitu tässä potilasryhmässä.
Edellä esitetyn perusteella joissakin kliinisissä olosuhteissa verensiirron tulisi olla ensisijainen hoito syövän sairastavien anemian hoidossa. Päätös yhdistelmä-erytropoietiinien antamisesta tulee perustaa hyöty-riskisuhteen arviointiin, johon yksittäinen potilas osallistuu Tässä arvioinnissa on otettava huomioon syövän tyyppi ja sen vaihe, anemian aste, elinajanodote, ympäristö, jossa potilasta hoidetaan, ja potilaan mieltymykset (ks. kohta 5.1).
Jos potilailla, joilla on kiinteitä kasvaimia tai lymfoproliferatiivisia kasvaimia, hemoglobiiniarvo ylittää 12 g / dl (7,5 mmol / l), kohdassa 4.2 kuvattua annoksen säätöä on noudatettava tarkasti tromboembolisten tapahtumien riskin minimoimiseksi. Verihiutaleiden määrä ja hemoglobiinitaso on tarkistettava säännöllisin väliajoin.
04.5 Yhteisvaikutukset muiden lääkevalmisteiden kanssa sekä muut yhteisvaikutukset
Tähän mennessä saadut kliiniset tulokset eivät viittaa darbepoetiini alfan yhteisvaikutukseen muiden aineiden kanssa. On kuitenkin mahdollista, että "vuorovaikutus aineiden kanssa, jotka sitoutuvat merkittävästi punasoluihin, kuten syklosporiini ja takrolimuusi. hemoglobiinin nousun mukaan.
04.6 Raskaus ja imetys
Raskaus
Ei ole olemassa riittäviä ja hyvin kontrolloituja tutkimuksia Aranesp-valmisteen käytöstä raskaana oleville naisille.
Eläinkokeet eivät osoittaneet suoria haitallisia vaikutuksia raskauteen, alkion / sikiön kehitykseen, synnytykseen tai synnytyksen jälkeiseen kehitykseen. Hedelmällisyyden heikkenemistä ei havaittu.
Varovaisuutta on noudatettava määrättäessä Aranesp -valmistetta raskaana oleville naisille.
Naisia, jotka tulevat raskaaksi Aranesp -hoidon aikana, kannustetaan ilmoittautumaan Amgenin raskaudenvalvontaohjelmaan. Yhteystiedot ovat pakkausselosteen kohdassa 6.
Ruokinta-aika
Ei tiedetä, erittyykö Aranesp äidinmaitoon. Vauvojen riskiä ei voida sulkea pois. On päätettävä, lopetetaanko imetys vai lopetetaanko Aranesp-hoito tai pidättäydytäänkö siitä ottaen huomioon imetyksen hyödyt lapselle ja hoidon hyödyt naiselle.
04.7 Vaikutus ajokykyyn ja koneiden käyttökykyyn
Aranespilla ei ole haitallista vaikutusta ajokykyyn tai koneiden käyttökykyyn.
04.8 Haittavaikutukset
Yhteenveto turvallisuusprofiilista
Aranesp -valmisteen käyttöön liittyviä haittavaikutuksia ovat kohonnut verenpaine, aivohalvaus, tromboemboliset tapahtumat, kouristukset, allergiset reaktiot, ihottuma / punoitus ja puhdas punasoluaplasia (ks. Kohta 4.4).
Pistoskohdan kivun katsottiin johtuvan hoidosta tutkimuksissa, joissa Aranesp annettiin ihonalaisena injektiona. Pistoskohdan epämukavuus oli yleensä lievää ja ohimenevää ja esiintyi pääasiassa ensimmäisen injektion jälkeen.
Taulukko haittavaikutuksista
Haittavaikutusten ilmaantuvuus on esitetty alla elinjärjestelmäluokituksen ja esiintymistiheysluokan mukaan.Esiintymistiheydet on määritelty seuraavasti: Hyvin yleinen (≥ 1/10); yleinen (≥ 1/100,
Tiedot esitetään erikseen kroonista munuaisten vajaatoimintaa sairastavista potilaista ja syöpäpotilaista, jotta heijastavat eri haittavaikutusprofiileja näissä populaatioissa.
Potilaat, joilla on krooninen munuaisten vajaatoiminta
Kontrolloiduista kliinisistä tutkimuksista saadut tiedot sisälsivät 1357 potilasta, 766 Aranesp-hoitoa ja 591 r-HuEPO-hoitoa saavaa potilasta. Aranesp -ryhmässä 83% potilaista sai dialyysihoitoa ja 17% ei ollut dialyysissä. Aivohalvaus todettiin haittavaikutukseksi kliinisessä lisätutkimuksessa (TREAT, ks. Kohta 5.1).
Haittavaikutusten ilmaantuvuus kontrolloiduissa kliinisissä tutkimuksissa ja markkinoille tulon jälkeen on seuraava:
* katso kohta "Valikoitujen haittavaikutusten kuvaus"
Syöpäpotilaat
Haittavaikutukset määritettiin tietojen perusteella, jotka oli kerätty seitsemästä satunnaistetusta, kaksoissokkoutetusta, lumekontrolloidusta tutkimuksesta, joihin osallistui yhteensä 2112 potilasta (1200 Aranespia, 912 lumelääkettä). Kliinisiin tutkimuksiin osallistui potilaita, joilla oli kiinteitä kasvaimia (esim. Keuhko-, rinta-, paksusuolen- ja munasarjasyöpä) ja pahanlaatuisia imusolmukkeita (esim. Lymfooma, multippeli myelooma).
Haittavaikutusten ilmaantuvuus kontrolloiduissa kliinisissä tutkimuksissa ja markkinoille tulon jälkeen on seuraava:
* katso kohta "Valikoitujen haittavaikutusten kuvaus"
Valittujen haittavaikutusten kuvaus
Potilaat, joilla on krooninen munuaisten vajaatoiminta
TREAT -hoidossa aivohalvaus raportoitiin yleiseksi CRF -potilailla (ks. Kohta 5.1).
Yksittäistapauksissa puhdasta punasolujen aplasiaa (PRCA), jossa on neutraloivia vasta -aineita erytropoietiinille, ja jotka liittyvät Aranesp -hoitoon, pääasiassa ihonalaisesti hoidetuilla CRF -potilailla. Jos PRCA todetaan, Aranesp -hoito on lopetettava eikä potilaita saa hoitaa toisella yhdistelmä -erytropoieettisella proteiinilla (ks. Kohta 4.4).
Kliinisten tutkimustietojen perusteella kaikkien yliherkkyysreaktioiden esiintymistiheys määriteltiin erittäin yleiseksi CRF -potilailla. Darbepoetiini alfan käyttöön on raportoitu vakavia yliherkkyysreaktioita, mukaan lukien anafylaktinen reaktio, angioedeema, allerginen bronkospasmi, ihottuma ja nokkosihottuma.
Kouristuskohtauksia on raportoitu darbepoetiini alfaa saavilla potilailla (ks. Kohta 4.4).
Kliinisten tutkimustietojen perusteella esiintymistiheys määritellään harvinaiseksi CRF -potilailla.
Syöpäpotilaat
Markkinoille tulon jälkeen verenpainetta on havaittu syöpäpotilailla (ks. Kohta 4.4) Kliinisistä tutkimuksista saatujen tietojen perusteella esiintymistiheys määritellään yleiseksi syöpäpotilailla ja yleiseksi myös lumelääkettä saaneilla ryhmillä.
Markkinoille tulon jälkeisen käytön aikana syöpäpotilailla on havaittu yliherkkyysreaktioita. Kliinisistä tutkimuksista saatujen tietojen perusteella esiintymistiheys määritellään hyvin yleiseksi syöpäpotilailla. Yliherkkyysreaktiot olivat hyvin yleisiä. Myös lumeryhmissä. yliherkkyysreaktiot, jotka liittyvät darbepoetiini alfan käyttöön, mukaan lukien anafylaktinen reaktio, angioedeema, allerginen bronkospasmi, ihottuma ja nokkosihottuma.
Markkinoille tulon jälkeen on raportoitu kouristuskohtauksia darbepoetiini alfaa saaneilla potilailla (ks. Kohta 4.4) Kliinisten tutkimusten tietojen perusteella esiintymistiheys on harvinainen syöpäpotilailla. Kouristukset ovat yleisiä lumelääkeryhmissä.
Pediatriset potilaat, joilla on krooninen munuaisten vajaatoiminta
Kaikissa IRC: n lapsilla tehdyissä kliinisissä tutkimuksissa lapsipotilailla ei havaittu muita haittavaikutuksia kuin aiemmin raportoitiin aikuispotilailla (ks. Kohta 5.1).
Epäillyistä haittavaikutuksista ilmoittaminen
Ilmoittaminen epäillyistä haittavaikutuksista, jotka ilmenevät lääkkeen hyväksynnän jälkeen, on tärkeää, koska se mahdollistaa lääkkeen hyöty -haitta -tasapainon jatkuvan seurannan. Terveydenhuollon ammattilaisia pyydetään ilmoittamaan kaikista epäillyistä haittavaikutuksista kansalliseen raportointijärjestelmään. - Verkkosivusto: http // www.agenziafarmaco.gov.it / it / managerit).
04.9 Yliannostus
Aranesp -enimmäismäärää, joka voidaan turvallisesti antaa yksittäisinä tai useina annoksina, ei ole määritetty. Aranesp -hoito voi johtaa polysytemiaan, jos hemoglobiinia ei seurata huolellisesti eikä annosta säädetä asianmukaisesti .. Vaikeaa verenpainetautia on havaittu Aranesp -yliannostuksen jälkeen (ks. Kohta 4.4).
Polysytemian ilmetessä Aranesp -hoito on keskeytettävä väliaikaisesti (ks. Kohta 4.2). Jos se on kliinisesti osoitettu, flebotomia voidaan suorittaa.
05.0 FARMAKOLOGISET OMINAISUUDET
05.1 Farmakodynaamiset ominaisuudet
Farmakoterapeuttinen ryhmä: Anemian vastaiset valmisteet, muut anemian vastaiset valmisteet. ATC -koodi: B03XA02.
Toimintamekanismi
Ihmisen erytropoietiini, endogeeninen glykoproteiinihormoni, on erytropoieesin tärkein säätelijä, koska se on spesifisesti vuorovaikutuksessa erytropoietiinireseptorin kanssa luuytimen punasolujen esisoluissa. Erytropoietiinin tuotanto tapahtuu pääasiassa ja sitä säädellään munuaisissa vastauksena muutoksiin kudosten hapettumisessa Endogeeninen erytropoietiinin tuotanto vähenee kroonista munuaisten vajaatoimintaa sairastavilla potilailla ja erytropoietiinin puutos on näiden potilaiden anemian ensisijainen syy. Kemoterapiaa saavilla syöpäpotilailla anemian etiologia on monitahoinen. Näillä potilailla erytropoietiinin puutos ja erytroidisten esisolujen heikentynyt vaste endogeeniselle erytropoietiinille ovat molemmat anemiaan vaikuttavia tekijöitä.
Farmakodynaamiset vaikutukset
Darbepoetiini alfa stimuloi erytropoieesia samalla mekanismilla kuin endogeeninen hormoni. Darbepoetiini alfassa on viisi hiilihydraattiketjua, jotka on liitetty N-päähän, kun taas endogeenisellä hormonilla ja ihmisen yhdistelmä-erytropoietiinilla (r-HuEPO) on kolme. Muita hiilihydraattitähteitä ei voida erottaa molekyylitasolla niistä, joita esiintyy endogeenisessä hormonissa.Korkeamman hiilihydraattipitoisuuden vuoksi darbepoetiini alfalla on pidempi terminaalinen puoliintumisaika kuin r-HuEPO: lla ja siten suurempi aktiivisuus. in vivo. Näistä molekyylimuunnoksista huolimatta darbepoetiini alfa säilyttää erittäin korkean spesifisyyden erytropoietiinireseptorille.
Kliininen teho ja turvallisuus
Potilaat, joilla on krooninen munuaisten vajaatoiminta
Kahdessa kliinisessä tutkimuksessa CRF -potilailla oli suurempi kuoleman ja vakavien sydän- ja verisuonitapahtumien riski, kun ESA -lääkkeitä annettiin korkeampien hemoglobiinitasojen saavuttamiseksi kuin alemmat hemoglobiinitasot (13,5 g / dl (8, 4 mmol / l) verrattuna 11,3 g / dl (7,1) 14 g / dl (8,7 mmol / l) verrattuna 10 g / dl (6,2 mmol / l)).
Satunnaistetussa, kaksoissokkoutetussa korjaustutkimuksessa (n = 358), jossa verrattiin kerran joka toinen viikko ja kerran kuukaudessa annosteluohjelmia CRF-potilailla, jotka eivät olleet dialyysissä, darbepoetiini alfa -annos kerran päivässä kuukaudessa paransi anemiaa vähintään Keskimääräinen aika (kvartiili 1, kvartiili 3) hemoglobiinikorjauksen saavuttamiseen (≥ 10,0 g / dl ja nousu ≥ 1,0 g / dl lähtötasosta) oli 5 viikkoa molemmilla kerran kahdessa viikossa ( 3,7 viikkoa) ja kerran kuukaudessa (3,9 viikkoa). Arviointijakson aikana (viikot 29--33) keskimääräinen viikoittainen ekvivalenttiannos (95%: n luottamusväli) oli 0,20 (0,17 - 0,24) mcg / kg kahden viikon välein ja 0,27 (0,23 - 0,32) mcg / kg käsivarsi kerran kuukaudessa.
Satunnaistetussa, kaksoissokkoutetussa, lumekontrolloidussa tutkimuksessa (TREAT), johon osallistui 4038 ei-dialyysipitoista CRF-potilasta, joilla oli tyypin 2 diabetes ja hemoglobiinipitoisuus ≤ 11 g / dl, potilaat saivat joko darbepoetiini alfa -hoitoa hemoglobiinitavoitteen saavuttamiseksi 13 g / dl tai lumelääke (palautushoidolla darbepoetiini alfalla hemoglobiinipitoisuuden ollessa alle 9 g / dl). Tutkimus ei saavuttanut ensisijaista tavoitetta osoittaa kuolleisuuden tai sydän- ja verisuonisairauksien riskin pienenemistä (darbepoetiini alfa verrattuna lumelääkkeeseen; HR 1,05, 95%: n luottamusväli (0,94--1,17)), o Kaikista syistä johtuva kuolleisuus o Loppuvaihe munuaissairaus (ESRD) (darbepoetiini alfa verrattuna lumelääkkeeseen; HR 1,06, 95%: n luottamusväli (0,95-1,19)). "Yhdistetyn päätepisteen yksittäisten komponenttien analyysi osoitti seuraavan HR: n (95%: n luottamusväli): kuolema 1,05 (0,92-1,21) ), kongestiivinen sydämen vajaatoiminta (CHF) 0,89 (0,74-1,08), sydäninfarkti (MI) 0,96 (0,75-1,23), aivohalvaus 1,92 (1,38-2,68), sydänlihasiskemian sairaalahoito 0,84 (0,55-1,27), ESRD 1,02 (0,87) -1,18).
Yhdistetyt post-hoc -analyysit kliinisistä ESA-tutkimuksista tehtiin potilailla, joilla oli krooninen munuaisten vajaatoiminta (dialyysihoidossa, ei dialyysissä, diabeetikko, ei-diabeetikko). Suhteellisen kuolleisuuden, sydän- ja verisuonitautien ja aivoverisuonitapahtumien riskin arvioitiin lisääntyvän, kun yhdistettynä suurempiin kumulatiivisiin ESA -annoksiin riippumatta diabeteksesta tai dialyysitilasta (ks. Kohdat 4.2 ja 4.4).
Pediatriset potilaat
Satunnaistetussa kliinisessä tutkimuksessa 114 2–18 -vuotiasta lapsipotilasta, joilla oli krooninen munuaissairaus, dialyysi tai ei -dialyysi, jotka olivat aneemisia (hemoglobiini
Kliinisessä tutkimuksessa, johon osallistui 124 kroonista munuaissairautta sairastavaa lapsipotilasta, jotka saivat dialyysi- tai ei -dialyysihoitoa 1–18 -vuotiaille potilaille, potilaat, jotka pysyivät stabiilina epoetiini alfalla, satunnaistettiin saamaan darbepoetiini alfaa kerran viikossa (ihon alle) tai suonensisäisesti käyttäen annoksen muuttamisprosenttia 238: 1, tai jatka epoetiini alfa -hoitoa samalla annoksella, aikataululla ja antotavalla. Ensisijainen tehon päätetapahtuma [hemoglobiinitasojen muutos lähtötilanteen ja arviointijakson välillä (viikot 21-28)] oli samanlainen molemmissa ryhmissä.RHuEPO: n ja darbepoetiini alfan keskimääräiset hemoglobiinitasot lähtötilanteessa olivat 11,1 (SD 0,7) g / dL ja 11,3 (SD 0,6) g / dL. rHuEPO: n ja darbepoetiini alfan keskimääräiset hemoglobiinitasot viikolla 28 olivat 11,1 (SD 1,4) g / dl ja 11,1 (SD 1,1) g / dl.
Eurooppalaisessa havaintorekisteritutkimuksessa, johon osallistui 319 kroonista munuaissairautta sairastavaa pediatrista potilasta (13 (4,1%) ikäistä potilasta)
Näissä tutkimuksissa ei havaittu merkittäviä eroja pediatristen potilaiden turvallisuusprofiilin ja aiemmin aikuispotilaiden raportoitujen turvallisuusprofiilien välillä (ks. Kohta 4.8).
Potilaat, joilla on syöpä ja jotka saavat kemoterapiaa
Prospektiivisessa, satunnaistetussa, kaksoissokkoutetussa, lumekontrolloidussa tutkimuksessa 314 keuhkosyöpäpotilaasta, jotka saivat platinapohjaista kemoterapiaa, verensiirtojen tarve väheni merkittävästi (p
Kliiniset tutkimukset ovat osoittaneet, että darbepoetiini alfan teho on samanlainen, kun sitä annetaan kerta -annoksena kerran 3 viikossa, kerran kahdessa viikossa tai viikoittain ilman, että kokonaisannosta on lisättävä.
Aranesp-hoidon siedettävyyttä ja tehokkuutta 3 viikon välein verensiirtojen tarpeen vähentämisessä solunsalpaajahoitoa saavilla potilailla arvioitiin satunnaistetussa, kaksoissokkoutetussa, kansainvälisessä tutkimuksessa. Tämä tutkimus tehtiin 705 potilaalla. Potilaat satunnaistettiin saamaan Aranesp -valmistetta annoksina 500 mcg kerran 3 viikossa tai annoksina 2,25 mcg / kg kerran viikossa. Molemmissa ryhmissä annosta pienennettiin 40% edellisestä annoksesta (esim. ensimmäinen annoksen pienentäminen, tämä pienennettiin 300 mikrogrammaan kerran kolmen viikon välein ja 1,35 mikrogrammaan / kg kerran viikossa), jos hemoglobiini nousi yli 1 g / dl 14 päivässä . Kerran kolmen viikon välein 72% potilaista tarvitsi annoksen pienentämistä. Kerran viikossa ryhmässä 75% potilaista tarvitsi annoksen pienentämistä. Tämä tutkimus osoittaa, että 500 mcg: n annostus 3 viikon välein on verrattavissa kerran viikossa annettavaan annokseen niiden potilaiden ilmaantuvuuden suhteen, jotka tarvitsevat vähintään yhden verensiirron viikon 5 ja hoidon päättymisen välillä.
Prospektiivisessa, satunnaistetussa, kaksoissokkoutetussa, lumekontrolloidussa tutkimuksessa, johon osallistui 344 aneemista potilasta, joilla oli lymfoproliferatiivisia kasvaimia ja jotka saivat solunsalpaajahoitoa, verensiirtojen tarve väheni merkittävästi ja hemoglobiinivaste parani (p
Erytropoietiini on kasvutekijä, joka stimuloi ensisijaisesti punasolujen tuotantoa, ja erytropoietiinireseptoreita voidaan ekspressoida eri syöpäsolujen pinnalla.
Selviytymistä ja kasvaimen etenemistä arvioitiin viidessä suuressa kontrolloidussa kliinisessä tutkimuksessa, joihin osallistui yhteensä 2833 potilasta; joista neljä oli lumekontrolloituja ja kaksoissokkotutkimuksia ja yksi avoin. Kaksi näistä tutkimuksista otti mukaan potilaita, joita hoidettiin kemoterapialla. Hemoglobiinin tavoitepitoisuus oli yli 13 g / dl kahdessa tutkimuksessa; lopuissa kolmessa tutkimuksessa se oli 12-14 g / dl. Avoimessa tutkimuksessa kokonaiseloonjäämisessä ei havaittu eroja yhdistelmä-DNA-yhdistelmän ihmisen erytropoietiinihoitoa saaneiden potilaiden ja kontrollipotilaiden välillä. Neljässä lumekontrolloidussa tutkimuksessa kokonaiseloonjäämisen riskisuhteet vaihtelivat välillä 1,25-2,47 kontrolliryhmän hyväksi. Nämä tutkimukset osoittivat kontrolleihin verrattuna jatkuvan ja selittämättömän tilastollisesti merkitsevän kuolleisuuden lisääntymisen potilailla, joilla oli anemia, joka liittyi erityyppisiin yleisiin kasvaimiin ja jotka saivat rekombinanttia ihmisen erytropoietiinia. Näiden tutkimusten kokonaiseloonjäämistulosta ei voitu selittää tyydyttävästi tromboosin ja siihen liittyvien komplikaatioiden ilmaantuvuuden erojen perusteella yhdistelmä -DNA -yhdistelmä -ihmisen erytropoietiinilla hoidettujen potilaiden ja kontrolliryhmän potilaiden välillä.
Lisäksi suoritettiin systemaattinen analyysi 57 kliinisestä tutkimuksesta, joihin osallistui yli 9 000 syöpäpotilasta.Kokonaiseloonjäämistietojen meta-analyysi osoitti pistemäärän riskiarvosta 1,08 kontrollien hyväksi (95%: n luottamusväli: 0,99--1,18; 42 tutkimukset ja 8167 potilasta).
Tromboembolisten tapahtumien suhteellinen riski (RR 1,67, 95%: n luottamusväli: 1,35--2,06, 35 tutkimusta ja 6769 potilasta) suureni potilailla, joita hoidettiin yhdistelmä-DNA-tekniikalla tehdyllä ihmisen erytropoietiinilla. Siksi on olemassa johdonmukaisia todisteita siitä, että yhdistelmä -DNA -ihmisen erytropoietiinilla hoidetuista syöpäpotilaista voi olla merkittävää haittaa. On epäselvää, missä määrin näitä tuloksia voidaan soveltaa ihmisen yhdistelmä -erytropoietiinihoitoon syöpäpotilaille, jotka saavat solunsalpaajahoitoa hemoglobiinipitoisuuden saavuttamiseksi alle 13 g / dl, koska harvat potilaat, joilla oli nämä ominaisuudet, sisällytettiin analysoituihin tietoihin.
Yksittäisten potilastietojen analyysi suoritettiin myös yli 13 900 syöpäpotilaalla (kemo-, radio-, kemoradio- tai ei -hoito), jotka osallistuivat 53 kontrolloituun kliiniseen tutkimukseen, joissa käytettiin eri epoetiinia. Kokonaiseloonjäämistietojen meta-analyysi tuotti piste-estimaatin riskisuhteesta 1,06 kontrollien hyväksi (95%: n luottamusväli: 1,00--1,12; 53 tutkimusta ja 13933 potilasta) ja riskisuhde 1,04 syöpää sairastavilla potilailla ( 95%: n luottamusväli: 0,97--1,11; 38 tutkimusta ja 10 441 potilasta.) Meta-analyysi osoittaa myös johdonmukaisesti, että tromboembolisten tapahtumien suhteellinen riski on merkittävästi lisääntynyt syöpäpotilailla, jotka saavat yhdistelmä-DNA-tekniikalla saatua ihmisen erytropoietiinia (ks. Kohta 4.4).
05.2 Farmakokineettiset ominaisuudet
Kun otetaan huomioon korkeampi hiilihydraattipitoisuus, darbepoetiini alfan verenkierrossa oleva taso pysyy pienemmän erytropoieesia stimuloivan pitoisuuden yläpuolella pidempään kuin r-HuEPO: n molaarinen ekvivalenttiannos, jolloin darbepoetiini alfa voidaan antaa harvemmin saman biologisen vasteen saavuttamiseksi.
Potilaat, joilla on krooninen munuaisten vajaatoiminta
Darbepoetiini alfan farmakokinetiikkaa on tutkittu kliinisesti kroonista munuaisten vajaatoimintaa sairastavilla potilailla laskimonsisäisen ja ihonalaisen annon jälkeen. Darbepoetiini alfan terminaalinen puoliintumisaika on 21 tuntia (SD 7,5) laskimonsisäisesti annettaessa. Plasman tilavuus (50 ml / kg). Biologinen hyötyosuus on 37% ihon alle. Kun darbepoetiini alfa on annettu kuukausittain ihon alle, annoksilla 0,6-2,1 μg / kg, terminaalinen puoliintumisaika oli 73 tuntia (SD 24). Ihon alle tapahtuvan imeytymisen kinetiikka johtaa darbepoetiini alfan "terminaaliseen puoliintumisaikaan pidempään, kun sitä annetaan ihon alle kuin laskimonsisäisesti. Kliinisissä tutkimuksissa kumulaatiota havaittiin minimaalisesti molemmilla antoreiteillä. Prekliiniset tutkimukset ovat osoittaneet, että" munuaispuhdistuma on minimaalinen (enintään 2% kokonaispuhdistumasta), eikä se vaikuta seerumin puoliintumisaikaan.
Tiedot 809 Aranespilla hoidetusta potilaasta eurooppalaisissa kliinisissä tutkimuksissa analysoitiin hemoglobiinin ylläpitämiseen tarvittavan annoksen määrittämiseksi; laskimonsisäisesti tai ihonalaisesti annetun keskimääräisen viikoittaisen annoksen välillä ei havaittu eroa.
Darbepoetiini alfan farmakokinetiikkaa pediatrisilla potilailla (2-16-vuotiaat) sekä dialyysi- että ei-dialyysipotilailla arvioitiin enintään 2 viikon (336 tunnin) näytteenottoajoista yhden tai kahden ihonalaisen tai laskimonsisäisen annoksen jälkeen. Käyttämällä samaa näytteenottoaikaa havaitut farmakokineettiset tiedot ja populaatiofarmakokineettinen malli osoittivat, että darbepoetiini alfan farmakokineettinen profiili oli samanlainen lapsilla ja aikuisilla CRF -potilailla.
Vaiheen I farmakokineettisessä tutkimuksessa laskimonsisäisen annon jälkeen havaittiin noin 25%: n ero lapsipotilaiden ja aikuispotilaiden välillä käyrän alla olevalla alueella 0: sta äärettömään (AUC [0-∞]); tämä ero oli kuitenkin alle kaksi kertaa AUC [0-∞] -alue havaittu lapsipotilailla. AUC [0-∞] ihonalaisen annon jälkeen oli samanlainen aikuisilla ja lapsilla, joilla oli CRF. Puoliintumisaika oli samanlainen myös aikuispotilailla ja lapsilla, joilla oli CRF laskimoon ja ihon alle.
Potilaat, joilla on syöpä ja jotka saavat kemoterapiaa
Kun aikuisille syöpäpotilaille annettiin ihon alle 2,25 μg / kg, darbepoetiini alfan keskimääräinen huippupitoisuus 10,6 ng / ml (SD 5,9) saavutettiin keskimäärin 91 tunnin kuluttua (SD 19,7). Nämä parametrit olivat yhdenmukaisia annoksesta riippuvan lineaarisen farmakokinetiikan kanssa laajalla annosalueella (0,5-8 mcg / kg viikoittain ja 3-9 mcg / kg kahden viikon välein). Farmakokineettiset parametrit eivät muuttuneet toistuvan annostelun jälkeen 12 viikon ajan (viikoittain tai 2 viikon välein). Odotettavissa oli kohtalainen nousu (
05.3 Prekliiniset tiedot turvallisuudesta
Kaikissa rotilla ja koirilla tehdyissä tutkimuksissa darbepoetiini alfa johti hemoglobiinin, hematokriitin, punasolujen ja retikulosyyttien nousuun, mikä vastasi odotettuja farmakologisia vaikutuksia. Hyvin suurina annoksina esiintyneiden haittatapahtumien katsottiin johtuvan liiallisesta farmakologisesta vaikutuksesta (kudosten perfuusion heikkeneminen "lisääntyneen veren viskositeetin vuoksi"). Näitä tapahtumia ovat myelofibroosi, pernan hypertrofia ja myös EKG-QRS-kompleksin venyminen "EKG-koirilla" , mutta rytmihäiriöitä tai vaikutusta QT -aikaan ei havaittu.
Darbepoetiini alfa ei osoittanut genotoksista potentiaalia eikä sillä ollut vaikutusta proliferaatioon in vitro tai in vivo ei-hematologisista soluista. Kroonisen toksisuuden tutkimuksissa odottamattomia onkogeenisiä tai mitogeenisiä vasteita ei havaittu minkään tyyppisissä kudoksissa. Darbepoetiini alfan karsinogeenisuutta ei ole arvioitu pitkäaikaisissa eläinkokeissa.
Rotilla ja kaneilla tehdyissä tutkimuksissa ei havaittu kliinisesti merkittäviä todisteita haittavaikutuksista raskauteen, alkion / sikiön kehitykseen, synnytykseen tai synnytyksen jälkeiseen kehitykseen.Transplacental -kulku oli minimaalinen. Hedelmällisyyden heikkenemistä ei havaittu.
06.0 FARMASEUTTISET TIEDOT
06.1 Apuaineet
Yksiemäksinen natriumfosfaatti
Kaksiemäksinen natriumfosfaatti
Natriumkloridia
Polysorbaatti 80
Injektionesteisiin käytettävä vesi
06.2 Yhteensopimattomuus
Yhteensopivuustutkimusten puuttuessa tätä lääkevalmistetta ei saa sekoittaa muiden lääkevalmisteiden kanssa tai antaa infuusiona muiden lääkevalmisteiden kanssa.
06.3 Voimassaoloaika
3 vuotta.
06.4 Säilytys
Säilytä jääkaapissa (2 ° C - 8 ° C).
Ei saa jäätyä.
Säilytä pakkaus ulkopakkauksessa suojataksesi lääkettä valolta.
Avohoidossa Aranesp voidaan säilyttää huoneenlämmössä (enintään 25 ° C) vain kerran ja enintään seitsemän päivän ajan. Kun se on otettu pois jääkaapista ja se on saavuttanut huoneenlämpötilan (jopa 25 ° C), se on käytettävä 7 päivän kuluessa tai hävitettävä.
06.5 Välipakkauksen luonne ja pakkauksen sisältö
Aranesp 10 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
0,4 ml injektionestettä (25 mcg / ml darbepoetiini alfa) tyypin 1 lasisessa esitäytetyssä ruiskussa, jossa on ruostumaton teräs 27 neula. Pakkauskoko 1 tai 4 esitäytettyä ruiskua.
Aranesp 15 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
0,375 ml injektioneste, liuos (40 mcg / ml darbepoetiini alfa), tyypin 1 lasisessa esitäytetyssä ruiskussa, jossa on ruostumaton teräs 27 neula. Pakkauskoko 1 tai 4 esitäytettyä ruiskua.
Aranesp 20 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
0,5 ml injektioneste, liuos (40 mcg / ml darbepoetiini alfa) tyypin 1 lasisessa esitäytetyssä ruiskussa, jossa on ruostumaton teräs 27 neula. Pakkauskoko 1 tai 4 esitäytettyä ruiskua.
Aranesp 30 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
0,3 ml injektionestettä (100 mcg / ml darbepoetiini alfa) tyypin 1 lasisessa esitäytetyssä ruiskussa, jossa on ruostumaton teräs 27 neula. Pakkauskoko 1 tai 4 esitäytettyä ruiskua.
Aranesp 40 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
0,4 ml injektionestettä (100 mcg / ml darbepoetiini alfa) tyypin 1 lasisessa esitäytetyssä ruiskussa, jossa on ruostumaton teräs 27 neula. Pakkauskoko 1 tai 4 esitäytettyä ruiskua.
Aranesp 50 mcg injektioneste, liuos esitäytetyssä ruiskussa
0,5 ml injektioneste, liuos (100 mcg / ml darbepoetiini alfa) tyypin 1 lasisessa esitäytetyssä ruiskussa, jossa on ruostumaton teräs 27 neula. Pakkauskoko 1 tai 4 esitäytettyä ruiskua.
Aranesp 60 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
0,3 ml injektionestettä (200 μg / ml darbepoetiini alfa) esitäytetyssä tyypin 1 lasiruiskussa, jossa on ruostumattomasta teräksestä valmistettu 27 neula. Pakkauskoko 1 tai 4 esitäytettyä ruiskua.
Aranesp 80 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
0,4 ml injektionestettä (200 μg / ml darbepoetiini alfa) tyypin 1 lasisessa esitäytetyssä ruiskussa, jossa on ruostumaton teräs 27 neula. Pakkauskoko 1 tai 4 esitäytettyä ruiskua.
Aranesp 100 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
0,5 ml injektioneste, liuos (200 μg / ml darbepoetiini alfa) tyypin 1 lasisessa esitäytetyssä ruiskussa, jossa on ruostumaton teräs 27 neula. Pakkauskoko 1 tai 4 esitäytettyä ruiskua.
Aranesp 130 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
0,65 ml injektioneste, liuos (200 mcg / ml darbepoetiini alfa) tyypin 1 lasisessa esitäytetyssä ruiskussa, jossa on ruostumaton teräs 27 neula. Pakkauskoko 1 tai 4 esitäytettyä ruiskua.
Aranesp 150 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
0,3 ml injektionestettä (500 mcg / ml darbepoetiini alfa) tyypin 1 lasisessa esitäytetyssä ruiskussa, jossa on ruostumaton teräs 27 neula. Pakkauskoko 1 tai 4 esitäytettyä ruiskua.
Aranesp 300 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
0,6 ml injektionestettä (500 mcg / ml darbepoetiini alfa) tyypin 1 lasisessa esitäytetyssä ruiskussa, jossa on ruostumaton teräs 27 neula. Pakkauskoko 1 tai 4 esitäytettyä ruiskua.
Aranesp 500 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
1 ml injektionestettä (500 mcg / ml darbepoetiini alfa) tyypin 1 lasisessa esitäytetyssä ruiskussa, jossa on ruostumaton teräs 27 neula. Pakkauskoko 1 tai 4 esitäytettyä ruiskua.
Ruiskut voidaan pakata läpipainopakkauksiin (1 ja 4 ruiskun pakkaukset), automaattisen neulansuojuksen kanssa tai ilman, tai ilman rakkuloita (vain 1 ruiskun pakkaukset).
Esitäytetyn ruiskun neulansuojus sisältää kuivaa luonnonkumia (lateksin johdannainen) (ks. Kohta 4.4).
Aranesp 10 mikrogrammaa injektioneste, liuos, esitäytetty kynä
0,4 ml injektionestettä (25 mcg / ml darbepoetiini alfa) esitäytetyssä kynässä, jossa on tyypin 1 lasiruisku ja ruostumattomasta teräksestä valmistettu 27 neula. Pakkaus sisältää 1 tai 4 esitäytettyä kynää.
Aranesp 15 mikrogrammaa injektioneste, liuos, esitäytetty kynä
0,375 ml injektioneste, liuos (40 mcg / ml darbepoetiini alfa), esitäytetty kynä, tyypin 1 lasiruisku ja ruostumattomasta teräksestä valmistettu 27 neula. Pakkaus sisältää 1 tai 4 esitäytettyä kynää.
Aranesp 20 mikrogrammaa injektioneste, liuos, esitäytetty kynä
0,5 ml injektioneste, liuos (40 mcg / ml darbepoetiini alfa), esitäytetty kynä, tyypin 1 lasiruisku ja ruostumattomasta teräksestä valmistettu 27 neula. Pakkaus sisältää 1 tai 4 esitäytettyä kynää.
Aranesp 30 mikrogrammaa injektioneste, liuos, esitäytetty kynä
0,3 ml injektionestettä (100 mcg / ml darbepoetiini alfa) esitäytetyssä kynässä, jossa on tyypin 1 lasiruisku ja ruostumattomasta teräksestä valmistettu 27 neula. Pakkaus sisältää 1 tai 4 esitäytettyä kynää.
Aranesp 40 mikrogrammaa injektioneste, liuos, esitäytetty kynä
0,4 ml injektionestettä (100 μg / ml darbepoetiini alfa) esitäytetyssä kynässä, jossa on tyypin 1 lasiruisku ja ruostumattomasta teräksestä valmistettu 27 neula. Pakkaus sisältää 1 tai 4 esitäytettyä kynää.
Aranesp 50 mcg injektioneste, liuos, esitäytetty kynä
0,5 ml injektioneste, liuos (100 mcg / ml darbepoetiini alfa) esitäytetyssä kynässä, jossa on tyypin 1 lasiruisku ja ruostumattomasta teräksestä valmistettu 27 neula. Pakkaus sisältää 1 tai 4 esitäytettyä kynää.
Aranesp 60 mikrogrammaa injektioneste, liuos, esitäytetty kynä
0,3 ml injektioneste, liuos (200 μg / ml darbepoetiini alfa), esitäytetty kynä, tyypin 1 lasiruisku ja ruostumattomasta teräksestä valmistettu 27 neula. Pakkaus sisältää 1 tai 4 esitäytettyä kynää.
Aranesp 80 mikrogrammaa injektioneste, liuos, esitäytetty kynä
0,4 ml injektionestettä (200 μg / ml darbepoetiini alfa) esitäytetyssä kynässä, jossa on tyypin 1 lasiruisku ja ruostumattomasta teräksestä valmistettu 27 neula. Pakkaus sisältää 1 tai 4 esitäytettyä kynää.
Aranesp 100 mcg injektioneste, liuos, esitäytetty kynä
0,5 ml injektioneste, liuos (200 μg / ml darbepoetiini alfa) esitäytetyssä kynässä, jossa on tyypin 1 lasiruisku ja ruostumattomasta teräksestä valmistettu 27 neula. Pakkaus sisältää 1 tai 4 esitäytettyä kynää.
Aranesp 130 mcg injektioneste, liuos, esitäytetty kynä
0,65 ml injektioneste, liuos (200 mcg / ml darbepoetiini alfa) esitäytetyssä kynässä, jossa on tyypin 1 lasiruisku ja ruostumattomasta teräksestä valmistettu 27 neula. Pakkaus sisältää 1 tai 4 esitäytettyä kynää.
Aranesp 150 mikrogrammaa injektioneste, liuos, esitäytetty kynä
0,3 ml injektioneste, liuos (500 mcg / ml darbepoetiini alfa) esitäytetyssä kynässä, jossa on tyypin 1 lasiruisku ja ruostumattomasta teräksestä valmistettu 27 neula. Pakkaus sisältää 1 tai 4 esitäytettyä kynää.
Aranesp 300 mcg injektioneste, liuos, esitäytetty kynä
0,6 ml injektionestettä (500 mcg / ml darbepoetiini alfa) esitäytetyssä kynässä, jossa on tyypin 1 lasiruisku ja ruostumaton teräs 27 neula. Pakkaus sisältää 1 tai 4 esitäytettyä kynää.
Aranesp 500 mcg injektioneste, liuos, esitäytetty kynä
1 ml injektionestettä (500 mcg / ml darbepoetiini alfa) esitäytetyssä kynässä, jossa on tyypin 1 lasiruisku ja ruostumattomasta teräksestä valmistettu 27 neula. Pakkauskoko 1 tai 4 Aranesp-esitäytettyä kynää.
Esitäytetyn kynän neulansuojus sisältää kuivaa luonnonkumia (lateksin johdannainen) (ks. Kohta 4.4).
Aranesp 25 mcg injektioneste, liuos injektiopullossa
1 ml injektionestettä (25 mcg / ml darbepoetiini alfa) tyypin I lasisessa injektiopullossa, jossa on fluoropolymeeripäällysteiset kumitulpat ja alumiinitiiviste, jossa on pölynpoisto. Pakkauskoko 1 tai 4 injektiopulloa.
Aranesp 40 mcg injektioneste, liuos injektiopullossa
1 ml injektioneste, liuos (40 mcg / ml darbepoetiini alfa) tyypin I lasisessa injektiopullossa, jossa on fluoropolymeeripäällysteiset kumitulpat ja alumiinitiiviste, jossa on pölynpoisto. Pakkauskoko 1 tai 4 injektiopulloa.
Aranesp 60 mcg injektioneste, liuos injektiopullossa
1 ml injektionestettä (60 mcg / ml darbepoetiini alfa) tyypin I lasisessa injektiopullossa, jossa on fluoropolymeeripäällysteiset kumitulpat ja alumiinitiiviste, jossa on pölynpoisto. Pakkauskoko 1 tai 4 injektiopulloa.
Aranesp 100 mcg injektioneste, liuos injektiopullossa
1 ml injektioneste, liuos (100 mcg / ml darbepoetiini alfa) tyypin I lasisessa injektiopullossa, jossa on fluoropolymeeripäällysteiset kumitulpat ja alumiinitiiviste, jossa on pöly pois. Pakkauskoko 1 tai 4 injektiopulloa.
Aranesp 200 mcg injektioneste, liuos injektiopullossa
1 ml injektioneste, liuos (200 mcg / ml darbepoetiini alfa) tyypin I lasisessa injektiopullossa, jossa on fluoropolymeeripäällysteiset kumitulpat ja alumiinitiiviste, jossa on pöly pois. Pakkauskoko 1 tai 4 injektiopulloa.
Aranesp 300 mcg injektioneste, liuos injektiopullossa
1 ml injektioneste, liuos (300 mcg / ml darbepoetiini alfa) tyypin I lasisessa injektiopullossa, jossa on fluoropolymeeripäällysteiset kumitulpat ja alumiinitiiviste, jossa on pölynpoisto. Pakkauskoko 1 tai 4 injektiopulloa.
Kaikkia pakkauskokoja ei välttämättä ole myynnissä.
06.6 Käyttö- ja käsittelyohjeet
Pakkaus sisältää pakkausselosteen, joka sisältää täydelliset käyttö- ja käsittelyohjeet.
Aranesp-esitäytetty kynä (SureClick) antaa täyden annoksen jokaista esitystä varten.
Aranesp on steriili tuote, mutta ei sisällä säilöntäaineita. Älä anna enempää kuin yksi annos. Kaikki jäljellä oleva määrä lääkkeitä on hävitettävä.
Ennen Aranesp -liuoksen antamista on tarkistettava näkyvien hiukkasten puuttuminen. Vain värittömiä, kirkkaita tai hieman opaalinhohtoisia liuoksia tulee pistää. Älä ravista. Anna säiliön lämmetä huoneenlämpöiseksi ennen liuoksen pistämistä.
Käyttämätön lääke ja tästä lääkkeestä peräisin oleva jäte on hävitettävä paikallisten määräysten mukaisesti.
07.0 MYYNTILUVAN HALTIJA
Amgen Europe B.V.
Vähintään 7061
NL-4817 ZK Breda
Alankomaat
08.0 MYYNTILUVAN NUMERO
Aranesp 10 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
EU/1/01/185/001 1 kpl, läpipainopakkaus
EU/1/01/185/002 4 kappaletta läpipainopakkauksessa
EU/1/01/185/033 1 kpl ilman läpipainopakkausta
EU/1/01/185/074 1 kpl, läpipainopakkaus, jossa neulansuoja
EU/1/01/185/075 4 kappaletta läpipainopakkauksessa, jossa on neulansuoja
Aranesp 15 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
EU/1/01/185/003 1 kpl, läpipainopakkaus
EU/1/01/185/004 4 kappaletta läpipainopakkauksessa
EU/1/01/185/034 1 kpl ilman läpipainopakkausta
EU/1/01/185/076 1 kpl, läpipainopakkaus, jossa neulansuoja
EU/1/01/185/077 4 kappaletta läpipainopakkauksessa, jossa on neulansuoja
Aranesp 20 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
EU/1/01/185/005 1 kpl, läpipainopakkaus
EU/1/01/185/006 4 kappaletta läpipainopakkauksessa
EU/1/01/185/035 1 kpl ilman läpipainopakkausta
EU/1/01/185/078 1 kpl, läpipainopakkaus, jossa neulansuoja
EU/1/01/185/079 4 kappaletta läpipainopakkauksessa, jossa on neulansuoja
Aranesp 30 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
EU/1/01/185/007 1 kpl, läpipainopakkaus
EU/1/01/185/008 4 kappaletta läpipainopakkauksessa
EU/1/01/185/036 1 kpl ilman läpipainopakkausta
EU/1/01/185/080 1 kpl, läpipainopakkaus, jossa neulansuoja
EU/1/01/185/081 4 kappaletta läpipainopakkauksessa, jossa on neulansuoja
Aranesp 40 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
EU/1/01/185/009 1 kpl, läpipainopakkaus
EU/1/01/185/010 4 kappaletta läpipainopakkauksessa
EU/1/01/185/037 1 kpl ilman läpipainopakkausta
EU/1/01/185/082 1 kpl, läpipainopakkaus, jossa neulansuoja
EU/1/01/185/083 4 kappaletta läpipainopakkauksessa, jossa on neulansuoja
Aranesp 50 mcg injektioneste, liuos esitäytetyssä ruiskussa
EU/1/01/185/011 1 kpl, läpipainopakkaus
EU/1/01/185/012 4 kappaletta läpipainopakkauksessa
EU/1/01/185/038 1 kpl ilman läpipainopakkausta
EU/1/01/185/084 1 kpl, läpipainopakkaus, jossa neulansuoja
EU/1/01/185/085 4 kappaletta läpipainopakkauksessa, jossa on neulansuoja
Aranesp 60 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
EU/1/01/185/013 1 kpl, läpipainopakkaus
EU/1/01/185/014 4 kappaletta läpipainopakkauksessa
EU/1/01/185/039 1 kpl ilman läpipainopakkausta
EU/1/01/185/086 1 kpl, läpipainopakkaus, jossa neulansuoja
EU/1/01/185/087 4 kappaletta läpipainopakkauksessa, jossa on neulansuoja
Aranesp 80 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
EU/1/01/185/015 1 kpl, läpipainopakkaus
EU/1/01/185/016 4 kappaletta läpipainopakkauksessa
EU/1/01/185/040 1 kpl ilman läpipainopakkausta
EU/1/01/185/088 1 kpl, läpipainopakkaus, jossa neulansuoja
EU/1/01/185/089 4 kappaletta läpipainopakkauksessa, jossa on neulansuoja
Aranesp 100 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
EU/1/01/185/017 1 kpl, läpipainopakkaus
EU/1/01/185/018 4 kappaletta läpipainopakkauksessa
EU/1/01/185/041 1 kpl ilman läpipainopakkausta
EU/1/01/185/090 1 kpl, läpipainopakkaus, jossa neulansuoja
EU/1/01/185/091 4 kappaletta läpipainopakkauksessa, jossa on neulansuoja
Aranesp 130 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
EU/1/01/185/069 1 kpl, läpipainopakkaus
EU/1/01/185/070 4 kappaletta läpipainopakkauksessa
EU/1/01/185/071 1 kpl ilman läpipainopakkausta
EU/1/01/185/092 1 kpl, läpipainopakkaus, jossa neulansuoja
EU/1/01/185/093 4 kappaletta läpipainopakkauksessa, jossa on neulansuoja
Aranesp 150 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
EU/1/01/185/019 1 kpl, läpipainopakkaus
EU/1/01/185/020 4 kappaletta läpipainopakkauksessa
EU/1/01/185/042 1 kpl ilman läpipainopakkausta
EU/1/01/185/094 1 kpl, läpipainopakkaus, jossa neulansuoja
EU/1/01/185/095 4 kappaletta läpipainopakkauksessa, jossa on neulansuoja
Aranesp 300 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
EU/1/01/185/021 1 kpl, läpipainopakkaus
EU/1/01/185/022 4 kappaletta läpipainopakkauksessa
EU/1/01/185/043 1 kpl ilman läpipainopakkausta
EU/1/01/185/096 1 kpl, läpipainopakkaus, jossa neulansuoja
EU/1/01/185/097 4 kappaletta läpipainopakkauksessa, jossa on neulansuoja
Aranesp 500 mikrogrammaa injektioneste, liuos, esitäytetty ruisku
EU/1/01/185/031 1 kpl, läpipainopakkaus
EU/1/01/185/032 4 kappaletta läpipainopakkauksessa
EU/1/01/185/044 1 kpl ilman läpipainopakkausta
EU/1/01/185/098 1 kpl, läpipainopakkaus, jossa neulansuoja
EU/1/01/185/099 4 kappaletta läpipainopakkauksessa, jossa on neulansuoja
Aranesp 10 mikrogrammaa injektioneste, liuos, esitäytetty kynä
EU/1/01/185/045 1 kpl
EU/1/01/185/057 4 kpl
Aranesp 15 mikrogrammaa injektioneste, liuos, esitäytetty kynä
EU/1/01/185/046 1 kpl
EU/1/01/185/058 4 kpl
Aranesp 20 mikrogrammaa injektioneste, liuos, esitäytetty kynä
EU/1/01/185/047 1 kpl
EU/1/01/185/059 4 kpl
Aranesp 30 mikrogrammaa injektioneste, liuos, esitäytetty kynä
EU/1/01/185/048 1 kpl
EU/1/01/185/060 4 kpl
Aranesp 40 mikrogrammaa injektioneste, liuos, esitäytetty kynä
EU/1/01/185/049 1 kpl
EU/1/01/185/061 4 kappaletta
Aranesp 50 mcg injektioneste, liuos, esitäytetty kynä
EU/1/01/185/050 1 kpl
EU/1/01/185/062 4 kappaletta
Aranesp 60 mikrogrammaa injektioneste, liuos, esitäytetty kynä
EU/1/01/185/051 1 kpl
EU/1/01/185/063 4 kappaletta
Aranesp 80 mikrogrammaa injektioneste, liuos, esitäytetty kynä
EU/1/01/185/052 1 kpl
EU/1/01/185/064 4 kappaletta
Aranesp 100 mcg injektioneste, liuos, esitäytetty kynä
EU/1/01/185/053 1 kpl
EU/1/01/185/065 4 kpl
Aranesp 130 mcg injektioneste, liuos, esitäytetty kynä
EU/1/01/185/072 1 kpl
EU/1/01/185/073 4 kappaletta
Aranesp 150 mikrogrammaa injektioneste, liuos, esitäytetty kynä
EU/1/01/185/054 1 kpl
EU/1/01/185/066 4 kappaletta
Aranesp 300 mcg injektioneste, liuos, esitäytetty kynä
EU/1/01/185/055 1 kpl
EU/1/01/185/067 4 kappaletta
Aranesp 500 mcg injektioneste, liuos, esitäytetty kynä
EU/1/01/185/056 1 kpl
EU/1/01/185/068 4 kappaletta
Aranesp 25 mcg injektioneste, liuos injektiopullossa
EU/1/01/185/100 1 kpl
EU/1/01/185/101 4 kpl
Aranesp 40 mcg injektioneste, liuos injektiopullossa
EU/1/01/185/102 1 kpl
EU/1/01/185/103 4 kpl
Aranesp 60 mcg injektioneste, liuos injektiopullossa
EU/1/01/185/104 1 kpl
EU/1/01/185/105 4 kpl
Aranesp 100 mcg injektioneste, liuos injektiopullossa
EU/1/01/185/106 1 kpl
EU/1/01/185/107 4 kpl
Aranesp 200 mcg injektioneste, liuos injektiopullossa
EU/1/01/185/108 1 kpl
EU/1/01/185/109 4 kpl
Aranesp 300 mcg injektioneste, liuos injektiopullossa
EU/1/01/185/110 1 kpl
EU/1/01/185/111 4 kpl
035691017
035691029
035691031
035691043
035691056
035691068
035691070
035691082
035691094
035691106
035691118
035691120
035691132
035691144
035691157
035691169
035691171
035691183
035691195
035691207
035691219
035691221
035691310
035691322
035691334
035691346
035691359
035691361
035691373
035691385
035691397
035691409
035691411
035691423
035691435
035691447
035691536
035691548
035691551
035691563
035691575
035691587
035691599
035691601
035691613
035691625
035691637
035691649
035691652
035691664
035691676
035691688
035691690
035691702
035691714
035691726
035691738
035691740
035691753
035691765
035691777
035691789
09.0 MYYNTILUVAN TAI UUDISTAMISPÄIVÄMÄÄRÄ
Myyntiluvan myöntämisen päivämäärä: 8. kesäkuuta 2001
Viimeisimmän uudistamisen päivämäärä: 19. toukokuuta 2006
10.0 TEKSTIN MUUTTAMISPÄIVÄMÄÄRÄ
Syyskuuta 2015