
Mitä Bortezomib Hospira on ja mihin sitä käytetään?
Bortezomib Hospira on syöpälääke, jota käytetään multippelin myelooman, verisyövän, hoitoon seuraavissa potilasryhmissä:
- aikuispotilaille, joiden sairaus on edennyt vähintään yhden aiemman hoitokerran jälkeen ja jotka ovat jo saaneet tai eivät ole oikeutettuja veren kantasolusiirtoon. Bortezomib Hospiraa käytetään näillä potilailla yksinään tai yhdessä pegyloidun liposomaalisen doksorubisiinin tai deksametasonin kanssa;
- aiemmin hoitamattomille aikuispotilaille, joille ei voida suorittaa suuriannoksista solunsalpaajahoitoa veren kantasolusiirrolla. Näille potilaille Bortezomib Hospiraa käytetään yhdessä melfalaanin ja prednisonin kanssa;
- aiemmin hoitamattomille aikuispotilaille, joille tehdään suuri annos kemoterapiaa ja joiden jälkeen suoritetaan veren kantasolusiirto. Tässä potilasryhmässä Bortezomib Hospiraa käytetään yhdessä deksametasonin tai deksametasonin ja talidomidin kanssa.
Bortezomib Hospira on tarkoitettu myös vaippasolulymfooman, toisen verisyövän, hoitoon aiemmin hoitamattomille aikuisille, joille ei voida tehdä veren kantasolusiirtoa. Vaippasolulymfooman hoitoon Bortezomib Hospiraa käytetään yhdessä rituksimabin, syklofosfamidin, doksorubisiinin ja prednisonin kanssa.
Bortezomib Hospira on geneerinen lääke. Tämä tarkoittaa sitä, että Bortezomib Hospira on samanlainen kuin ”vertailulääke”, jolla on jo Euroopan unionin (EU) myyntilupa Velcade. Lisätietoja geneerisistä lääkkeistä on kysymyksissä ja vastauksissa napsauttamalla tätä.
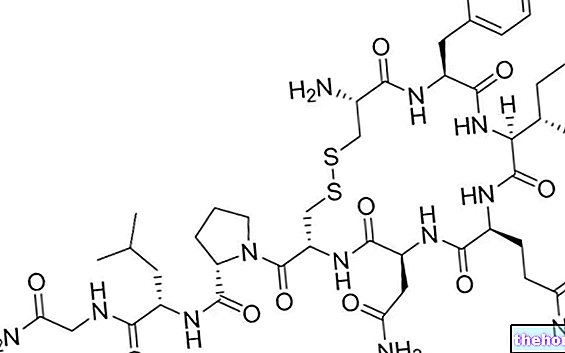
Bortezomib Hospira sisältää vaikuttavana aineena bortetsomibia.
Miten Bortezomib Hospiraa käytetään?
Lääkettä saa vain reseptillä, ja hoito tulee aloittaa ja antaa vain kemoterapeuttisten aineiden käyttöön perehtyneen lääkärin valvonnassa.
Bortezomib Hospiraa on saatavana 3,5 mg: n injektiopulloissa jauheena, josta valmistetaan injektioneste, liuos laskimoon tai ihon alle. Bortezomib Hospiraa ei saa antaa muille reiteille.
Suositeltu annos on laskettava potilaan pituuden ja painon perusteella. Jos liuos annetaan laskimoon, se annetaan katetrin (steriilin putken) kautta. Kahden peräkkäisen Bortezomib Hospira -annoksen välillä on oltava vähintään 72 tuntia. ihon alle injektio annetaan reiteen tai vatsaan (vatsaan).
Bortezomib Hospira -annoksia annetaan jaksoittain, taukojen välillä annosten välillä, kolmen tai kuuden viikon hoitojaksoina riippuen siitä, annetaanko Bortezomib Hospiraa monoterapiana vai yhdessä muiden lääkkeiden kanssa. Jos vakavia haittavaikutuksia ilmenee hoidon jälkeen, hoito on keskeytettävä tai sitä on lykättävä tai annosta on muutettava.
Potilaita, joilla on kohtalainen tai vaikea maksan vajaatoiminta, tulee hoitaa pienemmillä annoksilla. Lisätietoja Bortezomib Hospiran käytöstä on valmisteyhteenvedossa (sisältyy myös EPAR -lausuntoon).
Miten Bortezomib Hospira vaikuttaa?
Bortezomib Hospiran vaikuttava aine bortetsomibi on proteasomien estäjä (mekanismi soluissa, joka hajottaa proteiineja, joita ei enää tarvita), mikä tarkoittaa, että se toimii estämällä niiden toimintaa. Proteasomijärjestelmän tukos aiheuttaa solukuoleman. Syöpäsolut ovat herkempiä kuin normaalit solut proteasomien estäjien, kuten bortetsomibin, vaikutuksille
Mitä hyötyä Bortezomib Hospirasta on havaittu tutkimuksissa?
Koska Bortezomib Hospira on geneerinen lääke, sen hyötyjen ja riskien katsotaan olevan samat kuin alkuperäislääkkeen.
Yhtiö esitti tieteellisestä kirjallisuudesta tietoja bortetsomibista. Lisätutkimuksia ei tarvittu, koska Bortezomib Hospira on geneerinen lääke, joka annetaan injektiona ja joka sisältää samaa vaikuttavaa ainetta kuin alkuperäislääke Velcade.
Mitä riskejä Bortezomib Hospiraan liittyy?
Koska Bortezomib Hospira on geneerinen lääke, sen hyötyjen ja riskien katsotaan olevan samat kuin alkuperäislääkkeen.
Miksi Bortezomib Hospira on hyväksytty?
Viraston ihmisille tarkoitettuja lääkkeitä käsittelevä komitea (CHMP) katsoi, että EU: n vaatimusten mukaisesti Bortezomib Hospira on osoitettu vertailukelpoiseksi Velcaden kanssa. Siksi lääkevalmistekomitea katsoi, että Velcaden tapaan hyödyt ovat havaittuja riskejä suuremmat, ja suositteli, että Bortezomib Hospira hyväksytään käytettäväksi EU: ssa.
Miten voidaan varmistaa Bortezomib Hospiran turvallinen ja tehokas käyttö?
Bortezomib Hospiraa markkinoiva yritys tarjoaa koulutusmateriaalia terveydenhuollon ammattilaisille injektion asettamisesta ja antamisesta, annoksen laskemisesta sekä oikean kantasolusiirron saaneiden potilaiden hoitamisesta.
Bortezomib Hospiran turvallisuutta ja tehokasta käyttöä koskevia suosituksia ja varotoimia, joita terveydenhuollon ammattilaisten ja potilaiden on noudatettava, on myös lisätty valmisteyhteenvetoon ja pakkausselosteeseen.
Lisätietoja Bortezomib Hospirasta
Katso täydellinen versio Bortezomib Hospiran EPAR -arviointilausunnosta viraston verkkosivustolta: ema.europa.eu/Find medicine / Human medicines / European public assessment reports. Lisätietoja Bortezomib Hospira -hoidosta saa pakkausselosteesta (sisältyy EPAR -lausuntoon) tai lääkäriltä tai apteekista.
Viittauslääkkeen täydellinen EPAR -versio on myös viraston verkkosivustolla.
Tällä sivulla julkaistut tiedot Bortezomib Hospirasta voivat olla vanhentuneita tai puutteellisia. Jos haluat käyttää näitä tietoja oikein, katso Vastuuvapauslauseke ja hyödyllisiä tietoja -sivu.











-non-sentire-i-sapori.jpg)

-cos-cause-e-terapia.jpg)






-cos-cause-sintomi-e-cura.jpg)






