Yleisyys
Amyloidoosi on termi, jota käytetään määrittelemään sairauksien ryhmä, jolle on tunnusomaista amyloidiksi määritellyn fibrillaarisen proteiinimateriaalin kertyminen usein solunulkoiselle alueelle.Liukenemattomat amyloidikuidut muodostavat erityisen stabiileja kerrostumia useissa elimissä.

Muut kuvat Amyloidoosi - Galleria 2
Taudin oireet ja vakavuus riippuvat elimistöstä, johon amyloidien kertyminen vaikuttaa pääasiassa, ja amyloidoosin tyypistä. Useimmat tapaukset ovat kuitenkin systeemisiä. Toisin sanoen fibrillikerrostumat ovat laajalle levinneitä ja voivat mahdollisesti heikentää monien kehon kudosten ja elinten toimintaa. . Diagnoosi määritetään biopsialla tutkimalla pieni kudosnäyte mikroskoopilla. Mahdolliset etiologiset tekijät vaihtelevat amyloidoosin variantin mukaan. Saatavilla olevat hoidot voivat auttaa hallitsemaan oireita ja rajoittamaan amyloidituotantoa.
Amyloidikerrostumien ominaisuudet
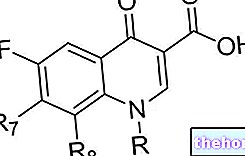
Amyloidoosi johtuu proteiinien toissijaisen rakenteen häiriöistä (β-taitettu arkin kokoonpano). Normaaleissa olosuhteissa proteiinit syntetisoidaan lineaarisessa aminohappojonossa, joka taitettuna saa spesifisen tilakonformaation (proteiinin taitto). Rakenteensa ja siksi oikean proteiinitaitoksensa ansiosta proteiini pystyy suorittamaan fysiologiset tehtävänsä, joista se on vastuussa. Amyloidiproteiinit ovat peräisin solujen väärin käsittelemästä esiasteesta ("vääristymisen" vuoksi) "). Fibrillien muodostavat proteiinit ovat monipuolisia koon, aminohapposekvenssin ja luontaisen rakenteen mukaan, mutta niistä tulee liukenemattomia aggregaatteja, jotka ovat rakenteeltaan ja ominaisuuksiltaan samanlaisia. Fibrillien esiasteita edustavat primaarimolekyylit (esimerkki: immunoglobuliinien kevyt ketju, β2-mikroglobuliini, apolipoproteiini A1 jne.) tai tuotteista, jotka heijastavat aminohappoekvenssi. Poikkeava toissijainen rakenne altistaa fibrillien muodostumiselle, jotka voivat kerääntyä paikallisesti kudoksiin ja elimiin ja johtaa niiden normaalin fysiologisen toiminnan heikkenemiseen. On tunnistettu yli 20 erilaista proteiiniprekursoria, jotka voivat ottaa amyloidikonformaation. miksi niitä esiintyy monia erilaisia amyloidoosia.
Amyloidikerrostumien sijainnin perusteella tauti voidaan jakaa:
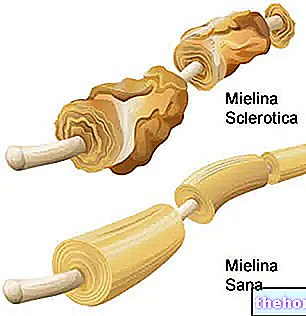
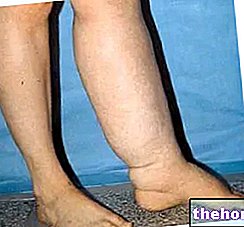
- Paikallinen muoto: rajoittuu tiettyyn elimeen tai kudokseen (sydän, munuaiset, ruoansulatuskanava, hermosto ja dermis) ja on yleensä lievempi kuin systeeminen (diffuusi) muoto. Esimerkiksi amyloidoosi voi vaikuttaa vain ihoon aiheuttaen värimuutoksia ja / tai kutinaa. Erityistä amyloidiproteiinityyppiä on havaittu myös Alzheimerin tautia sairastavien aivoissa. Paikallinen amyloidoosi on tyypillistä ikääntymiselle ja sairastuneille potilaille. Tyypin 2 diabetes (jossa proteiinia kertyy haimaan).
- Systeeminen muoto: amyloidikerrostumia esiintyy eri elimissä ja ne tunnistavat yleensä neoplastisen, tulehduksellisen, geneettisen tai iatrogeenisen alkuperän.
Luokitus
On olemassa monia amyloidoosin muotoja, jotka on luokiteltu fibrillikerrostumien muodostavien proteiinien luonteen mukaan.
Yleisimmät vaihtoehdot ovat:
- Primaarinen amyloidoosi (kutsutaan myös kevyen ketjun amyloidoosiksi, AL);
- Toissijainen amyloidoosi (kutsutaan myös hankituksi amyloidoosiksi, AA);
- Perinnöllinen amyloidoosi;
- Ikääntymiseen liittyvä amyloidoosi (tai seniilinen systeeminen amyloidoosi).








.jpg)