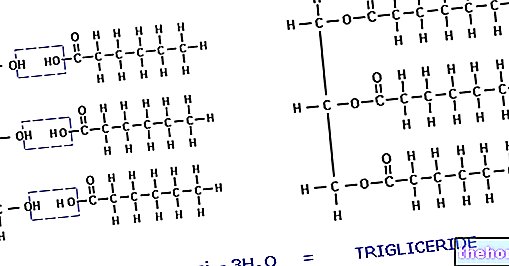
Proteiinit
Proteiinit ovat polymeerimolekyylejä, jotka koostuvat yli 100: sta aminohappoja sidottu peptidisidoksilla (lyhyempiä aminohappoketjuja kutsutaan polypeptideiksi tai peptideiksi); proteiinien rakenne voi olla enemmän tai vähemmän pitkä, taitettuna taaksepäin ja kiinnittynyt muihin molekyyleihin (tekijät, jotka määrittävät niiden monimutkaisuuden ja luonnehtivat niiden biologista toimintaa). Nämä rakenteet voidaan luokitella seuraavasti: primaarirakenne, toissijainen rakenne (a-helix ja β-arkki), tertiäärinen rakenne ja kvaternaarinen rakenne.


Proteiinien toiminnot
Luonnossa proteiinit suorittavat monia toimintoja ja tunnetuin on epäilemättä rakenteellinen; ajattele vain, että jokainen kehomme kudosmatriisi perustuu luurankoon tai polymeeriseen mosaiikkiin, joka muodostuu peptideistä (esim. Lihaskuidut, luumatriisi, kudos- tietystä näkökulmasta, jopa verta).
Vähemmän tärkeä on biosääntelyn ja kemiallisen / hormonaalisen välityksen toiminta, itse asiassa proteiinit ovat sekä entsyymien että monien hormonien perusaineosia.
Veressä proteiineilla on myös erittäin tärkeä kuljetustoiminto; tämä koskee hemoglobiinia (hapen kuljetus), transferriiniä (raudan kuljetus), albumiinia (lipidimolekyylien kuljetus) jne.
Aina verenkierrossa olevat proteiinit osoittautuvat hyödyllisiksi immuunipuolustukseksi; ne muodostavat ANTIBODIES, välttämättömiä lymfosyyttien tuottamia molekyylejä, jotka ovat hyödyllisiä kehon vasteessa taudinaiheuttajia vastaan.
Lopuksi proteiineja - mutta tarkemmin sanottuna aminohappoja - voidaan käyttää energiatarkoituksiin maksan neoglukogeneesin kautta ja ne tarjoavat 4 kilokaloria (kcal) grammaa kohti. Se on melko monimutkainen prosessi, joka mahdollistaa transaminoinnin ja deaminoinnin avulla kehon tuottaa glukoosia hypoglykeemisissä olosuhteissa (mahdollisesti paastoamisen, erityisen voimakkaan ja / tai pitkittyneen lihasten voimakkuuden, haitallisten patologisten tai kliinisten tilojen jne. Vuoksi). voi myös olla ketogeeninen, joten niiden muuntaminen määrää ketonikappaleiksi kutsuttujen happomolekyylien vapautumisen.
HUOM. Proteiinien energiafunktion tulisi olla marginaalinen ja sokerin ja rasvan alainen.
Aminohapot
Aminohapot ovat kvaternaarisia molekyylejä, jotka koostuvat hiilestä, vedystä, hapesta ja typestä. Yli 500 tyyppiä tunnetaan ja niiden yhdistelmä erottaa lukemattomat peptidimuodot. Tavallisia, L-aminohappoja, on 20: alaniini, arginiini, asparagiini, asparagiinihappo, kysteiini, glutamiinihappo, glutamiini, glysiini, histidiini, isoleusiini, leusiini, lysiini, metioniini, fenyylialaniini, proliini, seriini, treoniini, tryptofaani, tyrosiini ja valiini. Jälkimmäisen aineenvaihdunnasta on mahdollista saada laaja valikoima ei-tavallisia tai satunnaisia aminohappoja, jotka koostuvat pääasiassa hormoneista, entsyymeistä tai välimolekyyleistä (karnitiini, homokysteiini, kreatiini, tauriini jne.).
Tavallisten aminohappojen joukosta jotkut EI VOI syntetisoida elimistössä, ja niitä kutsutaan ESSENTIAL :iksi; aikuiselle miehelle niitä on 9: fenyylialaniini, leusiini, isoleusiini, lysiini, metioniini, treoniini, tryptofaani ja valiini. Lapsilla niitä on yhteensä 11; edellä olevaan lisätään: histidiini ja arginiini.
Muita aminohappoluokituksia ovat: niiden sivuketjujen napaisuuden perusteella (neutraali apolaarinen, neutraali polaarinen, happopanos, emäsvaraus) tai radikaaliryhmän tyypin mukaan (hydrofobinen, hydrofiilinen, happo, emäksinen, aromaattinen).
Haarautuneen ketjun aminohapot
Välttämättömien joukossa on myös kolme aminohappoa, joita kutsutaan haarautuneiksi ketjuiksi (BCAA): leusiini, isoleusiini ja valiini; erityispiirre, joka erottaa haarautuneen ketjun aminohapot muista, edustaa erilainen metabolian polku energiantuotannossa.
Kuten jo selitettiin, transaminoinnin ja deaminoinnin jälkeen suurin osa aminohapoista voidaan kohdentaa neoglukogeneesiin ja siirtyä Krebs-sykliin oksaloasetaatti vihaat pyruvaatti. Lopulta, jos todellista tarvetta olisi, jotkut verenkierrossa olevista aminohapoista joutuisivat maksan maksasoluihin ja poistuvat glukoosin muodossa; haarautuneiden aminohappojen kohdalla näin ei ole. Verrattuna muihin BCAA: t ovat molekyylejä, joita lihakset voivat käyttää suoraan, ja tämä ominaisuus tekee niistä paljon tehokkaampia suorassa energiantuotannossa ja muuntamisessa glykogeenivarantojen palauttamiseksi; on sanomattakin selvää, että jos organismi on riittävästi ravittu, haarautuneiden aminohappojen katabolia edustaa lähes merkityksetöntä neoglukogeenistä osaa; glukoosi on AINA ensisijainen energianlähde, joten riittävien glykeemian ja glykogeenivarantojen olosuhteissa ei ole mitään syytä pelätä, että normaalin urheilusuorituksen aikana lihakset tarvitsevat ylimääräistä haarautunutta aminohappoa.
Muut artikkelit aiheesta "Proteiinit ja haarautuneet ketjuaminohapot"
- Haarautuneen ketjun aminohapot: milloin ne otetaan?
- Ruokavalion proteiinit
- Proteiinien hajoaminen - milloin ottaa se?









.jpg)