Vaikuttavat aineet: klopidogreeli
Plavix 75 mg kalvopäällysteiset tabletit
Plavix -pakkausselosteita on saatavana seuraaville pakkauskokoille:- Plavix 75 mg kalvopäällysteiset tabletit
- Plavix 300 mg kalvopäällysteiset tabletit
Miksi Plavixia käytetään? Mitä varten se on?
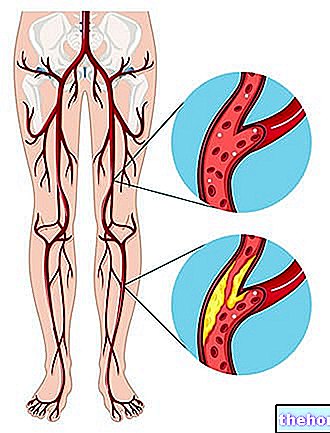
Plavix sisältää klopidogreelia ja kuuluu verihiutaleiden vastaisten lääkkeiden ryhmään. Verihiutaleet ovat veren mikroskooppisia elementtejä, jotka kasautuvat yhteen veren hyytymisen aikana. Estämällä tätä kasautumista verihiutaleiden vastaiset lääkkeet vähentävät verihyytymien muodostumisen mahdollisuutta (ilmiö, jota kutsutaan tromboosiksi).
Aikuiset ottavat Plavixia estääkseen verihyytymien (trombien) muodostumisen kovettuneisiin verisuoniin (valtimoihin), joka tunnetaan aterotromboosina ja joka voi aiheuttaa aterotromboottisia tapahtumia (kuten aivohalvauksen, sydänkohtauksen tai kuoleman). Plavix on määrätty sinulle estämään verihyytymiä ja vähentämään näiden vakavien tapahtumien riskiä, koska:
- sinulla on sairaus, joka tunnetaan valtimoiden kovettumisena (kutsutaan myös ateroskleroosiksi), esim
- sinulla on aiemmin ollut sydänkohtaus, aivohalvaus tai perifeerinen valtimotauti, tai
- sinulla on aiemmin ollut voimakasta rintakipua, joka tunnetaan nimellä "epästabiili angina pectoris" tai "sydäninfarkti" (sydänkohtaus). Tämän sairauden hoitamiseksi lääkäri on saattanut laittaa stentin tukkeutuneeseen tai kaventuneeseen valtimoosi verenkierron palauttamiseksi. estää veren hyytymistä),
- sinulla on epäsäännöllinen sydämenlyönti, eteisvärinäksi kutsuttu tila, etkä voi ottaa lääkkeitä, joita kutsutaan suun kautta otettaviksi antikoagulantteiksi (K -vitamiiniantagonistit), jotka estävät uusien hyytymien muodostumisen ja nykyisten muodostumisen. Sinulle on kerrottu, että "oraaliset antikoagulantit" ovat tehokkaampia kuin asetyylisalisyylihappo tai Plavixin ja asetyylisalisyylihapon yhdistelmäkäyttö tämän tilan hoidossa.Jos et voi ottaa "oraalisia antikoagulantteja" eikä sinulla ole suurentunut verenvuotoriski, lääkäri on saattanut määrätä Plavixia ja asetyylisalisyylihappoa.
Vasta -aiheet Milloin Plavixia ei tule käyttää
Älä ota Plavixia
- Jos olet allerginen (yliherkkä) klopidogreelille tai tämän lääkkeen jollekin muulle aineelle (lueteltu kohdassa 6).
- Jos sinulla on aktiivinen verenvuoto, kuten mahahaava tai verenvuoto aivojen alueella.
- Jos sinulla on vaikea maksasairaus.
Jos luulet, että jokin näistä koskee sinua tai jos olet epävarma, kysy neuvoa lääkäriltäsi ennen Plavixin käyttöä.
Käyttöä koskevat varotoimet Mitä sinun on tiedettävä, ennen kuin otat Plavix -valmistetta
Jos jokin alla mainituista tilanteista ilmenee, kerro siitä lääkärillesi ennen Plavixin ottamista:
- jos sinulla on verenvuotoriski, kuten: - sairaus, joka altistaa sinut sisäiselle verenvuodolle (kuten "mahahaava") - verisairaus, joka saa sinut alttiiksi sisäiselle verenvuodolle (verenvuoto kudoksessa, elimessä tai kehossa nivel) - viimeaikainen vakava vamma - äskettäinen leikkaus (mukaan lukien hammaskirurgia) - leikkaus (mukaan lukien hammaskirurgia), joka on suunniteltu seuraavien 7 päivän aikana
- jos sinulla on ollut hyytymä "aivovaltimossa (iskeeminen aivohalvaus)" viimeisten 7 päivän aikana
- jos sinulla on munuais- tai maksasairaus
- jos sinulla on koskaan ollut allergia tai reaktio mille tahansa lääkkeelle, jota käytetään sairautesi hoitoon
Kun käytät Plavixia:
- Kerro lääkärillesi, jos tarvitset leikkausta (mukaan lukien hammaskirurgia)
- Kerro heti lääkärillesi, jos sinulle kehittyy sairaus (tunnetaan myös nimellä tromboottinen trombosytopeeninen purppura tai PTT), johon kuuluu kuumetta ja mustelmia ihon alla ja jotka näkyvät punaisina pisteinä, tai joilla on selittämätön äärimmäinen väsymys, sekavuus, ihon kellastuminen tai silmät (keltaisuus) (ks. kohta 4 "Mahdolliset haittavaikutukset")
- Jos leikkaat tai vahingoitat itseäsi, verenvuodon pysähtyminen voi kestää tavallista kauemmin. Tämä johtuu lääkkeen toiminnasta, koska se estää verihyytymien muodostumisen. Pienet leikkaukset ja vammat, kuten itsesi leikkaaminen tai parranajo, ei yleensä ole ongelma. Jos kuitenkin olet huolestunut verenvuodostasi, ota heti yhteys lääkäriisi (ks. Kohta 4 '' Mahdolliset haittavaikutukset '')
- Lääkäri voi määrätä verikokeita
Lapset ja nuoret
Älä anna tätä lääkettä lapsille, koska se ei ole tehokas.
Yhteisvaikutukset Mitkä lääkkeet tai elintarvikkeet voivat muuttaa Plavixin vaikutusta
Kerro lääkärille tai apteekkihenkilökunnalle, jos parhaillaan käytät, olet äskettäin käyttänyt tai saatat käyttää muita lääkkeitä, myös lääkkeitä, joita lääkäri ei ole määrännyt.
Jotkut lääkkeet voivat vaikuttaa Plavixin käyttöön tai päinvastoin.
Sinun on kerrottava lääkärille tarkasti, jos käytät:
- oraaliset antikoagulantit, veren hyytymistä vähentävät lääkkeet,
- ei-steroidinen tulehduskipulääke, jota yleensä käytetään lihasten tai nivelten kivuliaiden ja / tai tulehduksellisten tilojen hoitoon,
- hepariini tai muu injektoitava lääke, jota käytetään veren hyytymisen vähentämiseen,
- omepratsoli, esomepratsoli tai simetidiini, vatsavaivojen hoitoon käytettävät lääkkeet
- flukonatsoli, vorikonatsoli, siprofloksasiini tai kloramfenikoli, bakteeri- tai sieni -infektioiden hoitoon käytettävät lääkkeet,
- karbamatsepiini tai okskarbatsepiini, lääkkeitä, joita käytetään joidenkin epilepsian muotojen hoitoon,
- tiklopidiini, muut verihiutaleiden vastaiset aineet,
- selektiivinen serotoniinin takaisinoton estäjä (mukaan lukien, mutta ei rajoittuen, fluoksetiini tai fluvoksamiini), lääkkeet, joita tavallisesti käytetään masennuksen hoitoon,
- moklobemidi, lääke, jota käytetään masennuksen hoitoon.
Jos sinulla on ollut voimakasta rintakipua (epästabiili angina pectoris tai sydänkohtaus), sinulle on ehkä määrätty Plavix yhdessä asetyylisalisyylihapon kanssa, joka on aine, jota esiintyy monissa kipua lievittävissä ja kuumetta lievittävissä lääkkeissä. Asetyylisalisyylihapon satunnaisen käytön (enintään 1000 mg 24 tunnin aikana) ei pitäisi yleensä aiheuttaa ongelmia, mutta pitkäaikaisesta käytöstä muissa olosuhteissa on keskusteltava lääkärisi kanssa.
Plavix ruuan ja juoman kanssa
Plavix voidaan ottaa ruoan kanssa tai ilman.
Varoitukset On tärkeää tietää, että:
Raskaus ja imetys
Tätä lääkettä ei suositella otettavaksi raskauden aikana.
Jos olet raskaana tai epäilet olevasi raskaana, kerro siitä lääkärille tai apteekkihenkilökunnalle ennen Plavixin ottamista. Jos tulet raskaaksi Plavix -hoidon aikana, ota välittömästi yhteys lääkäriisi, koska Plavix -valmisteen käyttöä ei suositella raskauden aikana.
Älä imetä tämän lääkkeen käytön aikana. Jos imetät tai suunnittelet imettämistä, keskustele lääkärisi kanssa ennen tämän lääkkeen ottamista.
Kysy lääkäriltäsi tai apteekista neuvoa ennen minkään lääkkeen käyttöä.
Ajaminen ja koneiden käyttö
Plavix ei todennäköisesti vaikuta ajokykyyn ja koneiden käyttökykyyn.
Plavix sisältää laktoosia
Jos lääkäri on kertonut sinulle, että sinulla on jokin sokeri -intoleranssi (esim. Laktoosi), keskustele lääkärisi kanssa ennen tämän lääkkeen ottamista.
Plavix sisältää hydrattua risiiniöljyä
Tämä voi aiheuttaa vatsavaivoja tai ripulia.
Annos, antotapa ja antotapa Plavixin käyttö: Annostus
Ota tätä lääkettä juuri siten kuin lääkäri tai apteekki on määrännyt.
Jos olet epävarma, käänny lääkärin tai apteekkihenkilökunnan puoleen. Jos sinulla on ollut voimakasta rintakipua (epästabiili angina pectoris tai sydänkohtaus), lääkäri voi antaa sinulle 300 mg Plavixia (1 300 mg: n tabletti tai 4 75 mg: n tablettia) kerran hoidon alussa. Sen jälkeen suositeltu annos on yksi 75 mg: n Plavix -tabletti vuorokaudessa suun kautta ruoan kanssa tai ilman ja samaan aikaan joka päivä.
Plavixia tulee ottaa niin kauan kuin lääkäri katsoo sen tarpeelliseksi.
Yliannostus Mitä tehdä, jos olet ottanut liikaa Plavixia
Jos otat enemmän Plavixia kuin sinun pitäisi
Ota yhteys lääkäriisi tai lähimmän sairaalan päivystykseen verenvuotoriskin vuoksi.
Jos unohdat ottaa Plavixia
Jos unohdat ottaa annoksen, mutta muistat 12 tunnin sisällä tavallisesta ajasta, ota yksi tabletti heti ja ota seuraava tabletti tavalliseen aikaan.
Jos on kulunut yli 12 tuntia, ota yksinkertainen annos tavalliseen aikaan. Älä ota kaksinkertaista annosta korvataksesi unohtamasi tabletin.
Pakkauksissa, joissa on 7, 14, 28 ja 84 tablettia, voit tarkistaa viimeisen Plavix -tabletin ottamispäivän läpipainopakkaukseen painetusta kalenterista.
Jos lopetat Plavixin käytön
Älä lopeta hoitoa, ellei lääkäri niin kehota. Ota yhteys lääkäriisi tai apteekkiin ennen sen lopettamista.
Jos sinulla on kysymyksiä tämän lääkkeen käytöstä, käänny lääkärin tai apteekkihenkilökunnan puoleen.
Sivuvaikutukset Mitkä ovat Plavixin sivuvaikutukset
Kuten kaikki lääkkeet, tämäkin lääke voi aiheuttaa haittavaikutuksia. Kaikki eivät kuitenkaan niitä saa.
Ota heti yhteys lääkäriisi, jos:
- kuume, infektion merkit tai voimakas heikkous. Nämä vaikutukset voivat johtua joidenkin verisolujen harvinaisesta vähenemisestä
- merkkejä maksaongelmista, kuten ihon ja / tai silmien keltaisuus (keltaisuus), johon voi liittyä verenvuotoa tai ilman ja joka ilmenee ihon alla punaisina pisteinä, ja / tai sekavuus (ks. kohta 2 "Varoitukset ja varotoimet")
- suun turvotus tai ihosairaudet, kuten ihottuma, kutina, rakkulat iholla. Nämä voivat olla merkkejä allergisesta reaktiosta.
Plavixin yleisin raportoitu sivuvaikutus on verenvuoto. Verenvuoto voi ilmetä vatsan tai suoliston verenvuotona, mustelmina, mustelmina (epätavallinen verenvuoto tai mustelmat ihon alla), nenäverenvuotoina, verinäytteenä virtsassa.Joissakin tapauksissa verenvuotoa silmään, kallonsisäiseen, keuhkoihin ja niveliin.
Jos sinulla ilmenee pitkittynyttä verenvuotoa Plavix -hoidon aikana
Jos leikkaat tai vahingoitat itseäsi, verenvuodon pysähtyminen voi kestää tavallista kauemmin. Tämä johtuu lääkkeen toiminnasta, koska se estää verihyytymien muodostumisen. Pienet leikkaukset ja vammat, kuten itsesi leikkaaminen tai parranajo, ei yleensä ole ongelma. Jos kuitenkin olet huolestunut verenvuodostasi, ota heti yhteys lääkäriisi (ks. Kohta 2 'Varoitukset ja varotoimet').
Muita haittavaikutuksia ovat:
Yleiset haittavaikutukset (voi esiintyä enintään 1 potilaalla 10: stä):
Ripuli, vatsakipu, ruoansulatushäiriöt tai närästys.
Melko harvinaiset haittavaikutukset (voi esiintyä enintään 1 potilaalla 100: sta):
Päänsärky, mahahaava, oksentelu, pahoinvointi, ummetus, ylimääräinen kaasu mahassa tai suolistossa, ihottuma, kutina, huimaus, pistely ja tunnottomuus.
Harvinaiset haittavaikutukset (voi esiintyä enintään 1 potilaalla 1000: sta):
Huimaus.
Hyvin harvinaiset haittavaikutukset (voi esiintyä enintään 1 potilaalla 10000: sta):
Keltaisuus voimakas vatsakipu, johon liittyy selkäkipu tai ilman sitä; kuume, hengitysvaikeudet, joihin liittyy joskus yskää; yleistyneet allergiset reaktiot (esimerkiksi laajalle levinnyt kuumotus ja äkillinen yleinen huonovointisuus jopa pyörtymiseen); turvotus suussa; ihon rakkulat; ihoallergia; suun kipu (stomatiitti); verenpaineen lasku; sekavuus; hallusinaatiot nivelkipu; lihaskipu; maun muutokset.
Lisäksi lääkäri on saattanut havaita muutoksia veri- ja virtsakokeissa.
Sivuvaikutusten ilmoittaminen
Jos havaitset haittavaikutuksia, käänny lääkärin tai apteekkihenkilökunnan puoleen. Tämä koskee myös kaikkia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa.
Voit ilmoittaa haittavaikutuksista myös suoraan liitteessä V luetellun kansallisen ilmoitusjärjestelmän kautta. Ilmoittamalla haittavaikutuksista voit auttaa saamaan enemmän tietoa tämän lääkkeen turvallisuudesta.
Vanhentuminen ja säilyttäminen
Ei lasten ulottuville eikä näkyville.
Älä käytä tätä lääkettä pakkauksessa ja läpipainopakkauksessa mainitun viimeisen käyttöpäivämäärän (EXP) jälkeen. Viimeinen käyttöpäivämäärä tarkoittaa kuukauden viimeistä päivää.
Katso ulkopakkauksessa mainitut säilytysolosuhteet. Jos Plavix toimitetaan PVC / PVDC / alumiiniläpipainopakkauksissa, säilytä alle 30 ° C: ssa. Jos Plavix toimitetaan alumiini / alumiiniläpipainopakkauksissa, lääkevalmiste ei vaadi erityisiä säilytysolosuhteita.
Älä käytä tätä lääkettä, jos huomaat näkyviä heikkenemisen merkkejä.
Älä heitä lääkkeitä viemäriin tai talousjätteisiin. Kysy apteekista, kuinka heittää pois lääkkeet, joita et enää käytä. Tämä auttaa suojelemaan ympäristöä.
Koostumus ja lääkemuoto
Mitä Plavix sisältää
Vaikuttava aine on klopidogreeli. Yksi tabletti sisältää 75 mg klopidogreelia (vetysulfaattina).
Muut aineet ovat (ks. Kohta 2 "Plavix sisältää laktoosia" ja "Plavix sisältää hydrattua risiiniöljyä"):
- Tabletin ydin: mannitoli (E421), hydrattu risiiniöljy, mikrokiteinen selluloosa, makrogoli 6000 ja vähän substituoitu hydroksipropyyliselluloosa,
- Tabletin päällyste: laktoosimonohydraatti (maitosokeri), hypromelloosi (E464), triasetiini (E1518), punainen rautaoksidi (E 172), titaanidioksidi (E 171)
- Kiillotusaine: karnaubavaha.
Lääkevalmisteen kuvaus ja pakkaus
Plavix 75 mg kalvopäällysteiset tabletit ovat pyöreitä, kaksoiskupera, vaaleanpunaisia, ja niiden toisella puolella on numero "75" ja toisella puolella numero "1171".
- 7, 14, 28, 30, 84, 90 ja 100 tablettia PVC / PVDC / alumiiniläpipainopakkauksessa tai alumiini / alumiiniläpipainopakkauksessa,
- 50 x 1 tablettia PVC / PVDC / alumiiniläpipainopakkauksissa tai kerta-annospakkauksina. Kaikkia pakkauskokoja ei välttämättä ole myynnissä.
Alkuperäinen pakkausseloste: AIFA (Italian lääkevirasto). Sisältö julkaistu tammikuussa 2016. Esitetyt tiedot eivät välttämättä ole ajan tasalla.
Jotta saat käyttöösi uusimman version, on suositeltavaa käyttää AIFA: n (Italian Medicines Agency) verkkosivustoa. Vastuuvapauslauseke ja hyödyllistä tietoa.
01.0 LÄÄKEVALMISTEEN NIMI
PLAVIX 75 MG TABLETIT, PÄÄLLYTETTY FILMILLÄ
02.0 LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS
Yksi kalvopäällysteinen tabletti sisältää 75 mg klopidogreelia (vetysulfaattina).
Apuaineet, joiden vaikutukset tunnetaan:
Yksi kalvopäällysteinen tabletti sisältää 3 mg laktoosia ja 3,3 mg hydrattua risiiniöljyä.
Täydellinen apuaineluettelo, katso kohta 6.1.
03.0 LÄÄKEMUOTO
Kalvopäällysteinen tabletti
Vaaleanpunainen, pyöreä, kaksoiskupera, kaiverrettu "75" toisella puolella ja "1171" toisella puolella.
04.0 KLIINISET TIEDOT
04.1 Käyttöaiheet
Aterotromboottisten tapahtumien ehkäisy
Klopidogreeli on tarkoitettu:
• Aikuispotilaat, joilla on sydäninfarkti (muutamasta päivästä alle 35 päivään), iskeeminen aivohalvaus (7 päivästä alle 6 kuukauteen) tai todettu perifeerinen valtimotauti
• Aikuiset potilaat, joilla on akuutti sepelvaltimotauti:
- akuutti sepelvaltimo -oireyhtymä ilman ST -segmentin kohoamista (epästabiili angina pectoris tai sydäninfarkti ilman Q -aaltoja), mukaan lukien potilaat, joille on asetettu stentti perkutaanisen sepelvaltimotoimenpiteen jälkeen yhdessä asetyylisalisyylihapon (ASA) kanssa.
- akuutti sepelvaltimo -oireyhtymä, johon liittyy ST -segmentin nousu yhdessä ASA: n kanssa lääkehoitopotilailla, jotka ovat ehdolla trombolyyttiseen hoitoon.
Aterotromboottisten ja tromboembolisten tapahtumien ehkäisy eteisvärinässä
Klopidogreeli yhdessä ASA: n kanssa on tarkoitettu aterotromboottisten ja tromboembolisten tapahtumien, mukaan lukien aivohalvauksen, ehkäisyyn aikuisilla eteisvärinäpotilailla, joilla on vähintään yksi verisuonitapahtumien riskitekijä ja jotka eivät sovellu hoitoon K -vitamiiniantagonisteilla (AVK) ja joilla on pieni verenvuotoriski.
Lisätietoja on kohdassa 5.1.
04.2 Annostus ja antotapa
Annostus
• Aikuiset ja vanhukset
Klopidogreeli annetaan kerta -annoksena 75 mg.
Potilaat, joilla on akuutti sepelvaltimotauti:
- akuutti sepelvaltimo -oireyhtymä ilman ST -segmentin kohoamista (epästabiili angina pectoris tai sydäninfarkti ilman Q -aaltoja): Klopidogreelihoito tulee aloittaa yhdellä 300 mg: n kyllästysannoksella ja jatkaa sitten annoksella 75 mg kerran vuorokaudessa (yhdessä asetyylisalisyylihapon (ASA) kanssa 75 mg) -325 mg päivässä). Koska suurempia ASA -annoksia on korreloitu korkeamman verenvuotoriskin kanssa, on suositeltavaa, että ASA -annos ei ylitä 100 mg. Optimaalista hoidon kestoa ei ole virallisesti vahvistettu. Kliinisistä tutkimuksista saadut tiedot tukevat käyttöä enintään 12 kuukauteen, ja suurin hyöty saavutettiin 3 kuukauden kuluttua (ks. Kohta 5.1).
- ST -segmentin kohoava akuutti sydäninfarkti: klopidogreeli on annettava 75 mg: n kerta -annoksena, alkaen 300 mg: n aloitusannoksesta yhdessä ASA: n kanssa, trombolyyttisten lääkkeiden kanssa tai ilman. Yli 75 -vuotiailla potilailla klopidogreelihoito tulee aloittaa ilman kyllästysannosta. Yhdistelmähoito on aloitettava mahdollisimman varhain oireiden ilmaantumisen jälkeen ja sitä on jatkettava vähintään 4 viikkoa. Tässä tilanteessa klopidogreelin ja ASA: n yhdistämisen hyötyä ei ole tutkittu (ks. Kohta 5.1).
Potilaille, joilla on eteisvärinä, klopidogreeli voidaan antaa kerta -annoksena 75 mg. ASA-hoito (75--100 mg vuorokaudessa) tulee aloittaa ja jatkaa yhdessä klopidogreelin kanssa (ks. Kohta 5.1).
Jos annos jää väliin:
- 12 tunnin kuluessa suunnitellusta annoksesta: potilaan on otettava annos välittömästi ja seuraava annos tavanomaiseen aikaan.
- jos yli 12 tuntia on kulunut: potilaan on otettava seuraava annos tavalliseen aikaan eikä hänen pitäisi ottaa kaksinkertaista annosta.
• Pediatriset potilaat
Klopidogreelia ei saa käyttää lapsille tehokkuuden vuoksi. (ks. kohta 5.1)
• Munuaisten vajaatoiminta
Terapeuttinen kokemus munuaisten vajaatoimintaa sairastavista potilaista on rajallinen (ks. Kohta 4.4).
• Maksan vajaatoiminta
Terapeuttinen kokemus potilaista, joilla on kohtalainen maksan vajaatoiminta ja joilla saattaa olla verenvuototaipumus, on rajallinen (ks. Kohta 4.4).
Antotapa
Suun kautta.
Tabletti voidaan ottaa aterian yhteydessä tai ilman.
04.3 Vasta -aiheet
• Yliherkkyys vaikuttavalle aineelle tai kohdassa 2 tai 6.1 mainituille apuaineille.
• Vaikea maksan vajaatoiminta.
• Patologinen verenvuoto, kuten esim. mahahaavan tai kallonsisäisen verenvuodon läsnä ollessa.
04.4 Varoitukset ja käyttöön liittyvät varotoimet
Verenvuoto ja hematologiset patologiat
Verenvuodon ja hematologisten haittavaikutusten riskin vuoksi täydellinen verenkuva ja / tai muut asianmukaiset testit on otettava välittömästi huomioon aina, kun hoidon aikana ilmenee verenvuotoon viittaavia kliinisiä oireita (ks. Kohta 4.8) Kuten muidenkin verihiutaleiden vastaisten lääkkeiden kanssa, klopidogreelin tulee sitä tulee käyttää varoen potilailla, joilla voi olla lisääntynyt verenvuoto trauman, leikkauksen tai muun patologisen tilan jälkeen, sekä potilailla, joita hoidetaan ASA: lla, hepariinilla, glykoproteiini-inhibiittoreilla. IIb / IIIa tai ei-steroidiset tulehduskipulääkkeet -2 -inhibiittoreita tai selektiivisiä serotoniinin takaisinoton estäjiä (SSRI -lääkkeitä) .Potilaita on seurattava tarkasti mahdollisten verenvuodon merkkien, myös piilevän verenvuodon, varalta etenkin ensimmäisten hoitoviikkojen aikana ja / tai sydäntoimenpiteiden jälkeen invasiivisia tai kirurgisia toimenpiteitä. Klopidogreelin ja oraalisten antikoagulanttien samanaikaista käyttöä ei suositella, koska se voi lisätä verenvuodon voimakkuutta (ks. Kohta 4.5).
Jos potilaalle tehdään elektiivinen leikkaus, johon verihiutaleiden vastaista toimintaa ei tilapäisesti suositella, klopidogreelin käyttö on lopetettava 7 päivää ennen leikkausta. Ennen leikkausta ja ennen uuden leikkauksen aloittamista. Lääkitys Potilaiden tulee kertoa lääkärille ja hammaslääkärille, että Klopidogreeli pidentää verenvuotoaikaa ja sitä tulee käyttää varoen potilailla, joilla on verenvuotoon alttiita leesioita (erityisesti maha-suolikanavan ja silmänsisäisiä).
Potilaita tulee neuvoa, että klopidogreelin käyttö (yksinään tai yhdessä ASA: n kanssa) voi pidentää verenvuotoa ja että heidän on ilmoitettava lääkärille mahdollisista epänormaaleista verenvuodoista (paikannus tai kesto).
Tromboottinen trombosytopeeninen purppura (PTT)
Tromboottista trombosytopeenista purppuraa (TTP) on raportoitu hyvin harvoin klopidogreelin käytön jälkeen, joskus lyhyen altistuksen jälkeen.Tämä on ominaista trombosytopenia ja mikroangiopaattinen hemolyyttinen anemia, johon liittyy tai liittyy neurologisia ongelmia, munuaisten vajaatoimintaa tai kuumetta.
TTP on mahdollisesti kuolemaan johtava tila, joka vaatii välitöntä hoitoa, mukaan lukien plasmafereesi.
Hankittu hemofilia
Hankittua hemofiliaa on raportoitu klopidogreelin käytön jälkeen. Jos yksittäinen aktivoitu osittainen tromboplastiiniaika (aPTT) pidentyy jatkuvalla verenvuodolla tai ilman sitä, on harkittava hankittua hemofiliaa. Potilaita, joilla on vahvistettu diagnoosi hankitusta hemofiliasta, tulee hoitaa ja hoitaa lääkäri. Klopidogreelihoito on lopetettava.
Äskettäinen iskeeminen aivohalvaus
Tietojen puutteen vuoksi klopidogreelia ei voida suositella ensimmäisten 7 päivän aikana akuutin iskeemisen aivohalvauksen jälkeen.
Sytokromi P450 2C19 (CYP2C19)
Farmakogenetiikka: Kun klopidogreelia annetaan suositellulla annoksella potilaille, joilla on heikko CYP2C19 -metaboloija, klopidogreelin aktiivisen metaboliitin muodostuminen vähenee ja vaikutus verihiutaleiden toimintaan on vähäinen.Testit ovat saatavilla potilaan CYP2C19 -genotyypin tunnistamiseksi.
Koska klopidogreeli muuttuu osittain aktiiviseksi metaboliitiksi CYP2C19 -entsyymin välityksellä, tämän entsyymin toimintaa estävien lääkkeiden käytön odotetaan johtavan klopidogreelin aktiivisen metaboliitin farmakologisten tasojen laskuun. Tämän vuorovaikutuksen kliininen merkitys on epävarma. Varotoimenpiteenä vahvojen tai kohtalaisten CYP2C19 -estäjien samanaikaista käyttöä ei suositella (katso luettelo CYP2C19 -estäjistä kohdasta 4.5; katso myös kohta 5.2).
Ristireaktiot tienopyridiinien välillä
Potilaiden kliininen historia yliherkkyydestä tienopyridiinille (kuten klopidogreelille, tiklopidiinille, prasugreelille) on arvioitava, koska tienopyridiinien välillä on raportoitu ristireaktiivisuutta (ks. Kohta 4.8 "Haittavaikutukset"). Tienopyridiinit voivat aiheuttaa kohtalaisia tai vaikeita allergisia reaktioita, kuten ihottumaa, angioedeemaa tai hematologisia ristireaktioita, kuten trombosytopeniaa ja neutropeniaa. Potilailla, joilla on aiemmin ollut allerginen ja / tai hematologinen reaktio yhdelle tienopyridiinille, saattaa olla suurempi riski saada sama tai "muu reaktio" toiseen tienopyridiiniin. Yliherkkyysoireiden seurantaa suositellaan potilailla, joilla on tunnettu allergia tienopyridiinille.
Munuaisten vajaatoiminta
Klopidogreelin käytöstä on vain vähän kokemusta munuaisten vajaatoimintaa sairastavilla potilailla, joten klopidogreelia on käytettävä varoen näille potilaille (ks. Kohta 4.2).
Maksan vajaatoiminta
Terapeuttinen kokemus klopidogreelin käytöstä potilailla, joilla on kohtalainen maksan vajaatoiminta ja joilla voi olla verenvuototaipumus, on siksi vähäinen, joten klopidogreelia on käytettävä varoen näille potilaille (ks. Kohta 4.2).
Apuaineet
Plavix sisältää laktoosia. Potilaiden, joilla on harvinainen perinnöllinen galaktoosi-intoleranssi, Lapp-laktaasin puutos tai glukoosi-galaktoosi-imeytymishäiriö, ei tule käyttää lääkettä.
Tämä lääke sisältää hydrattua risiiniöljyä, joka voi aiheuttaa vatsavaivoja ja ripulia.
04.5 Yhteisvaikutukset muiden lääkevalmisteiden kanssa sekä muut yhteisvaikutukset
Oraaliset antikoagulantit: klopidogreelin ja oraalisten antikoagulanttien samanaikaista käyttöä ei suositella, koska se voi lisätä verenvuodon voimakkuutta (ks. kohta 4.4). Vaikka klopidogreelin 75 mg / vrk antaminen ei muuttanut S-varfariinin farmakokinetiikkaa tai kansainvälistä normalisoitua suhdetta (INR) potilailla, jotka saavat pitkäaikaista varfariinia, klopidogreelin ja varfariinin samanaikainen käyttö lisää verenvuotoriskiä. riippumattomat vaikutukset hemostaasiin.
Glykoproteiini IIb / IIIa: n estäjät: klopidogreelia on käytettävä varoen potilailla, jotka saavat samanaikaisesti glykoproteiini IIb / IIIa: n estäjiä (ks. kohta 4.4).
Asetyylisalisyylihappo (ASA) : ASA ei muuta ADP: n aiheuttaman verihiutaleiden aggregaation klopidogreelin välittämää estoa; klopidogreeli kuitenkin tehostaa ASA: n vaikutusta kollageenin aiheuttamaan verihiutaleiden aggregaatioon. Kuitenkin 500 mg ASA: n samanaikainen anto kahdesti vuorokaudessa yhden päivän ajan ei pidentänyt merkittävästi entisestään klopidogreelin aiheuttamaa verenvuotoaikaa. Farmakodynaamiset yhteisvaikutukset ovat mahdollisia klopidogreelin ja asetyylisalisyylihapon välillä, mikä lisää verenvuotoriskiä, joten samanaikaista käyttöä on noudatettava varoen (ks. Kohta 4.4). Kuitenkin klopidogreelia ja ASA: ta annettiin yhdessä enintään 1 vuoden ajan (ks. Kohta 5.1).
Hepariini: Terveillä koehenkilöillä tehdyssä kliinisessä tutkimuksessa klopidogreelin annon jälkeen hepariiniannoksen muuttaminen ei ollut tarpeen eikä hepariinin vaikutus hyytymiseen muuttunut. Hepariinin samanaikainen anto ei vaikuttanut klopidogreelin aiheuttamaan verihiutaleiden aggregaation estoon. Farmakodynaamiset yhteisvaikutukset ovat mahdollisia klopidogreelin ja hepariinin välillä, mikä lisää verenvuotoriskiä, joten samanaikaista käyttöä on noudatettava varoen (ks. Kohta 4.4).
Trombolyytit: klopidogreelin, fibriinin tai ei-fibriinispesifisten trombolyyttisten lääkkeiden ja hepariinien samanaikaisen käytön turvallisuutta tutkittiin potilailla, joilla oli akuutti sydäninfarkti.
Kliinisesti merkittävän verenvuodon ilmaantuvuus oli samanlainen kuin trombolyyttisiä lääkkeitä ja hepariinia annettaessa yhdessä ASA: n kanssa (ks. Kohta 4.8).
Tulehduskipulääkkeet: kliinisessä tutkimuksessa, joka suoritettiin terveillä vapaaehtoisilla, klopidogreelin ja naprokseenin samanaikainen anto johti salattujen maha -suolikanavan verenvuotojen lisääntymiseen.
Kuitenkin, koska yhteisvaikutustutkimuksia muiden tulehduskipulääkkeiden kanssa ei ole, on tällä hetkellä epäselvää, onko kaikkien tulehduskipulääkkeiden kanssa lisääntynyt ruoansulatuskanavan verenvuodon riski. Siksi tulehduskipulääkkeiden, mukaan lukien COX-2-estäjät ja klopidogreeli, samanaikainen anto on tehtävä varoen (ks. Kohta 4.4).
Selektiiviset serotoniinin takaisinoton estäjät (SSRI): Koska SSRI-lääkkeet vaikuttavat verihiutaleiden aktivaatioon ja lisäävät verenvuotoriskiä, SSRI-lääkkeiden samanaikainen käyttö klopidogreelin kanssa on tehtävä varoen.
Muut samanaikaiset hoidot:
Koska klopidogreeli muuttuu osittain aktiiviseksi metaboliitiksi CYP2C19 -entsyymin välityksellä, tämän entsyymin toimintaa estävien lääkkeiden käytön odotetaan johtavan klopidogreelin aktiivisen metaboliitin farmakologisten tasojen laskuun. Tämän vuorovaikutuksen kliininen merkitys on epävarma. Varotoimenpiteenä voimakkaiden tai kohtalaisten CYP2C19 -estäjien samanaikaista käyttöä on vältettävä (ks. Kohdat 4.4 ja 5.2).
Lääkkeitä, jotka estävät CYP2C19: tä, ovat omepratsoli ja esomepratsoli, fluvoksamiini, fluoksetiini, moklobemidi, vorikonatsoli, flukonatsoli, tiklopidiini, siprofloksasiini, simetidiini, karbamatsepiini, oksikarbatsepiini ja kloramfenikoli.
Protonipumpun estäjät (PPI)
Omepratsolin kerta -annos 80 mg / vrk ja klopidogreeli samanaikaisesti ja 12 tunnin välein vähensi altistumista aktiiviselle metaboliitille 45% (kyllästysannos) ja 40% (ylläpitoannos). verihiutaleiden aggregaation estämisen väheneminen 39% (kyllästysannos) ja 21% (ylläpitoannos). samanlainen vuorovaikutus.
Sekä kliinisissä että havainnointitutkimuksissa on raportoitu ristiriitaisia tietoja tämän farmakokineettisen (PK) / farmakodynaamisen (PD) vuorovaikutuksen kliinisistä vaikutuksista merkittäviin sydän- ja verisuonitapahtumiin. Varotoimenpiteenä omepratsolin ja esomepratsolin samanaikaista käyttöä tulee välttää (ks. Kohta 4.4).
Pantopratsolin ja lansopratsolin käytön yhteydessä metaboliittialtistuksen vähenemistä havaittiin vähemmän.
Aktiivisen metaboliitin pitoisuudet plasmassa pienenivät 20% (kyllästysannos) ja 14% (ylläpitoannos) samanaikaisen hoidon aikana pantopratsolia 80 mg kerran vuorokaudessa. Tämä liittyi verihiutaleiden aggregaation keskimääräisen estämisen vähenemiseen 15% ja 11%. Nämä tulokset osoittavat, että klopidogreelia voidaan antaa yhdessä pantopratsolin kanssa.
Ei ole näyttöä siitä, että muut mahahapon happamuutta vähentävät lääkkeet, kuten H2 -salpaajat (paitsi simetidiini, joka on CYP2C19: n estäjä) tai antasidit, häiritsevät klopidogreelin verihiutaleiden toimintaa.
Muut lääkkeet:
Klopidogreelilla ja muilla samanaikaisilla hoidoilla on tehty useita muita kliinisiä tutkimuksia mahdollisten farmakodynaamisten ja farmakokineettisten yhteisvaikutusten tutkimiseksi.
Merkittäviä farmakodynaamisia yhteisvaikutuksia ei havaittu, kun klopidogreelia annettiin yhdessä atenololin tai nifedipiinin kanssa yksin tai yhdistelmänä. Lisäksi fenobarbitaalin tai estrogeenin samanaikainen anto ei vaikuttanut merkittävästi klopidogreelin farmakodynaamiseen aktiivisuuteen.
Klopidogreelin samanaikainen käyttö ei vaikuttanut digoksiinin ja teofylliinin farmakokinetiikkaan. Antasidit eivät muuttaneet klopidogreelin imeytymistä.
CAPRIE -tutkimuksen tiedot osoittavat, että fenytoiinia ja tolbutamidia, jotka metaboloituvat CYP2C9: n kautta, voidaan turvallisesti antaa samanaikaisesti klopidogreelin kanssa.
Edellä kuvattujen erityislääkkeiden yhteisvaikutuksia koskevien tietojen lisäksi klopidogreelin ja joidenkin aterotromboottista tautia sairastaville potilaille yleisesti annettavien lääkkeiden kanssa ei ole tehty yhteisvaikutustutkimuksia. Klopidogreelin kliinisiin tutkimuksiin osallistuneet potilaat saivat kuitenkin useita samanaikaisia hoitoja, mukaan lukien diureetit, beetasalpaajat, ACE: n estäjät, kalsiumkanavan salpaajat, kolesterolia alentavat aineet, sepelvaltimoiden laajentimet, diabeteslääkkeet (mukaan lukien insuliini), epilepsialääkkeet ja glykoproteiini IIb / IIIa -antagonistit ilman todisteita kliinisesti merkittävistä negatiivisista vuorovaikutuksista.
04.6 Raskaus ja imetys
Raskaus
Koska kliinistä tietoa klopidogreelialtistuksesta raskauden aikana ei ole saatavilla, klopidogreelia ei suositella käytettäväksi raskauden aikana varotoimenpiteenä.
Eläinkokeet eivät osoita suoria tai epäsuoria haitallisia vaikutuksia raskauteen, alkion / sikiön kehitykseen, synnytykseen tai synnytyksen jälkeiseen kehitykseen (ks. Kohta 5.3).
Ruokinta-aika
Ei tiedetä, erittyykö klopidogreeli äidinmaitoon. Eläinkokeet ovat osoittaneet, että klopidogreeli erittyy maitoon. Varotoimenpiteenä imetystä ei saa jatkaa Plavix -hoidon aikana.
Hedelmällisyys
Eläinkokeissa klopidogreeli ei osoittanut hedelmällisyyden heikkenemistä.
04.7 Vaikutus ajokykyyn ja koneiden käyttökykyyn
Klopidogreelilla ei ole haitallista vaikutusta ajokykyyn tai koneiden käyttökykyyn.
04.8 Haittavaikutukset
Yhteenveto turvallisuusprofiilista
Klopidogreelin turvallisuutta on arvioitu yli 44 000 potilaalla, jotka ovat osallistuneet kliinisiin tutkimuksiin, joista yli 12 000 on hoidettu vähintään vuoden ajan. CAPRIE -tutkimuksessa klopidogreeli annoksella 75 mg / vrk oli kaiken kaikkiaan verrattavissa ASA 325 mg / vrk potilaiden iästä, sukupuolesta ja rodusta riippumatta. COMMIT ja ACTIVE-A käsitellään alla.
Kliinisten tutkimusten kokemusten lisäksi haittavaikutuksia on raportoitu spontaanisti.
Verenvuoto on yleisimmin raportoitu reaktio sekä kliinisissä tutkimuksissa että markkinoille tulon jälkeen, jolloin sitä raportoitiin pääasiassa ensimmäisen hoitokuukauden aikana.
CAPRIE-tutkimuksessa sekä klopidogreeli- että ASA-hoitoa saaneilla potilailla verenvuotojen yleinen ilmaantuvuus oli 9,3%. Vaikeiden tapausten ilmaantuvuus oli samanlainen klopidogreelilla ja ASA: lla.
CURE -tutkimuksessa klopidogreeli ja ASA eivät saaneet liiallista suurta verenvuotoa 7 päivän aikana sepelvaltimon ohitussiirron jälkeen potilailla, jotka lopettivat hoidon yli 5 päivää ennen leikkausta. 5 päivää ennen ohitusleikkausta esiintyvyys oli 9,6% klopidogreelilla ja ASA: lla ja 6,3% lumelääkkeellä ja ASA: lla.
CLARITY -tutkimuksessa verenvuoto lisääntyi yleisesti klopidogreeli ja ASA -ryhmässä verrattuna lumelääke ja ASA -ryhmään. Suurten verenvuotojen ilmaantuvuus oli samanlainen kaikissa ryhmissä.Tämä tulos oli johdonmukainen kaikissa potilaiden alaryhmissä, jotka määriteltiin lähtötilanteen ominaisuuksien ja fibrinolyyttisen tai hepariinihoidon tyypin mukaan.
COMMIT-tutkimuksessa ei-aivoverenvuotojen tai aivoverenvuotojen kokonaismäärä oli alhainen ja samanlainen molemmissa ryhmissä.
ACTIVE-A-tutkimuksessa vakavien verenvuotojen kokonaisluku oli suurempi klopidogreeli + ASA -ryhmässä kuin lumelääke + ASA-ryhmässä (6,7% vs 4,3%). Suuri verenvuoto oli pääasiassa ekstrakraniaalista alkuperää molemmissa ryhmissä (5,3% klopidogreeli + ASA -ryhmässä; 3,5% lumelääke + ASA -ryhmässä), useimmiten maha -suolikanavassa (3,5% vs 1,8%). Liikaa kallonsisäistä verenvuotoa havaittiin klopidogreeli + ASA -ryhmässä verrattuna lumelääke + ASA -ryhmään (1,4% vs. 0,8%). Kuolemaan johtaneiden verenvuotojen (1,1% klopidogreeli + ASA -ryhmässä ja 0,7% plasebo + ASA -ryhmässä) ja verenvuotohäiriöiden (0,8% ja 0,6%) välillä ei ollut tilastollisesti merkitseviä eroja ryhmien välillä.
Taulukko haittavaikutuksista
Kliinisissä tutkimuksissa havaitut tai spontaanisti raportoidut haittavaikutukset on esitetty alla olevassa taulukossa. Niiden esiintymistiheys määritellään seuraavien käytäntöjen mukaisesti: yleinen (≥ 1/100,
* Tietoja klopidogreelista, jonka esiintymistiheys on "tuntematon".
Epäillyistä haittavaikutuksista ilmoittaminen
Ilmoittaminen epäillyistä haittavaikutuksista, jotka ilmenevät lääkkeen myyntiluvan myöntämisen jälkeen, on tärkeää. Se mahdollistaa jatkuvan seurannan lääkkeen hyöty -haittasuhteesta. Terveydenhuollon ammattilaisia pyydetään ilmoittamaan kaikista epäillyistä haittavaikutuksista kansallisen ilmoitusjärjestelmän kautta. "Liite V .
04.9 Yliannostus
Klopidogreelin yliannostus voi johtaa pitkittyneeseen vuotoaikaan ja siitä johtuviin verenvuotokomplikaatioihin. Jos verenvuotoa havaitaan, asianmukaista hoitoa on harkittava.
Klopidogreelin farmakologiselle aktiivisuudelle ei ole tunnettua vastalääkettä. Kun pidennetyn vuotoajan nopea korjaaminen on tarpeen, verihiutaleiden siirto voi kääntää klopidogreelin vaikutukset.
05.0 FARMAKOLOGISET OMINAISUUDET
05.1 Farmakodynaamiset ominaisuudet
Farmakoterapeuttinen ryhmä: verihiutaleita estävät aineet, pois lukien hepariini.
ATC -koodi: B01AC / 04.
Toimintamekanismi
Klopidogreeli on aihiolääke, yksi sen metaboliiteista on verihiutaleiden aggregaation estäjä.
Klopidogreeli on metaboloitava CYP450 -entsyymien välityksellä, jotta muodostuu aktiivinen metaboliitti, joka estää verihiutaleiden aggregaatiota.
Klopidogreelin aktiivinen metaboliitti estää selektiivisesti adenosiinidifosfaatin (ADP) sitoutumista sen verihiutaleiden P2Y12-reseptoriin ja siten estää GPIIb-IIIa-glykoproteiinikompleksin ADP-välitteistä aktivaatiota ja siten verihiutaleiden aggregaatiota.
Palauttamattoman sitoutumisen vuoksi klopidogreelille altistuneet verihiutaleet vaikuttavat loppuelämänsä (noin 7-10 päivää) ja verihiutaleiden normaali toiminta palautuu normaalisti verihiutaleiden vaihtuvuudesta riippuen. Muiden agonistien kuin ADP: n aiheuttama verihiutaleiden aggregaatio estyy myös estämällä verihiutaleiden aktivaation monistumista vapautuneen ADP: n vuoksi.
Koska aktiivinen metaboliitti muodostuu CYP450 -entsyymien vaikutuksesta, joista osa on polymorfisia tai joita muut lääkkeet estävät, kaikilla potilailla ei ole riittävästi verihiutaleiden estoa.
Farmakodynaamiset ominaisuudet
Toistuvat 75 mg: n vuorokausiannokset antoivat merkittävän ADP: n aiheuttaman verihiutaleiden aggregaation esteen ensimmäisestä päivästä lähtien; esto lisääntyi asteittain, kunnes vakiintui kolmen ja seitsemännen päivän välillä. Tässä vakaan tilan keskimääräinen inhibitiotaso, joka havaittiin annoksella 75 mg vuorokaudessa, vaihteli välillä 40-60%. Verihiutaleiden aggregaatio ja verenvuotoaika palasivat vähitellen lähtötasolle, yleensä 5 päivän kuluessa hoidon lopettamisesta.
Kliininen teho ja turvallisuus
Klopidogreelin turvallisuutta ja tehoa arvioitiin viidessä kaksoissokkotutkimuksessa, joihin osallistui yli 88 000 potilasta: CAPRIE-tutkimus, jossa verrattiin klopidogreelia ja ASA: ta, ja CURE-, CLARITY-, COMMIT- ja ACTIVE-A-vertailututkimukset. Klopidogreelin ja lumelääkkeen välillä yhdessä ASA: n ja muiden tavanomaisten hoitojen kanssa.
Äskettäinen sydäninfarkti (MI), äskettäinen aivohalvaus tai dokumentoitu perifeerinen valtimotauti
CAPRIE -tutkimukseen osallistui 19 185 potilasta, joilla oli aterotromboosi, joka ilmeni äskettäisestä sydäninfarktista (
Klopidogreeli vähensi merkittävästi uusien iskeemisten tapahtumien (sydäninfarktin, iskeemisen aivohalvauksen ja verisuonikuoleman yhdistetty "päätepiste") ilmaantuvuutta ASA: hon verrattuna. (suhteellisen riskin pieneneminen (RRR) 8,7%, [95%: n luottamusväli: 0,2--16,4]; p = 0,045), joka vastaa 10: tä 2 vuoden ajan hoidettua potilasta kohti 10 lisäpotilasta [luottamusväli: 0--20] estää uusia iskeemisiä tapahtumia. Kokonaiskuolleisuuden analyysi toissijaisena päätetapahtumana ei osoittanut merkittävää eroa klopidogreelin (5,8%) ja ASA: n (6,0%) välillä.
"Alaryhmäanalyysissä, joka tehtiin patologiaa (sydäninfarkti, iskeeminen aivohalvaus ja perifeerinen valtimotauti) varten, hyöty näytti olevan johdonmukaisempi (saavuttaen tilastollisen merkitsevyyden p = 0,003) potilailla, joilla oli perifeerinen valtimotauti (erityisesti niillä, joilla on ollut sydäninfarkti) (RRR = 23,7%; CI: 8,9--36,2) ja vähemmän johdonmukainen (ei merkittävästi erilainen kuin ASA) aivohalvauspotilailla (RRR = 7,3%; CI: -5,7 - 18,7 [p = 0,258]). osallistui tutkimukseen pelkästään äskettäisen sydäninfarktin perusteella, klopidogreeli oli numeerisesti pienempi, mutta ei tilastollisesti erilainen kuin ASA (RRR = - 4,0%; CI: - 22,5 - 11,7 [p = 0,639]) Lisäksi alaryhmäanalyysi iän mukaan klopidogreelin hyöty yli 75 -vuotiailla potilailla oli pienempi kuin ≤75 -vuotiailla potilailla.
Koska CAPRIE -tutkimusta ei ole suunniteltu arvioimaan tehokkuutta yksittäisissä alaryhmissä, on epäselvää, ovatko erot suhteellisessa riskin vähenemisessä eri kelpoisuusolosuhteissa todellisia vai johtuvatko sattumasta.
Akuutti sepelvaltimo-oireyhtymä
CURE -tutkimus tehtiin 12 562 potilaalla, joilla oli akuutti sepelvaltimo -oireyhtymä ilman ST -segmentin kohoamista (epästabiili angina pectoris tai sydäninfarkti ilman Q -aaltoja), joiden viimeisin rintakipujakso tai iskemiaa vastaavat oireet alkoivat 24 tunnin aikana. Potilailta vaadittiin joko EKG -muutoksia, jotka vastasivat uutta iskemiaa tai kohonneita sydänentsyymejä tai troponiini I- tai T -arvoa vähintään 2 kertaa ULN -arvo. Potilaat satunnaistettiin saamaan klopidogreelihoitoa (300 mg: n kyllästysannos, jota seurasi 75 mg / vrk, N = 6259) tai lumelääkettä (N = 6303), molemmat yhdessä ASA: n (75--325 mg kerran vuorokaudessa) ja muiden tavanomaisten hoitojen kanssa Potilaita hoidettiin enintään vuoden ajan.CURE-tutkimuksessa 823 potilasta (6,6%) sai samanaikaisesti GPIIb / IIIa -reseptoriantagonistien hoito. Hepariinia annettiin yli 90%: lla potilaista ja suhteellista Samanaikainen hepariinihoito ei vaikuttanut merkittävästi klopidogreelin ja lumelääkkeen välillä.
Ensisijaisen päätetapahtuman (sydän- ja verisuonikuolema, sydäninfarkti tai aivohalvaus) kokeneiden potilaiden määrä oli 582 (9,3%) klopidogreeliryhmässä ja 719 (11,4%) lumelääkeryhmässä. Suhteellinen riski pieneni 20%(95%) Luottamusväli 10% - 28%; p = 0,00009) klopidogreeliryhmässä (17%: n suhteellinen riski pieneni, kun potilaita hoidettiin konservatiivisesti, 29%, kun heille tehtiin perkutaaninen transluminaalinen sepelvaltimoplastia (PTCA) stentin kanssa tai ilman ja 10% sepelvaltimon ohitusvaiheessa) siirtyminen (CABG) Uudet sydän- ja verisuonitapahtumat (ensisijainen päätetapahtuma) estettiin vähentämällä suhteellista riskiä 22% (luottamusväli: 8,6--33,4), 32% (luottamusväli: 12,8--46,4), 4% (luottamusväli: -26,9--26,7), 6% (luottamusväli: -33,5--34,3) ja 14% (luottamusväli: -31,6--44,2) tutkimusvälien aikana 0-1, 1-3, 3-6, 6-9 ja 9-12 kuukautta, vastaavasti 3 kuukauden hoidon lisäksi os Klopidogreeli + ASA -ryhmässä annosteltava annos ei lisääntynyt entisestään, kun verenvuotoriski säilyi (ks. kohta 4.4).
Klopidogreelin käyttö CURE -hoitoon liittyi trombolyyttisen hoidon (RRR = 43,3%; CI: 24,3% - 57,5%) ja GPIIb / IIIa -estäjien (RRR = 18, 2%; CI: 6,5%, 28,3) tarpeen vähenemiseen. %).
Potilaita, joilla oli ensisijainen päätetapahtuma (kardiovaskulaarinen kuolema, sydäninfarkti, aivohalvaus tai tulenkestävä iskemia), oli 1035 (16,5%) klopidogreeliryhmässä ja 1187 (18,8%) lumelääkeryhmässä, ja suhteellinen riski pieneni 14 % (95%: n luottamusväli 6% - 21%, p = 0,0005) klopidogreeliryhmässä.Tämä hyöty johtui pääasiassa sydäninfarktin ilmaantuvuuden tilastollisesti merkitsevästä vähenemisestä [287 (4,6%) klopidogreeliryhmässä ja 363 (5,8%) lumelääkeryhmässä]. Epävakaan angina pectoriksen sairaalahoitoon ei ollut vaikutusta.
Eri ominaisuuksilla (esim. Epästabiili angina pectoris tai sydäninfarkti ilman Q -aaltoja, matala tai korkea riskitaso, diabetes, revaskularisaation tarve, ikä, sukupuoli jne.) Eri populaatioissa saatujen tulosten havaittiin olevan yhdenmukaisia ensisijaisen Erityisesti post-hoc -analyysissä, jossa oli mukana 2172 potilasta (17 % CURE-tutkimuksen koko väestöstä), joille oli tehty stentti (Stent-CURE), tiedot osoittivat merkittävän 26,2 %: n RRR: n klopidogreelin hyväksi lumelääkkeeseen verrattuna ensisijainen päätetapahtuma (sydän- ja verisuonikuolema, sydäninfarkti, aivohalvaus) ja merkittävä 23,9%: n RRR toisella ensisijaisella päätetapahtumalla (sydän- ja verisuonikuolema, sydäninfarkti, aivohalvaus tai iskemia) Lisäksi klopidogreelin turvallisuusprofiili tässä Potilaiden alaryhmä ei paljastanut mitään erityisiä ongelmia, joten tämän alaryhmän tulokset ovat linjassa kokonaistulosten kanssa. ssivi tutkimuksesta.
Klopidogreelin havaittu hyöty ei ollut riippuvainen muiden akuuttien ja pitkäaikaisten sydän- ja verisuoniterapioiden (kuten hepariini / LMWH, glykoproteiini IIb / IIIa -antagonistit, lipidipitoisuutta alentavat lääkkeet, beetasalpaajat ja ACE: n estäjät) käytöstä. Klopidogreelin teho oli riippumatta ASA-annoksesta (75--325 mg kerran vuorokaudessa).
Potilailla, joilla oli akuutti ST-segmentin kohonnut MI, klopidogreelin turvallisuutta ja tehoa arvioitiin kahdessa satunnaistetussa, kaksoissokkoutetussa, lumekontrolloidussa tutkimuksessa, CLARITY ja COMMIT.
CLARITY-tutkimukseen osallistui 3491 potilasta, jotka esiintyivät 12 tunnin kuluessa ST-segmentin kohonneesta MI: stä ja olivat ehdokkaita trombolyyttiseen hoitoon. Potilaat saivat klopidogreelia (300 mg: n aloitusannos, jota seurasi 75 mg / vrk)., N = 1752) tai lumelääkettä (n = 1739), sekä yhdistelmänä ASA: n (150--325 mg: n aloitusannos, jota seurasi 75--162 mg / vrk), fibrinolyyttisen lääkkeen ja tarvittaessa hepariinin kanssa. havaittiin 30 päivän ajan. Ensisijainen päätetapahtuma oli jos esiintyy jokin seuraavista tapahtumista: infarktiin liittyvä valtimon tukos, joka havaitaan ennen purkausta tehdyssä angiografiassa, tai kuolema tai sydäninfarktin uusiutuminen ennen sepelvaltimoiden angiografiaa. Potilailla, joille ei tehty sepelvaltimoiden angiografiaa, ensisijainen päätetapahtuma oli kuolema tai MI päiväksi 8 tai sairaalahoitoon mennessä Potilaspopulaatioon kuului 19,7% naisia ja 29,2% potilaista ≥ 65 -vuotiaat yhteisöt. Kaiken kaikkiaan 99,7% potilaista sai fibrinolyyttejä (spesifinen fibriini: 68,7%, epäspesifinen fibriini: 31,1%), 89,5% hepariinia, 78,7% beetasalpaajia, 54,7% ACE: n estäjiä ja 63% statiineja.
Ensisijaisen päätetapahtuman ilmaantuvuus oli 15 prosenttia (15,0%) klopidogreeliryhmän potilaista ja 21,7% lumelääkeryhmän potilaista, absoluuttinen väheneminen 6,7% ja riski pieneni 36% klopidogreelin eduksi (95%) CI: 24, 47%; sydänkohtaukseen liittyvät parterit.
COMMIT -tutkimukseen, jossa oli 2x2 tekijärakennetta, osallistui 45 852 potilasta, jotka esiintyivät 24 tunnin kuluessa epäillyistä MI -oireista ja tukivat EKG -poikkeavuuksia (esim. ST -segmentin kohoaminen, ST -segmentin lasku tai tukos). Vasen haara). Potilaat saivat klopidogreelia (75 mg / vrk, n = 22,961) tai lumelääkettä (n = 22,891) yhdessä ASA: n (162 mg / vrk) kanssa 28 päivän ajan tai sairaalaan kotiuttamiseen saakka. ensimmäinen sydänkohtaus, aivohalvaus tai kuolema.Väestöön kuului 27,8% naisia, 58,4% ≥ 60-vuotiaita potilaita (26% ≥ 70-vuotiaita) ja 54,5% potilaista sai fibrinolyyttejä.
Klopidogreeli pienensi merkittävästi suhteellista kuolemanriskiä mistä tahansa syystä 7% (p = 0,029) ja suhteellista riskiä sydänkohtauksen, aivohalvauksen tai kuoleman yhdistelmästä 9% (p = 0,002), absoluuttinen väheneminen 0,5 % ja 0,9%. Tämä hyöty oli yhdenmukainen iän, sukupuolen ja fibrinolyyttisten aineiden käytön tai muun kanssa, ja se nähtiin jo ensimmäisten 24 tunnin aikana.
Eteisvärinä
ACTIVE-W- ja ACTIVE-A-tutkimukset, jotka ovat erillisiä ACTIVE-ohjelman tutkimuksia, sisälsivät eteisvärinää (AF) sairastavia potilaita, joilla oli vähintään yksi verisuonitapahtumien riskitekijä. Ilmoittautumiskriteerien perusteella lääkärit sisälsivät potilaita ACTIVE-W-tutkimukseen, jos he olivat oikeutettuja hoitoon K-vitamiiniantagonisteilla (kuten varfariinilla). ACTIVE-A-tutkimukseen osallistui potilaita, jotka eivät voineet saada AVK-hoitoa, koska he eivät pystyneet tai eivät halunneet saada hoitoa.
ACTIVE-W-tutkimus osoitti, että antikoagulanttihoito K-vitamiiniantagonisteilla oli tehokkaampi kuin klopidogreeli- ja ASA-hoito.
ACTIVE-A (n = 7554) on monikeskustutkimus, satunnaistettu, kaksoissokkoutettu, lumekontrolloitu tutkimus, jossa verrataan klopidogreelia 75 mg / vrk + ASA (N = 3772) lumelääke + ASA (N = 3782). Suositeltu ASA -annos vaihteli 75-100 mg / vrk. Potilaita hoidettiin jopa 5 vuoden ajan.
ACTIVE -ohjelmaan satunnaistetuilta potilailta vaadittiin dokumentoitu AF, esim. Pysyvä AF tai vähintään 2 jaksottaista AF -jaksoa, jotka olivat tapahtuneet viimeisten 6 kuukauden aikana ja joilla on oltava vähintään yksi seuraavista riskitekijöistä:
• ikä ≥ 75 vuotta tai
• ikä 55–74 vuotta e
- lääkehoitoa vaativa diabetes mellitus o
- aikaisemmin dokumentoitu MI tai dokumentoitu sepelvaltimotauti;
• hoidetaan systeemisen verenpaineen vuoksi;
• aikaisempi aivohalvaus, ohimenevä iskeeminen hyökkäys (TIA) tai muu kuin keskushermoston systeeminen embolia;
• vasemman kammion toimintahäiriö ja vasemman kammion ejektiofraktio
• dokumentoitu perifeerinen obliteratiivinen arteriopatia.
Keskimääräinen CHADS2-pistemäärä oli 2,0 (vaihteluväli 0-6).
Tärkeimmät poissulkukriteerit potilaille olivat peptinen haava, joka on dokumentoitu edellisen 6 kuukauden aikana; aikaisempi aivojen sisäinen verenvuoto; merkittävä trombosytopenia (verihiutaleiden määrä)
Seitsemänkymmentäkolme prosenttia (73%) ACTIVE-A-tutkimukseen osallistuneista potilaista oli kelvottomia ottamaan AVK: ta lääketieteellisen arvioinnin jälkeen, kyvyttömyys noudattaa INR (International Normalized Ratio) -seurantaa, alttius pudota tai kärsiä traumapäästä tai erityinen verenvuoto 26%: lla potilaista lääkärin päätös perustui potilaan haluttomuuteen ottaa VKA.
41,8% tutkittavista oli naisia. Keski -ikä oli 71 vuotta, 41,6% potilaista oli ≥ 75 -vuotiaita. Kaiken kaikkiaan 23% potilaista sai rytmihäiriölääkkeitä, 52,1% beetasalpaajia, 54,6% ACE: n estäjiä ja 25% statiineja.
Ensisijaisen päätetapahtuman (aika ensimmäiseen aivohalvaukseen, sydäninfarkti, ei-keskushermoston systeeminen embolia tai verisuonikuolema) saavuttaneiden potilaiden määrä oli 832 potilasta (22,1%) klopidogreeli + ASA-ryhmässä ja 924 potilasta (24,4%) lumelääkettä + ryhmässä (suhteellinen riskin väheneminen 11,1%; 95%: n luottamusväli 2,4%-19,1%; p = 0,013), lähinnä suuren vähenemisen vuoksi, esiintyi 296 potilaalla (7,8%), jotka saivat klopidogreelia + ASA: ta, ja 408 potilaalla (10,8%) lumelääke + ASA (suhteellinen riski pieneni 28,4%; 95% CI, 16,8% -38,3%; p = 0,00001).
Pediatriset potilaat
Lisäannostutkimuksessa, johon osallistui 86 vastasyntynyttä tai alle 24 kuukauden ikäistä pikkulapsia, joilla oli tromboosiriski (PICOLO), klopidogreelia arvioitiin peräkkäisillä annoksilla 0,01, 0,1 ja 0,2 mg / kg vastasyntyneillä ja imeväisillä ja 0,15 mg / kg vain vastasyntyneillä. Annos 0,2 mg / kg saavutti keskimäärin 49,3%: n esto (5 mcM ADP: n aiheuttama verihiutaleiden aggregaatio), mikä on verrattavissa Plavixia 75 mg / vrk käyttävien aikuisten vastaavaan. Satunnaistetussa tutkimuksessa kaksoissokkotutkimusryhmä (CLARINET) 906 lapsipotilasta (vastasyntynyttä ja imeväistä), joilla oli heikentynyt syanoottinen synnynnäinen sydänsairaus ja systeeminen keuhkovaltimon shuntti, satunnaistettiin saamaan klopidogreelia 0,2 mg / kg (n = 467) tai lumelääkettä (n = 439) ja samanaikaista taustahoitoa Keskimääräinen aika palliatiivisesta shuntin istutuksesta ensimmäisen tutkimuslääkkeen antoon oli 20 päivää. Noin 88% potilaista sai samanaikaisesti ASA: ta (1--23 mg / kg / vrk).Ryhmien välillä ei ollut merkittävää eroa yhdistetyssä ensisijaisessa päätetapahtumassa, joka oli kuolema, shunttitromboosi tai siihen liittyvä sydämen interventio ennen 120 päivän ikää tromboottiseksi pidetyn tapahtuman jälkeen (89 [19,1%] klopidogreeliryhmässä ja 90 [ 20,5%] lumelääkeryhmässä) (ks. Kohta 4.2). Verenvuoto oli yleisimmin raportoitu haittavaikutus sekä klopidogreeli- että lumelääkeryhmissä, mutta verenvuotojen määrässä ei ollut merkittävää eroa ryhmien välillä. yksi vuosi täyttänyt sai klopidogreelia enintään 18 kuukauden ikään asti.
CLARINET- ja PICOLO -tutkimukset tehtiin käyttämällä valmistettua klopidogreeliliuosta. Suhteellisen biologisen hyötyosuuden tutkimuksessa aikuisilla klopidogreelivalmiste imeytyi verrattavissa olevaan asteeseen ja hieman nopeammin tärkeimpään verenkierrossa (inaktiiviseen) metaboliittiin kuin lisensoitu tabletti.
05.2 Farmakokineettiset ominaisuudet
Imeytyminen
Kliopidogreeli imeytyy nopeasti kerta -annoksen ja toistuvien 75 mg: n vuorokausiannosten jälkeen. Lääkkeen huippupitoisuudet plasmassa (noin 2,2-2,5 ng / ml 75 mg: n kerta-annoksen jälkeen) ilmenevät noin 45 minuuttia annon jälkeen. Imeytyminen on vähintään 50% perustuu klopidogreelin metaboliittien erittymiseen virtsaan.
Jakelu
Vitrtai klopidogreeli ja sen tärkein (inaktiivinen) metaboliitti sitoutuvat palautuvasti ihmisen plasman proteiineihin (98% ja 94%). Sidos ei ole kyllästettävä in vitro laajalla pitoisuusalueella.
Biotransformaatio
Klopidogreeli metaboloituu laajasti maksassa. In vitro Ja in vivoKlopidogreeli metaboloituu kahdella tärkeällä metaboliareitillä: yksi esteraasi välittää hydrolyysin inaktiiviseksi karboksyylihappojohdannaiseksi (85% kiertävistä metaboliiteista) ja toinen useiden P450-sytokromien välityksellä. -klopidogreeli Myöhempi 2-oksoklopidogreelin välimetaboliitin muuntaminen johtaa aktiivisen metaboliitin, klopidogreelin tiolijohdannaisen, muodostumiseen. In vitro tätä metaboliareittiä välittävät CYP3A4, CYP2C19, CYP1A2, CYP2B6. Aktiivinen tiolimetaboliitti, joka eristettiin vitrtai se sitoutuu nopeasti ja peruuttamattomasti verihiutaleiden reseptoreihin, mikä estää verihiutaleiden aggregaation.
Yksittäisen 300 mg: n kyllästysannoksen klopidogreelin annon jälkeen aktiivisen metaboliitin Cmax oli kaksi kertaa korkeampi kuin 75 mg ylläpitoannoksen antamisen jälkeen 4 päivän ajan. Cmax havaitaan noin 30-60 minuuttia annon jälkeen.
Eliminaatio
Ihmisillä suun kautta otetun 14C-leimatun klopidogreeliannoksen jälkeen noin 50% erittyy virtsaan ja noin 46% ulosteeseen 120 tunnin kuluessa annostelusta. 75 mg: n kerta-annoksen jälkeen klopidogreelin puoliintumisaika on noin 6 Kiertävän (inaktiivisen) tärkeimmän metaboliitin eliminaation puoliintumisaika on kahdeksan tuntia sekä kerta- että toistuvan annoksen jälkeen.
Farmakogenetiikka
CYP2C19 osallistuu sekä aktiivisen metaboliitin että 2-oksoklopidogreelin välimetaboliitin muodostumiseen. Klopidogreelin aktiivisen metaboliitin farmakokinetiikka ja verihiutaleiden vastaiset vaikutukset verihiutaleiden aggregaatiomenetelmillä mitattuna ex vivo, vaihtelevat CYP2C19 -genotyypin mukaan. CYP2C19 * 1 -alleeli vastaa täysin toiminnallisesta aineenvaihdunnasta, kun taas CYP2C19 * 2- ja CYP2C19 * 3 -alleelit eivät ole toiminnallisia. Aasialaisilla (99%) .Muut alleelit, jotka liittyvät aineenvaihdunnan puutumiseen tai heikkenemiseen, ovat harvinaisempia ja sisältävät CYP2C19 * 4, * 5, * 6, * 7 ja * 8. Huonolla metaboloijalla on kaksi toimimatonta alleelia CYP2C19: n julkaistut esiintymistiheydet heikoille metaboloijille kuuluvia genotyyppejä on noin 2% valkoihoisilla, 4% mustilla ja 14% kiinalaisilla testeillä potilaan CYP2C19 -genotyypin tunnistamiseksi.
Ristikkäistutkimuksessa, johon osallistui 40 tervettä koehenkilöä, 10 potilasta kustakin neljästä CYP2C19-metaboloivasta ryhmästä (erittäin nopea, laaja, keskitasoinen ja hidas), arvioitiin farmakokineettistä ja verihiutaleiden vastausta käyttämällä 300 mg klopidogreelia, jota seurasi 75 mg / vrk ja 600 mg ja sen jälkeen 150 mg / vrk 5 päivän ajan (vakaa tila) kullekin ryhmälle. Aktiivisten metaboliittialtistusten ja verihiutaleiden aggregaation (PAH) keskimääräisen esteen välillä ei ollut merkittävää eroa erittäin nopeiden, laajojen ja väliaikaisten metaboloijien välillä.Huonoilla metaboloijilla altistuminen aktiiviselle metaboliitille pieneni 63%. Verihiutaleiden vastaus 300 mg / 75 mg: n klopidogreeli -annosohjelman jälkeen väheni huonoilla metaboloijilla, joiden keskimääräinen PAH (5 μM ADP) oli 24% (24 tuntia) ja 37% (päivä 5) verrattuna "PAH: iin, joka havaittiin laajoilla metaboloijilla 39% (24 tuntia) ja 58% (päivä 5) ja se, joka havaittiin metaboloivilla aineilla 37% (24 tuntia) ja 60% (päivä 5).
Kun heikot metaboloijat saivat 600 mg / 150 mg: n annosohjelman, altistus aktiiviselle metaboliitille oli suurempi kuin klopidogreeli 300 mg / 75 mg -ryhmässä. Lisäksi PAH oli 32% (24 tuntia) ja 61% (päivä 5), mikä on korkeampi arvo kuin 300 mg / 75 mg annosohjelmalla hoidetuilla heikkojen metaboloijien ryhmässä ja oli samanlainen kuin muilla ryhmillä CYP2C19 -metaboloijien hoito 300 mg / 75 mg -annosohjelmalla. Kliiniset tutkimukset eivät osoittaneet sopivaa annosta tälle potilasryhmälle.
Yllä olevien tulosten mukaisesti meta-analyysi, joka sisälsi kuusi tutkimusta, joissa oli yhteensä 335 potilasta, jotka saivat klopidogreelia vakaan tilan aikana, osoitti aktiiviselle metaboliitille altistumisen vähenevän 28% väliaikaisilla metaboloijilla ja 72% välitason metaboloijilla. verihiutaleiden aggregaation esto (5 μM ADP) väheni, kun PAH -erot olivat 5,9% ja 21,4% vastaavasti verrattuna laajoihin metaboloijiin.
CYP2C19-genotyypin vaikutusta kliinisiin tuloksiin klopidogreelilla hoidetuilla potilailla ei ole arvioitu prospektiivisissa, satunnaistetuissa, kontrolloiduissa kliinisissä tutkimuksissa.On kuitenkin olemassa useita retrospektiivisiä analyysejä tämän vaikutuksen arvioimiseksi klopidogreelihoitoa saaneilla potilailla, joille on saatu genotyyppituloksia : CURE (n = 2721), CHARISMA (n = 2428), CLARITY-TIMI 28 (N = 227), TRITON-TIMI 38 (N = 1477) ja ACTIVE-A (n = 601), ja useita julkaistuja kohortteja opinnot.
TRITON-TIMI 38 -tutkimuksessa ja kolmessa kohorttitutkimuksessa (Collet, Sibbing, Giusti) yhdistetty potilasryhmä, jolla oli sekä keskinkertaisia että hitaita metaboloijia, ilmoitti sydän- ja verisuonitapahtumien (kuolema, sydäninfarkti ja aivohalvaus) tai stentitromboosin ilmaantuvuuden verrattuna. laajoille metaboloijille.
CHARISMA -tutkimuksessa ja kohorttitutkimuksessa (Simon) tapahtumien ilmaantuvuutta havaittiin vain heikoilla metaboloijilla verrattuna laajoihin metaboloijiin.
Tutkimuksissa CURE, CLARITY, ACTIVE-A ja yhdessä kohorttitutkimuksessa (Trenk) tapahtumien ilmaantuvuuden lisääntymistä ei havaittu metaboloijan tilan perusteella.
Mikään näistä analyyseistä ei ollut riittävän kokoinen havaitsemaan eroja tuloksissa huonoissa metaboloijissa.
Erityisryhmät
Klopidogreelin aktiivisen metaboliitin farmakokinetiikkaa ei tunneta näissä erityisryhmissä.
Munuaisten vajaatoiminta
Toistuvien 75 mg / vrk klopidogreeliannosten jälkeen vaikeaa munuaisten vajaatoimintaa sairastavilla (kreatiniinipuhdistuma 5–15 ml / min) ADP: n aiheuttaman verihiutaleiden aggregaation esto oli pienempi (25%) kuin terveillä koehenkilöillä. verenvuotoaika pidentyi samalla tavalla kuin terveillä koehenkilöillä, jotka saivat klopidogreelia 75 mg / vrk. Lisäksi kliininen siedettävyys oli hyvä kaikilla potilailla.
Maksan vajaatoiminta
Toistuvien klopidogreelin 75 mg / vrk annosten jälkeen 10 päivän ajan vaikeaa maksan vajaatoimintaa sairastavilla potilailla ADP: n aiheuttaman verihiutaleiden aggregaation esto oli samanlainen kuin terveillä koehenkilöillä.
Verenvuodon keskimääräinen pidentyminen oli myös samanlainen näiden kahden ryhmän välillä.
Rotu
CYP2C19 -alleelien esiintyvyys, joka johtaa CYP2C19: n metabolisen aktiivisuuden heikkenemiseen ja välituotteeseen, vaihtelee rodun / etnisyyden mukaan (ks.Farmakogenetiikka). Kirjallisuudesta on saatavilla vain vähän tietoa Aasian populaatioista tämän CYP: n genotyypityksen kliinisen vaikutuksen arvioimiseksi kliinisiin tapahtumiin.
05.3 Prekliiniset tiedot turvallisuudesta
Rotilla ja paviaaneilla tehdyissä ei-kliinisissä tutkimuksissa maksan parametrien muuttaminen oli yleisimmin havaittu vaikutus. Tämä tapahtui annoksilla, jotka olivat vähintään 25 kertaa suurempia kuin vastaava kliininen 75 mg / vrk annos ihmisille, ja se oli seurausta vaikutus maksan metabolisiin entsyymeihin. Klopidogreelin vaikutusta maksan metabolisiin entsyymeihin ei havaittu ihmisillä terapeuttisina annoksina.
Hyvin suurilla annoksilla on raportoitu huonoa mahalaukun siedettävyyttä (gastriitti, mahalaukun eroosio ja / tai oksentelu) rotilla ja paviaaneilla.
Syöpää aiheuttavaa vaikutusta ei havaittu klopidogreelin annon jälkeen hiirille 78 viikon ajan ja rotille 104 viikon ajan annokseen 77 mg / kg / vrk (mikä vastaa vähintään 25 kertaa altistusta, joka esiintyy kliinisellä annoksella 75 mg / vrk) ihmisillä).
Klopidogreelia arvioitiin sarjassa genotoksisuustutkimuksia vuonna in vitro ja sisään vivtai se ei osoittanut genotoksista aktiivisuutta.
Klopidogreeli ei osoittanut mitään vaikutusta uros- ja naarasrottien hedelmällisyyteen eikä teratogeenisiä vaikutuksia rotalla tai kanilla. Kun klopidogreeli annettiin imettäville rotille, se viivästytti jälkeläisten kehittymistä. Leimatulla klopidogreelilla tehdyt erityiset farmakokineettiset tutkimukset ovat osoittaneet, että pääyhdiste ja sen metaboliitit erittyvät maitoon. Näin ollen suoraa (lievää myrkyllisyyttä) tai epäsuoraa (huono maku) vaikutusta ei voida sulkea pois.
06.0 FARMASEUTTISET TIEDOT
06.1 Apuaineet
Ydin:
mannitoli (E421);
makrogoli 6000;
mikrokiteinen selluloosa;
hydrattu risiiniöljy;
vähän substituoitu hydroksipropyyliselluloosa.
Pinnoite:
hypromelloosi (E464);
laktoosimonohydraatti;
triasetiini (E1518);
titaanidioksidi (E171);
punainen rautaoksidi (E172).
Kiillotusaine:
karnaubavaha.
06.2 Yhteensopimattomuus
Ei oleellinen.
06.3 Voimassaoloaika
3 vuotta.
06.4 Säilytys
Säilytä alle 30 ° C PVC / PVDC / alumiiniläpipainopakkauksissa.
Tämä lääkevalmiste ei vaadi erityisiä säilytysolosuhteita alumiini / alumiiniläpipainopakkauksissa.
06.5 Välipakkauksen luonne ja pakkauksen sisältö
PVC / PVDC / alumiiniläpipainopakkaukset tai alumiini / alumiiniläpipainopakkaukset pahvilaatikossa, joka sisältää 7, 14, 28, 30, 84, 90 ja 100 kalvopäällysteistä tablettia.
PVC / PVDC / alumiiniläpipainopakkaukset tai alumiinirei'itetyt kerta-annospakkaukset pahvilaatikossa, jotka sisältävät 50 x 1 kalvopäällysteistä tablettia.
Kaikkia pakkauskokoja ei välttämättä ole myynnissä.
06.6 Käyttö- ja käsittelyohjeet
Käyttämätön lääke ja tästä lääkkeestä peräisin oleva jäte on hävitettävä paikallisten määräysten mukaisesti.
07.0 MYYNTILUVAN HALTIJA
Sanofi Clir SNC
54, rue La Boétie
F-75008 Pariisi
Ranska
08.0 MYYNTILUVAN NUMERO
EU / 1/98/069 / 001a - Pakkaus, jossa 28 kalvopäällysteistä tablettia PVC / PVDC / Al -läpipainopakkauksessa
034128013
EU / 1/98/069 / 001b - Pakkaus, jossa 28 kalvopäällysteistä tablettia alumiini / alumiiniläpipainopakkauksessa
EU / 1/98/069 / 002a - 50 x 1 kalvopäällysteisen tabletin pakkaus PVC / PVDC / Al -läpipainopakkauksessa
034128025
EU / 1/98/069 / 002b - 50 x 1 kalvopäällysteisen tabletin pakkaus alumiini / alumiiniläpipainopakkauksessa
EU / 1/98/069 / 003a - Pakkaus, jossa 84 kalvopäällysteistä tablettia PVC / PVDC / Al -läpipainopakkauksessa
034128037
EU / 1/98/069 / 003b - Pakkaus, jossa 84 kalvopäällysteistä tablettia alumiini / alumiiniläpipainopakkauksessa
EU / 1/98/069 / 004a - Pakkaus, jossa 100 kalvopäällysteistä tablettia PVC / PVDC / Al -läpipainopakkauksessa
EU / 1/98/069 / 004b - Pakkaus, jossa 100 kalvopäällysteistä tablettia alumiini / alumiiniläpipainopakkauksessa
EU / 1/98/069 / 005a - Pakkaus, jossa 30 kalvopäällysteistä tablettia PVC / PVDC / Al -läpipainopakkauksessa
EU / 1/98/069 / 005b - Pakkaus, jossa 30 kalvopäällysteistä tablettia alumiini / alumiiniläpipainopakkauksessa
EU / 1/98/069 / 006a - Pakkaus, jossa 90 kalvopäällysteistä tablettia PVC / PVDC / Al -läpipainopakkauksessa
EU / 1/98/069 / 006b - Pakkaus, jossa 90 kalvopäällysteistä tablettia alumiini / alumiiniläpipainopakkauksessa
EU / 1/98/069 / 007a - Pakkaus, jossa 14 kalvopäällysteistä tablettia PVC / PVDC / Al -läpipainopakkauksessa
EU / 1/98/069 / 007b - Pakkaus, jossa 14 kalvopäällysteistä tablettia alumiini / alumiiniläpipainopakkauksessa
EU / 1/98/069 / 011a - Pakkaus, jossa 7 kalvopäällysteistä tablettia PVC / PVDC / Al -läpipainopakkauksessa
EU / 1/98/069 / 011b - Pakkaus, jossa 7 kalvopäällysteistä tablettia alumiini / alumiiniläpipainopakkauksessa
09.0 MYYNTILUVAN TAI UUDISTAMISPÄIVÄMÄÄRÄ
Myyntiluvan myöntämisen päivämäärä: 15. heinäkuuta 1998
Viimeisimmän uudistamisen päivämäärä: 15. heinäkuuta 2008
10.0 TEKSTIN MUUTTAMISPÄIVÄMÄÄRÄ
D.CCE lokakuussa 2015