Vaikuttavat aineet: Dronedarone
MULTAQ 400 mg kalvopäällysteiset tabletit
Miksi Multaqia käytetään? Mitä varten se on?
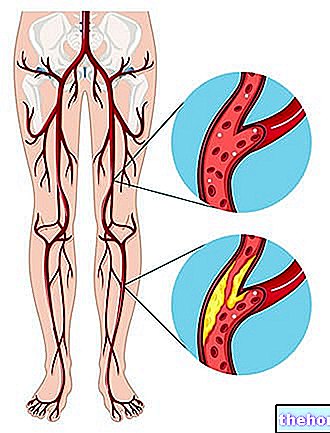
MULTAQ sisältää vaikuttavana aineena dronedaronia. Se kuuluu rytmihäiriölääkkeisiin, jotka auttavat säätelemään sydämen sykettä.
MULTAQ -valmistetta käytetään, jos sinulla on sykehäiriö, kuten epäsäännöllinen rytmihäiriö (eteisvärinä) ja kardioversio -hoito on saanut sydämen sykkeen normaaliksi.
MULTAQ estää epäsäännöllisen sydämenlyönnin ongelman uusiutumisen. Lääkäri harkitsee kaikkia käytettävissä olevia hoitovaihtoehtoja ennen MULTAQ -lääkkeen määräämistä.
Vasta -aiheet Milloin Multaqia ei tule käyttää
Älä ota MULTAQia:
- jos olet allerginen dronedaronille tai tämän lääkkeen jollekin muulle aineelle
- jos sinulla on sydämen hermoihin vaikuttava ongelma (sydämen lohko). Sydämesi voi lyödä hyvin hitaasti tai tunnet huimausta. Jos sinulle on istutettu sydämentahdistin tällaista ongelmaa varten, voit ottaa MULTAQin
- jos sinulla on hyvin hidas syke (alle 50 lyöntiä minuutissa),
- ja EKG (elektrokardiogrammi) osoitti sydänongelman nimeltä "venytetty QTc -aika" (tämä väli on yli 500 millisekuntia)
- jos sinulla on eräänlainen eteisvärinä (AF), jota kutsutaan pysyväksi eteisvärinäksi. Pysyvässä eteisvärinässä AF on ollut läsnä pitkään (vähintään 6 kuukautta) ja lääkäri on päättänyt olla palauttamatta sydämen rytmiä normaaliin eteisrytmiin kardioversiolla
- jos sinulla on tai on ollut ongelma, joka estää sydäntäsi pumppaamasta verta kehosi ympärille niin kuin pitäisi (tila, jota kutsutaan sydämen vajaatoiminnaksi). Saatat kokea jalkojen tai jalkojen turvotusta, hengitysvaikeuksia makuulla tai nukkumassa tai hengenahdistusta liikkuessasi
- jos veren prosenttiosuus, joka pumppaa sydämen joka kerta, kun se supistuu, on liian alhainen (vasemman kammion toimintahäiriö)
- jos olet aiemmin käyttänyt amiodaronia (toinen rytmihäiriölääke) ja sinulla on ollut keuhko- tai maksavaivoja
- jos käytät lääkkeitä "infektioon (mukaan lukien sieni -infektiot tai AIDS)", allergioihin, sykehäiriöihin, masennukseen tai elinsiirron jälkeen (katso "Muut lääkkeet ja MULTAQ" alla. antaa sinulle lisätietoja lääkkeitä, joita et voi käyttää yhdessä MULTAQin kanssa)
- jos sinulla on vaikea maksaongelma
- jos sinulla on vaikea munuaisongelma
- jos käytät dabigatraania (ks. kohta "Muut lääkevalmisteet ja MULTAQ").
Jos jokin edellä mainituista koskee sinua, älä ota MULTAQia.
Käyttöä koskevat varotoimet Mitä sinun on tiedettävä, ennen kuin otat Multaqia
Keskustele lääkärin tai apteekkihenkilökunnan kanssa ennen kuin otat MUTAQ -valmistetta, jos:
- sinulla on ongelma, joka aiheuttaa alhaisia veren kalium- tai magnesiumpitoisuuksia. Tämä ongelma on korjattava ennen MULTAQ -hoidon aloittamista
- on yli 75 -vuotias
- sinulla on sairaus, jossa sepelvaltimoita, jotka toimittavat verta sydämeen, kovettuvat ja kutistuvat leveästi (sepelvaltimotauti).
Kerro lääkärillesi, jos saat MULTAQ -hoitoa
- eteisvärinä muuttuu pysyväksi MULTAQ -hoidon aikana. Sinun on lopetettava MULTAQin käyttö
- kärsit jalkojen tai jalkojen turvotuksesta, hengitysvaikeuksista makuulla tai nukkumassa, hengenahdistuksesta liikkuessa tai painonnoususta (jotka ovat merkkejä ja oireita sydämen vajaatoiminnasta)
- kerro heti lääkärille, jos sinulle ilmaantuu jokin näistä maksavaivojen oireista: vatsakipu tai epämukavuus, ruokahaluttomuus, pahoinvointi, oksentelu, ihon tai silmänvalkuaisten keltaisuus (keltaisuus), epätavallinen väri tumma virtsa väsymys (erityisesti muiden edellä kuvattujen oireiden yhteydessä), kutina
- sinulla on hengenahdistus tai kuiva yskä. Kerro lääkärillesi, joka tarkistaa keuhkosi.
Jos jokin edellä mainituista koskee sinua (tai jos olet epävarma), keskustele lääkärin tai apteekkihenkilökunnan kanssa ennen kuin otat MULTAQ -valmistetta.
Sydän-, keuhko- ja verikokeet
Lääkärisi voi tehdä testejä MULTAQ -hoidon aikana terveydentilasi ja lääkkeen tehon tarkistamiseksi.
- Lääkäri voi tarkistaa sydämen sähköisen toiminnan EKG: llä (elektrokardiogrammi).
- Lääkäri määrää verikokeita maksan toiminnan tarkistamiseksi ennen MULTAQ -hoidon aloittamista ja hoidon aikana.
- Jos käytät tiettyjä lääkkeitä, jotka estävät verihyytymiä, kuten varfariinia, lääkäri määrää sinulle INR -nimisen verikokeen, jolla tarkistetaan, toimiiko lääke hyvin
- Lääkäri voi myös tehdä muita verikokeita. Munuaisten toiminnan (veren kreatiniinipitoisuudet) tarkistavien verikokeiden tulokset voivat muuttua MULTAQ -hoidon jälkeen. Lääkärisi ottaa tämän huomioon verikokeita tarkistaessaan ja käyttää toista vertailukohtaa "normaali" veren kreatiniinipitoisuus.
- Lääkärisi saattaa suorittaa keuhkojen kliinisen arvioinnin.
Joissakin tapauksissa voi olla tarpeen lopettaa MULTAQ -hoito.
Kerro verikokeita tarkastelevalle henkilölle, että hän käyttää MULTAQia.
Lapset ja nuoret
MULTAQ -valmistetta ei suositella lapsille ja alle 18 -vuotiaille nuorille.
Yhteisvaikutukset Mitkä lääkkeet tai elintarvikkeet voivat muuttaa Multaqin vaikutusta
Kerro lääkärille tai apteekkihenkilökunnalle, jos parhaillaan käytät, olet äskettäin käyttänyt tai saatat käyttää muita lääkkeitä.
Tilasi mukaan lääkärisi voi suositella verihyytymien muodostumista estävän lääkkeen (antikoagulantin) käyttöä.
MULTAQ ja jotkut muut lääkkeet voivat olla vuorovaikutuksessa keskenään ja aiheuttaa vakavia sivuvaikutuksia. Lääkärisi voi päättää muuttaa muiden käyttämiesi lääkkeiden annosta.
Älä ota mitään seuraavista lääkkeistä yhdessä MULTAQin kanssa:
- muut epäsäännöllisen tai nopean sydämenlyönnin hoitoon käytettävät lääkkeet, kuten flekainamidi, propafenoni, kinidiini, disopyramidi, dofetilidi, sotaloli, amiodaroni
- jotkut sieni -infektioiden hoitoon käytettävät lääkkeet, kuten ketokonatsoli, vorikanotsoli, itrakonatsoli tai posakonatsoli
- jotkut masennuslääkkeet, joita kutsutaan trisyklisiksi masennuslääkkeiksi
- jotkut rauhoittavat lääkkeet, nimeltään fenotiatsiinit
- bepridiili sydänsairauksien aiheuttamaan rintakipuun
- telitromysiini, erytromysiini tai klaritromysiini (infektioiden antibiootit)
- terfenadiini (allergialääke)
- nefatsodoni (masennuslääke)
- sisapridi (lääke ruoan tai hapan nesteen poistamiseen mahasta suuhun)
- ritonaviiri (aids -lääke)
- dabigatraani (lääke verihyytymien estämiseksi).
Kerro lääkärille tai apteekkihenkilökunnalle, jos käytät jotakin seuraavista lääkkeistä:
- muut lääkkeet, joita käytetään korkeaan verenpaineeseen, sydänsairauksien tai muiden sydänongelmien aiheuttamiin rintakipuihin, kuten verapamiili, diltiatseemi, nifedipiini, metoprololi, propranololi tai digoksiini
- jotkut veren kolesterolia alentavat lääkkeet (kuten simvastatiini, lovastatiini, atorvastatiini tai rosuvastatiini)
- jotkut lääkkeet verihyytymien muodostumista vastaan, kuten varfariini
- jotkut epilepsialääkkeet, joita kutsutaan fenobarbitaaliksi, karbamatsepiiniksi tai fenytoiiniksi
- sirolimuusi, takrolimuusi, everolimuusi ja syklosporiini (käytetään elinsiirron jälkeen)
- Mäkikuisma (mäkikuisma) - yrttilääke masennukseen
- rifampisiini - tuberkuloosiin.
MULTAQ ruuan ja juoman kanssa
Älä juo greippimehua MULTAQ -hoidon aikana. Tämä juoma voi lisätä dronedaronipitoisuutta veressäsi ja sivuvaikutusten todennäköisyyttä.
Varoitukset On tärkeää tietää, että:
Raskaus ja imetys
Jos olet raskaana tai imetät, epäilet olevasi raskaana tai jos suunnittelet lapsen hankkimista, kysy lääkäriltä neuvoa ennen tämän lääkkeen käyttöä.
- MULTAQ -valmistetta ei suositella, jos olet raskaana tai epäilet olevasi raskaana.
- Älä ota MULTAQia, jos olet nainen, joka voi saada lapsia etkä käytä tehokasta ehkäisyä.
- Lopeta tablettien käyttö ja ota heti yhteys lääkäriisi, jos tulet raskaaksi MULTAQ -hoidon aikana.
- Jos olet äiti, joka imettää vauvaa, on suositeltavaa neuvotella lääkärisi kanssa ennen kuin otat MULTAQ -valmistetta.
Ajaminen ja koneiden käyttö
MULTAQ ei yleensä vaikuta ajokykyyn tai koneiden käyttökykyyn. Haittavaikutukset, kuten väsymys (jos sellainen on), voivat kuitenkin heikentää kykyäsi ajaa ja käyttää koneita.
MULTAQ sisältää laktoosia
Laktoosi on eräänlainen sokeri. Jos lääkäri on kertonut sinulle, että sinulla on ”intoleranssi tietyntyyppisille sokereille, ota yhteys lääkäriisi ennen tämän lääkkeen ottamista.
Annostus ja käyttötapa Multaqin käyttö: Annostus
MULTAQ -hoito suoritetaan sydänsairauksien hoitoon perehtyneen lääkärin valvonnassa.
Ota tätä lääkettä juuri sen verran kuin lääkäri on määrännyt. Jos olet epävarma, käänny lääkärin tai apteekkihenkilökunnan puoleen.
Jos sinun on vaihdettava amiodaronista (toinen epäsäännöllisen sydämen sykkeen hoitoon käytettävä lääke) MULTAQ -hoitoon, lääkäri käsittelee muutosta varoen.
Kuinka paljon lääkettä otetaan
Tavanomainen annos on yksi 400 mg: n tabletti kahdesti vuorokaudessa. Ota:
- yksi tabletti aamiaisen aikana e
- yksi tabletti illallisen aikana.
Kerro lääkärille tai apteekkihenkilökunnalle, jos lääkkeen vaikutus on mielestäsi liian voimakas tai liian heikko.
Miten tämä lääke otetaan
Niele tabletti kokonaisena juomalla vettä aterian aikana. Tablettia ei saa jakaa yhtä suuriin annoksiin.
Jos unohdat ottaa MULTAQ -valmistetta
Älä ota kaksinkertaista annosta korvataksesi unohtamasi tabletin. Ota seuraava annos kellonaikaan, jolloin tavallisesti otat sen.
Jos lopetat MULTAQin käytön
Älä lopeta tämän lääkkeen käyttöä keskustelematta ensin lääkärin tai apteekkihenkilökunnan kanssa.
Jos sinulla on kysymyksiä tämän lääkkeen käytöstä, käänny lääkärin tai apteekkihenkilökunnan puoleen.
Yliannostus Mitä tehdä, jos olet ottanut liikaa Multaqia
Ota välittömästi yhteys lääkäriisi tai lähimpään ensiapuun tai sairaalaan Ota lääkepakkaus mukaasi.
Sivuvaikutukset Mitkä ovat Multaqin sivuvaikutukset?
Kuten kaikki lääkkeet, tämäkin lääke voi aiheuttaa haittavaikutuksia. Kaikki eivät kuitenkaan niitä saa.
Seuraavia haittavaikutuksia on raportoitu tämän lääkkeen käytön aikana: Kerro heti lääkärille, jos huomaat jonkin seuraavista vakavista haittavaikutuksista - saatat tarvita kiireellistä lääkärin apua
Hyvin yleinen (useammalla kuin yhdellä potilaalla 10: stä)
- sairaus, joka johtuu siitä, että sydän ei pumppaa verta kehon ympärille kunnolla (kuten kongestiivinen sydämen vajaatoiminta). Kliinisissä tutkimuksissa tätä sivuvaikutusta havaittiin yhtä usein MULTAQ -hoitoa saaneilla potilailla ja hoitamattomilla potilailla. Häiriön oireita ovat jalkojen tai jalkojen turvotus, hengitysvaikeudet makuulla tai nukkumassa, hengenahdistus liikkuessa tai painonnousu.
Yleiset (enintään 1 potilaalla 10: stä)
- Ripuli, oksentelu liiallisena, koska se voi johtaa munuaisongelmiin.
- Hidas syke.
Melko harvinaiset (enintään 1 potilaalla 100: sta)
- Keuhkotulehdus (mukaan lukien arpeutuminen ja keuhkojen paksuuntuminen). Oireita ovat hengenahdistus tai tuottamaton yskä.
Harvinaiset (enintään 1 potilaalla tuhannesta)
- Maksavaivat, mukaan lukien hengenvaarallinen maksan vajaatoiminta. Näitä oireita ovat vatsakipu tai epämukavuus, ruokahaluttomuus, pahoinvointi, oksentelu, ihon tai silmänvalkuaisten keltaisuus (keltaisuus), virtsan epänormaali tummuminen, väsymys (erityisesti muiden yllä lueteltujen oireiden yhteydessä) , kutinaa.
- Allergiset reaktiot, mukaan lukien kasvojen, huulten, suun, kielen tai kurkun turvotus.
Muita haittavaikutuksia ovat:
Hyvin yleinen (useammalla kuin yhdellä potilaalla 10: stä)
- muutokset verikokeen tuloksissa: veren kreatiniinipitoisuutesi
- muutokset EKG: ssä (elektrokardiogrammi), jota kutsutaan Bazettin mukaan QTc -ajan pitenemiseksi.
Yleiset (enintään 1 potilaalla 10: stä)
- ruoansulatusongelmat, kuten ripuli, pahoinvointi, oksentelu ja vatsakipu
- väsynyt olo
- iho -ongelmat, kuten ihottuma tai kutina
- muutokset maksan toiminnan tarkistamiseen käytettävien verikokeiden tuloksissa.
Melko harvinaiset (enintään 1 potilaalla 100: sta)
- muut iho -ongelmat, kuten ihon punoitus tai ihottuma (punoitus, kutina, polttaminen tai rakkulat)
- iho herkempi auringolle
- maun muutos.
Harvinaiset (enintään 1 potilaalla tuhannesta)
- maun menetys
- verisuonitulehdus (vaskuliitti, mukaan lukien leukosytoklastinen vaskuliitti).
Sivuvaikutusten ilmoittaminen
Jos havaitset haittavaikutuksia, käänny lääkärin tai apteekkihenkilökunnan puoleen, mukaan lukien mahdolliset haittavaikutukset, joita ei ole mainittu tässä pakkausselosteessa.
Voit ilmoittaa haittavaikutuksista myös suoraan (ks. Yhteystiedot alla).
Ilmoittamalla haittavaikutuksista voit auttaa saamaan enemmän tietoa tämän lääkkeen turvallisuudesta
Vanhentuminen ja säilyttäminen
Ei lasten ulottuville eikä näkyville.
Älä käytä tätä lääkettä läpipainopakkauksessa ja kotelossa mainitun viimeisen käyttöpäivämäärän "EXP" jälkeen. Viimeinen käyttöpäivämäärä viittaa mainitun kuukauden viimeiseen päivään.
Tämä lääke ei vaadi erityisiä säilytysolosuhteita.
Älä käytä tätä lääkettä, jos huomaat näkyviä heikkenemisen merkkejä (ks. Kohta 6 "MULTAQ -valmisteen kuvaus ja pakkauskoot").
Älä heitä lääkkeitä viemäriin tai talousjätteisiin. Kysy apteekista, kuinka heittää pois lääkkeet, joita et enää käytä. Tämä auttaa suojelemaan ympäristöä.
Muita tietoja
Mitä MULTAQ sisältää
- Vaikuttava aine on dronedaroni. Yksi kalvopäällysteinen tabletti sisältää 400 mg dronedaronia (hydrokloridina).
- Muut tabletin ytimen sisältämät aineet ovat: hypromelloosi (E464), maissitärkkelys, krospovidoni (E1202), poloksameeri 407, laktoosimonohydraatti, vedetön kolloidinen piidioksidi, magnesiumstearaatti (E572).
- Tabletin päällysteen muut aineosat ovat: hypromelloosi (E464), makrogoli 6000, titaanidioksidi (E171), karnaubavaha (E903).
Kuvaus MULTAQ -valmisteen ulkonäöstä ja pakkauksen sisällöstä
MULTAQ on valkoinen, soikea, kalvopäällysteinen tabletti (tabletti), jonka toisella puolella on kaksoisaalto ja toisella puolella numero "4142".
MULTAQ-kalvopäällysteiset tabletit toimitetaan läpinäkymättömissä PVC- ja alumiiniläpipainopakkauksissa, joissa on 20, 50, 60 tablettia ja 100 x 1 tabletin pakkauksissa läpinäkymättömissä PVC- ja alumiiniläpipainopakkauksissa.
Kaikkia pakkauskokoja ei välttämättä ole myynnissä.
Alkuperäinen pakkausseloste: AIFA (Italian lääkevirasto). Sisältö julkaistu tammikuussa 2016. Esitetyt tiedot eivät välttämättä ole ajan tasalla.
Jotta saat käyttöösi uusimman version, on suositeltavaa käyttää AIFA: n (Italian Medicines Agency) verkkosivustoa. Vastuuvapauslauseke ja hyödyllistä tietoa.
01.0 LÄÄKEVALMISTEEN NIMI
MULTAQ 400 MG TABLETIT, PÄÄLLYTTYNYT KALVOLLA
02.0 LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS
Yksi tabletti sisältää 400 mg dronedaronia (hydrokloridina).
Apuaineet, joiden vaikutukset tunnetaan:
Yksi tabletti sisältää myös 41,65 mg laktoosia (monohydraattina).
Täydellinen apuaineluettelo, katso kohta 6.1.
03.0 LÄÄKEMUOTO
Kalvopäällysteinen tabletti (tabletti).
Valkoisia, pitkänomaisia tabletteja, joihin on kaiverrettu kaksoisaalto toiselle puolelle ja numero "4142" toiselle puolelle.
04.0 KLIINISET TIEDOT
04.1 Käyttöaiheet
MULTAQ on tarkoitettu sinusrytmin ylläpitämiseen onnistuneen kardioversion jälkeen kliinisesti vakailla aikuispotilailla, joilla on paroksismaalinen tai jatkuva eteisvärinä (AF). Turvallisuusprofiilinsa vuoksi (ks. Kohdat 4.3 ja 4.4) MULTAQia tulisi määrätä vasta sen jälkeen, kun vaihtoehtoiset hoitovaihtoehdot on arvioitu.
MULTAQ -valmistetta ei saa antaa potilaille, joilla on vasemman kammion systolinen toimintahäiriö tai potilaille, joilla on aikaisempi tai nykyinen sydämen vajaatoiminta.
04.2 Annostus ja antotapa
MULTAQ -hoito tulee aloittaa ja seurata vain erikoislääkärin valvonnassa (ks. Kohta 4.4).
MULTAQ -hoito voidaan aloittaa avohoidossa.
Hoito luokan I tai III rytmihäiriölääkkeillä (kuten flekainidi, propafenoni, kinidiini, disopyramidi, dofetilidi, sotaloli, amiodaroni) on lopetettava ennen MULTAQ -hoidon aloittamista.
Optimaalisesta ajasta siirtyä amiodaronista MULTAQiin on vain vähän tietoa. On otettava huomioon, että amiodaronin vaikutus voi kestää pitkään sen lopettamisen jälkeen pitkän puoliintumisajan vuoksi. Jos vaihtoa suunnitellaan, se on tehtävä erikoislääkärin valvonnassa (ks. Kohdat 4.3 ja 5.1).
Annostus
Aikuisilla suositeltu annos on 400 mg kahdesti vuorokaudessa. On suositeltavaa ottaa
• yksi tabletti aamiaisen aikana e
• yksi tabletti illallisen aikana
Greippimehua ei tule ottaa samanaikaisesti MULTAQ -valmisteen kanssa (ks. Kohta 4.5).
Jos annos jää väliin, potilaan on otettava seuraava annos tavalliseen vuorokauden aikaan eikä hänen tule ottaa kaksinkertaista annosta.
Pediatriset potilaat
MULTAQin turvallisuutta ja tehoa alle 18 -vuotiaiden lasten hoidossa ei ole vielä varmistettu.Tietoja ei ole saatavilla.
Eläkeläiset
Lääkevalmisteen teho ja turvallisuus olivat vertailukelpoisia iäkkäillä potilailla, jotka eivät ole kärsineet muista sydän- ja verisuonitaudeista, ja nuoremmilla potilailla. Varovaisuutta on noudatettava potilailla, jotka ovat ≥ 75-vuotiaita, kun samanaikaisia sairauksia esiintyy (ks. Kohdat 4.3, 4.4 ja 5.1) Vaikka plasman altistus iäkkäille naispotilaille oli suurempi terveillä henkilöillä tehdyssä farmakokineettisessä tutkimuksessa, annoksen muuttamista ei pidetä tarpeellisena (ks. Kohdat 5.1 ja 5.2).
Maksan vajaatoiminta
Tietojen puutteen vuoksi MULTAQ on vasta -aiheinen potilaille, joilla on vaikea maksan vajaatoiminta (ks. Kohdat 4.3 ja 4.4). Annosta ei tarvitse muuttaa potilailla, joilla on lievä tai kohtalainen maksan vajaatoiminta (ks. Kohta 5.2).
Munuaisten vajaatoiminta
MULTAQ on vasta -aiheinen potilaille, joilla on vaikea munuaisten vajaatoiminta (kreatiniinipuhdistuma (CrCl))
Antotapa
Suun kautta
Tabletti on nieltävä kokonaisena vesilasillisen kera aterian aikana.
04.3 Vasta -aiheet
• Yliherkkyys vaikuttavalle aineelle tai kohdassa 6.1 mainituille apuaineille.
• Toisen tai kolmannen asteen eteis -kammiokatkos, täydellinen haarautuma, distaalinen lohko, sinusolmun toimintahäiriö, eteisjohtamisvaurio tai sinusolmun sairaus (ellei lääkettä käytetä yhdessä sydämentahdistimen kanssa).
• Bradykardia lyöntiä minuutissa (bpm)
• Pysyvä eteisvärinä (AF: n kesto ≥ 6 kuukautta tai ei tiedossa) ja yritykset palauttaa sinusrytmi, jota lääkäri ei enää pidä mahdollisena
• Epävakaat hemodynaamiset olosuhteet
• Aiempi tai nykyinen sydämen vajaatoiminta tai vasemman kammion toimintahäiriö
• Amiodaronin aiempaan käyttöön liittyvä maksan ja keuhkojen toksisuus
• Voimakkaiden sytokromi P 450 (CYP) 3A4: n estäjien, kuten ketokonatsolin, itrakonatsolin, vorikonatsolin, posakonatsolin, telitromysiinin, klaritromysiinin, nefatsodonin ja ritonaviirin, samanaikainen käyttö (ks. Kohta 4.5)
• Lääkkeet, jotka voivat aiheuttaa "torsades de pointes" -häiriöitä, kuten fenotiatsiini, sisapridi, bepridiili, trisykliset masennuslääkkeet, terfenadiini ja jotkut suun kautta otettavat makrolidit (kuten erytromysiini), luokan I ja III rytmihäiriölääkkeet (ks. Kohta 4.5)
• QTc -aika (Bazettin kaava) ≥ 500 millisekuntia
• Vaikea maksan vajaatoiminta
• Vaikea munuaisten vajaatoiminta (CrCl
• Dabigatraanin samanaikainen käyttö
04.4 Varoitukset ja käyttöön liittyvät varotoimet
Tarkkaa seurantaa suositellaan dronedaronin annon aikana arvioimalla säännöllisesti sydämen, maksan ja keuhkojen toimintaa (ks. Alla). Jos eteisvärinä uusiutuu, dronedaronin käytön lopettamista on harkittava. Dronedaronihoito on lopetettava, jos potilaalle kehittyy jokin sairaus, joka voi johtaa johonkin kohdassa 4.3 mainituista vasta -aiheista. Lääkkeiden, kuten digoksiinin ja antikoagulanttien, samanaikaista käyttöä on seurattava.
Potilaat, joille kehittyy pysyvä eteisvärinä hoidon aikana
Kliiniset tutkimukset potilailla, joilla oli pysyvä eteisvärinä (eteisvärinän kesto vähintään 6 kuukautta) ja joilla oli sydän- ja verisuonitaudin riskitekijöitä, lopetettiin ennenaikaisesti, koska MULTAQ -hoitoa saaneilla potilailla oli liikaa kuolleita sydän- ja verisuonitauteihin, aivohalvaukseen ja sydämen vajaatoimintaan (ks. kohta 5.1). On suositeltavaa suorittaa EKG säännöllisesti, vähintään 6 kuukauden välein Jos MULTAQ -hoitoa saaville potilaille kehittyy pysyvä eteisvärinä, MULTAQ -hoito on lopetettava.
Potilaat, joilla on aiempi tai nykyinen sydämen vajaatoiminta tai vasemman kammion systolinen toimintahäiriö.
MULTAQ on vasta -aiheinen potilaille, joilla on hemodynaamisesti epävakaa tila, joilla on aikaisempi tai nykyinen sydämen vajaatoiminta tai vasemman kammion systolinen toimintahäiriö (ks. Kohta 4.3).
Potilaita tulee arvioida huolellisesti kongestiivisen sydämen vajaatoiminnan oireiden varalta. Sydämen vajaatoimintajaksoja on ilmoitettu spontaanisti MULTAQ -hoidon aikana. Potilaita tulee neuvoa neuvottelemaan lääkärin kanssa, jos heille kehittyy tai ilmaantuu sydämen vajaatoiminnan oireita, kuten painonnousua, sydämen vajaatoiminnasta riippuvaista turvotusta tai lisääntynyttä hengenahdistusta.Jos sydämen vajaatoiminta kehittyy, MULTAQ-hoito on keskeytettävä.
Potilaita tulee seurata hoidon aikana vasemman kammion systolisen toimintahäiriön kehittymisen varalta. Jos vasemman kammion systolinen toimintahäiriö ilmenee, MULTAQ -hoito on lopetettava.
Potilaat, joilla on sepelvaltimotauti
Varovaisuutta on noudatettava potilailla, joilla on sepelvaltimotauti.
Eläkeläiset
Varovaisuutta on noudatettava iäkkäillä ≥ 75-vuotiailla potilailla, joilla on useita samanaikaisia sairauksia (ks. Kohdat 4.2 ja 5.1).
Maksavaurio
Maksasoluvaurioita, mukaan lukien hengenvaarallinen akuutti maksan vajaatoiminta, on raportoitu potilailla, jotka ovat saaneet MULTAQ-valmistetta markkinoille tulon jälkeen. Maksan toimintakokeet on tehtävä ennen dronedaronihoidon aloittamista, viikon kuluttua ja kuukauden kuluttua hoidon aloittamisesta ja toistetaan sitten kuukausittain kuuden kuukauden ajan 9. ja 12. kuukaudessa ja sen jälkeen määräajoin.
Jos alaniiniaminotransferaasi (ALT) on vähintään kolme kertaa normaalin yläraja (ULN), se on mitattava uudelleen 48-72 tunnin kuluessa. Jos ALAT -pitoisuuden vahvistetaan olevan 3 x ULN tai suurempi, dronedaronihoito on lopetettava.
Asianmukaista tutkimusta ja potilaiden tarkkaa seurantaa tulee jatkaa, kunnes ALAT -tasot normalisoituvat.
Potilaiden tulee välittömästi ilmoittaa lääkärille kaikista mahdollisen maksavaurion oireista (kuten uusi vakava vatsakipu, ruokahaluttomuus, pahoinvointi, oksentelu, kuume, huonovointisuus, väsymys, keltaisuus, tumma virtsa tai kutina).
"Kreatininemian lisääntymisen hallinta"
Veren kreatiniinipitoisuuden nousu (keskimääräinen nousu 10 μmol / l) havaittiin terveillä koehenkilöillä ja potilailla, kun annettiin 400 mg dronedaronia kahdesti vuorokaudessa. Useimmilla potilailla tämä nousu tapahtuu pian hoidon aloittamisen jälkeen ja saavuttaa tasangon 7 päivän kuluttua.Plasman kreatiniiniarvot on suositeltavaa mitata ennen dronedaronihoidon aloittamista ja 7 päivää sen jälkeen. Jos seerumin kreatiniinipitoisuus nousee, seerumin kreatiniinipitoisuus on mitattava uudelleen 7 päivän kuluttua.Jos seerumin kreatiniinipitoisuuden nousua ei enää havaita, tätä arvoa on käytettävä uutena lähtöviitearvona ottaen huomioon, että tämä nousu on odotettavissa dronedaronin annon jälkeen. Jos seerumin kreatiniiniarvo jatkaa nousuaan, on harkittava lisätutkimuksia ja hoidon lopettamista.
Veren kreatiniinipitoisuuden nousun ei välttämättä tarvitse johtaa ACE: n estäjien tai angiotensiini II -reseptorin salpaajien (sartaanien) käytön lopettamiseen.
Kreatiniinipitoisuuden suurentumista dronedaronihoidon aloittamisen jälkeen on raportoitu enemmän sen markkinoille tulon jälkeen.Joissakin tapauksissa raportoidaan myös veren ureatypen lisääntymisestä, mikä johtuu mahdollisesti hypoperfuusiosta, joka on seurausta kongestiivisen sydämen vajaatoiminnan kehittymisestä (veren urean typpi). Munuaiset) . Tällaisissa tapauksissa dronedaronin käyttö on lopetettava (ks. Kohdat 4.3 ja 4.4). On suositeltavaa seurata munuaisten toimintaa säännöllisesti ja harkita tarvittaessa lisätutkimuksia.
Elektrolyyttitasapaino
Koska rytmihäiriölääkkeet voivat olla tehottomia tai rytmihäiriöisiä potilailla, joilla on hypokalemia, mahdollinen kalium- tai magnesiumin puutos on korjattava ennen dronedaronihoidon aloittamista ja sen aikana.
QT -segmentin venyminen
Dronedaronin farmakologinen aktiivisuus voi aiheuttaa Bazettin kaavalla lasketun QTc: n kohtalaisen pidentymisen (noin 10 millisekuntia), joka liittyy pitkittyneeseen repolarisaatioon. Nämä vaihtelut liittyvät dronedaronin terapeuttiseen vaikutukseen eivätkä heijasta sen myrkyllisyyttä. Seurantaa, mukaan lukien EKG (elektrokardiogrammi), suositellaan hoidon aikana.Dronedaronihoito on lopetettava, jos QTc-aika (Bazettin kaava) on ≥ 500 millisekuntia (ks. Kohta 4.3).
Kliinisen kokemuksen perusteella dronedaroni osoitti ATHENA -tutkimuksessa heikon proarytmisen vaikutuksen ja vähentyneen rytmihäiriöitä (ks. Kohta 5.1).
Rytmihäiriöitä voi kuitenkin esiintyä tietyissä tilanteissa, kuten samanaikaisesti käytettäessä rytmihäiriöitä ja / tai elektrolyyttihäiriöitä edistäviä lääkkeitä (ks. Kohdat 4.4 ja 4.5).
Hengityselimet, rintakehä ja välikarsina
Markkinoille tulon jälkeen on raportoitu interstitiaalisen keuhkosairauden tapauksia, mukaan lukien keuhkokuume ja keuhkofibroosi. .
Yhteisvaikutukset (ks. Kohta 4.5)
Digoksiini.
Dronedaronin antaminen digoksiinihoitoa saaville potilaille voi suurentaa plasman digoksiinipitoisuuksia ja pahentaa siten digoksiinitoksisuuteen liittyviä oireita ja oireita.
Kliinistä, biologista ja EKG -seurantaa suositellaan ja digoksiiniannos puolitetaan. Lisäksi voi esiintyä synergististä vaikutusta sykkeeseen ja eteis -kammion johtumiseen.
Yhteishallinto beetasalpaajat tai kalsiumkanavasalpaajat joilla on masentava vaikutus sinusolmuun ja eteis -kammiosolmuun, tulee noudattaa varovaisuutta. Näitä lääkevalmisteita tulee antaa aluksi pieninä annoksina ja annoksen suurentamisesta on päätettävä vasta EKG: n arvioinnin jälkeen. On suositeltavaa suorittaa EKG ja tarvittaessa muuttaa annosta potilailla, jotka jo saavat kalsiumkanavasalpaa tai beetasalpaajaa ennen dronedaronihoidon aloittamista. .
Antikoagulantit
Potilaita on hoidettava asianmukaisesti antikoagulanttihoidolla AF: n kliinisten ohjeiden mukaisesti. Kansainvälistä normalisoitua suhdetta (INR) on seurattava tarkasti dronedaronihoidon aloittamisen jälkeen potilailla, jotka käyttävät K -vitamiiniantagonisteja, kuten näiden tuotteiden painotuotteissa on ilmoitettu.
Induktorien käyttöä ei suositella voimakas CYP 3A4 kuten rifampisiini, fenobarbitaali, karbamatsepiini, fenytoiini tai mäkikuisma (mäkikuisma).
Monoamiinioksidaasin (MAO) estäjät voi heikentää dronedaronin aktiivisen metaboliitin puhdistumaa, joten sitä on käytettävä varoen.
Statiinit on käytettävä varoen. Pienempiä statiinien aloitus- ja ylläpitoannoksia on harkittava ja potilaita on seurattava lihastoksisuuden kliinisten oireiden varalta.
Potilaita tulee neuvoa välttämään juomia, jotka sisältävät greippimehu kun annettiin dronedaronia.
Laktoosi
Tämä lääke sisältää laktoosia. Potilaiden, joilla on harvinainen perinnöllinen galaktoosi-intoleranssi, laktaasin puutos tai glukoosi-galaktoosi-imeytymishäiriö, ei tule käyttää tätä lääkettä.
04.5 Yhteisvaikutukset muiden lääkevalmisteiden kanssa sekä muut yhteisvaikutukset
Dronedaroni metaboloituu pääasiassa CYP 3A4: n kautta (ks. Kohta 5.2). Siksi CPY 3A4: n estäjät ja indusorit voivat olla vuorovaikutuksessa dronedaronin kanssa.
Dronedaroni on kohtalainen CYP 3A4: n, CYP 2D6: n estäjä ja voimakas Pglykoproteiinien (P-gp) estäjä. Siksi dronedaroni voi olla vuorovaikutuksessa lääkkeiden kanssa, jotka ovat Pgp: n, CYP 3A4: n tai CYP 2D6: n substraatteja. Dronedaronia ja / tai sen metaboliitteja on myös osoitettu in vitro estämään orgaanisten anionien kuljettajien (OAT), orgaanisten anionikuljetuspolypeptidien (OATP) ja orgaanisten kationien kuljettajien (OCT) perheisiin kuuluvia kuljetusproteiineja.
Dronedaronilla ei ole merkittävää potentiaalista vaikutusta substraattien CYP 1A2, CYP 2C9, CYP 2C19, CYP 2C8 ja CYP 2B6 estämiseen.
Mahdollista farmakodynaamista vuorovaikutusta beetasalpaajien, kalsiumkanavasalpaajien ja digitaliksen kanssa voidaan myös odottaa.
Lääkkeet, jotka voivat aiheuttaa "torsades de pointes"
Lääkkeet, jotka voivat aiheuttaa "kääntyvien kärkien takykardiaa", kuten fenotiatsiinit, sisapridi, bepridiili, trisykliset masennuslääkkeet, jotkut suun kautta otettavat makrolidit (kuten erytromysiini), terfenadiini ja luokan I tai III rytmihäiriölääkkeet ovat vasta -aiheisia proarytmian kehittymisen mahdollisen riskin vuoksi (ks. 4.3). Varovaisuutta on noudatettava annettaessa beetasalpaajia tai digitalis-valmistetta samanaikaisesti.
Muiden lääkevalmisteiden vaikutus MULTAQiin
Vahvat CYP 3A4: n estäjät
Toistuvat 200 mg: n vuorokausiannokset ketokonatsolia johtivat 17-kertaiseen dronedaronialtistukseen. Siksi ketokonatsolin ja muiden voimakkaiden CYP 3A4: n estäjien, kuten itrakonatsolin, vorikonatsolin, posakonatsolin, ritonaviirin, telitromysiinin, klaritromysiinin tai nefatsodonin, samanaikainen käyttö on vasta-aiheista (ks. 4.3).
Kohtalainen / heikko CYP 3A4: n estäjä
• Erytromysiini
Erytromysiini, suun kautta otettava makrolidi, voi aiheuttaa kääntyvien kärkien takykardiaa ja on siksi vasta -aiheinen (ks. Kohta 4.3). Toistuvat erytromysiiniannokset (500 mg kolme kertaa päivässä 10 päivän ajan) kasvattivat altistusta dronedaronille vakaassa tilassa 3,8 -kertaiseksi .
• Kalsiumantagonistit
Kalsiumkanavasalpaajat, diltiatseemi ja verapamiili, ovat kohtalaisia CYP 3A4: n substraatteja ja / tai estäjiä. Lisäksi, ottaen huomioon niiden bradykardisoiva vaikutus, verapamiili ja diltiatseemi voivat olla vuorovaikutuksessa dronedaronin kanssa farmakodynaamisesta näkökulmasta.
Diltiatseemin (240 mg kahdesti vuorokaudessa), verapamiilin (240 mg kerran vuorokaudessa) ja nifedipiinin (20 mg kahdesti vuorokaudessa) toistuvat annokset kasvattivat dronedaronialtistusta 1,7 - 1,4 ja 1,2 kertaa. altistuminen kalsiuminestäjille (verapamiili 1,4 kertaa ja nisoldipiini 1,5 kertaa).
Yleensä farmakokineettisten yhteisvaikutusten ja mahdollisten farmakodynaamisten yhteisvaikutusten vuoksi sinusolmukkeiden ja eteis -kammiosolmukkeiden masentavia kalsiumkanavasalpaajia, kuten verapamiilia ja diltiatseemia, tulee käyttää varoen, kun niitä annetaan yhdessä dronedaronin kanssa. Näitä lääkevalmisteita tulee antaa aluksi pieninä annoksina ja annoksia suurentaa vasta EKG -arvioinnin jälkeen. On suositeltavaa suorittaa EKG ja kalsiumkanavasalpaajan annos tarvittaessa säätää potilaille, jotka jo saavat kalsiumhoitoa. dronedaronihoidosta (ks. kohta 4.4).
• Muut heikot / kohtalaiset CYP 3A4: n estäjät
Myös muut kohtalaiset CYP3A4: n estäjät lisäävät todennäköisesti dronedaronialtistusta.
CYP 3A4: n indusorit
Rifampisiini (600 mg kerran vuorokaudessa) vähentää dronedaronialtistusta 80% muuttamatta merkittävästi altistusta sen aktiiviselle metaboliitille.Siksi rifampisiinin ja muiden voimakkaiden CYP 3A4: n indusoijien, kuten fenobarbitaalin, karbamatsepiinin, fenytoiinin tai mäkikuisman, samanaikaista käyttöä ei suositella koska ne vähentävät altistumista dronedaronille.
MAO -estäjät
Studiossa in vitro MAO: t vaikuttivat dronedaronin aktiivisen metaboliitin metaboliaan.
Tämän havainnon kliinistä merkitystä ei tunneta (ks. Kohdat 4.4 ja 5.2).
MULTAQin vaikutus muihin lääkevalmisteisiin
Yhteisvaikutukset CYP 3A4: n metaboloimien lääkkeiden kanssa
• Statiinit
Dronedaroni voi lisätä altistusta statiineille, jotka ovat CYP 3A4: n ja / tai P-gp: n substraatteja.
Dronedaroni (400 mg kahdesti vuorokaudessa) lisää altistusta simvastatiini- ja simvastatiinihapolle nelinkertaiseksi ja 2-kertaiseksi. Dronedaronin odotetaan myös lisäävän lovastatiinialtistusta samalla alueella kuin simvastatiinihappo. Dronedaronin ja atorvastatiinin välillä havaittiin heikko vuorovaikutus (mikä johti 1,7-kertaiseen keskimääräiseen altistukseen atorvastatiinille). Dronedaronin ja OATP: n kuljettamien statiinien, kuten rovustatiinin, välillä havaittiin heikko vuorovaikutus (jolloin rovustatiinialtistus kasvoi keskimäärin 1,4-kertaiseksi).
Kliiniset tutkimukset eivät paljastaneet turvallisuusongelmia, kun dronedaronia annettiin yhdessä CYP 3A4: n metaboloimien statiinien kanssa. Rabdomyolyysitapauksia on kuitenkin ilmoitettu spontaanisti, kun dronedaronia annettiin yhdessä statiinin (erityisesti simvastatiinin) kanssa, ja siksi statiinien samanaikaiseen käyttöön on suhtauduttava varoen.
Pienempiä aloitus- ja ylläpitoannoksia on harkittava yksittäisten statiinien valmisteyhteenvedon mukaisesti ja potilaita on seurattava lihasten toksisuuden kliinisten oireiden varalta (ks. Kohta 4.4).
• Kalsiumantagonistit
Dronedaronin vuorovaikutus kalsiumkanavasalpaajien kanssa on kuvattu edellä (ks. Kohta 4.4).
• Immunosuppressantit
Dronedaroni saattaa suurentaa immunosuppressiivisten aineiden (takrolimuusi, sirolimuusi, everolimuusi ja syklosporiini) pitoisuutta plasmassa. Plasman pitoisuuksien seurantaa ja asianmukaista annoksen muuttamista suositellaan, kun sitä annetaan samanaikaisesti dronedaronin kanssa.
• Ehkäisypillerit
Etinyyliestradioli- ja levonorgestreelipitoisuuksien laskua ei havaittu terveillä koehenkilöillä, jotka saivat dronedaronia (800 mg kahdesti vuorokaudessa) yhdessä suun kautta otettavien ehkäisyvalmisteiden kanssa.
Yhteisvaikutukset CYP 2D6: n metaboloimien lääkkeiden kanssa: beetasalpaajat, masennuslääkkeet
• Beetasalpaajat
Sotalol -hoito on lopetettava ennen MULTAQ -hoidon aloittamista (ks. Kohdat 4.3 ja 4.4).
Dronedaroni voi lisätä altistusta beetasalpaajille, jotka metaboloituvat CYP 2D6: n kautta. Lisäksi beetasalpaajat voivat olla vuorovaikutuksessa dronedaronin kanssa farmakodynaamisesta näkökulmasta. metoprololin ja 1,3-kertaisen propranololin (eli paljon pienempi kuin 6-kertainen ero, joka havaittiin heikkojen metaboloijien ja CYP 2D6: n laajojen metaboloijien välillä). Bradykardian jaksoja havaittiin useammin kliinisissä tutkimuksissa, kun dronedaronia annettiin yhdessä beetasalpaajien kanssa.
Farmakokineettisten yhteisvaikutusten ja mahdollisten farmakodynaamisten yhteisvaikutusten vuoksi beetasalpaajia on käytettävä varoen, kun niitä annetaan yhdessä dronedaronin kanssa. Näitä lääkevalmisteita tulee antaa aluksi pieninä annoksina ja annoksia tulee suurentaa vasta EKG: n arvioinnin jälkeen. dronedaronihoidon aloittamisesta (ks. kohta 4.4).
• Masennuslääkkeet
Koska dronedaroni on heikko CYP 2D6: n estäjä ihmisillä, oletetaan, että vuorovaikutus CYP 2D6: n metaboloimien masennuslääkkeiden kanssa on rajallinen.
P-gp-substraatin vuorovaikutukset
• Digoksiini
Dronedaroni (400 mg kahdesti vuorokaudessa) lisää digoksiinialtistusta 2,5 kertaa estämällä P-gp: n kuljetustoimintoa. Lisäksi digitalis voi olla vuorovaikutuksessa dronedaronin kanssa farmakodynaamisesta näkökulmasta. Se voidaan havaita. Synergistinen vaikutus sykkeeseen ja eteis-kammion johtumiseen . Kliinisissä tutkimuksissa on havaittu lisääntynyttä digitalis -tasoa ja / tai ruoansulatuskanavan häiriöiden indikaattoreita, kun dronedaronia annettiin yhdessä digitaliksen kanssa.
On suositeltavaa pienentää digoksiiniannosta noin 50%, seurata tarkasti seerumin digoksiinipitoisuuksia ja suorittaa kliinistä ja EKG -seurantaa.
• Dabigatraani
Kun dabigatraanieteksilaattia 150 mg kerran vuorokaudessa annettiin yhdessä dronedaronin 400 mg kahdesti vuorokaudessa kanssa, dabigatraanin AUC 0-24 ja Cmax nousivat 100% ja 70% .Kliinisiä tietoja näiden lääkevalmisteiden samanaikaisesta käytöstä ei ole saatavilla potilaille, joilla on eteisvärinä Samanaikainen käyttö on vasta-aiheista (ks. kohta 4.3).
Yhteisvaikutukset varfariinin ja losartaanin (CYP 2C9 -substraatit) kanssa
• Varfariini ja muut K -vitamiinin antagonistit
Dronedaroni (600 mg kahdesti vuorokaudessa) lisää S-varfariinialtistusta 1,2-kertaiseksi ilman muutoksia R-varfariinissa ja vain kansainvälisen normalisoidun suhteen (INR) nousua vain 1,07-kertaiseksi.
Kuitenkin INR: n kliinisesti merkittävää nousua (≥ 5), yleensä yhden viikon kuluessa dronedaronihoidon aloittamisesta, on raportoitu suun kautta otettavia antikoagulantteja käyttävillä potilailla. Siksi INR -arvoa on seurattava tarkasti dronedaronihoidon aloittamisen jälkeen potilailla, jotka ovat saaneet K -vitamiiniantagonisteja hyväksytyn kirjallisuuden mukaisesti.
• Losartaani ja muut AIIRA-lääkkeet (angiotensiini II -reseptorin salpaajat)
Yhteisvaikutuksia ei havaittu dronedaronin ja losartaanin välillä, eikä yhteisvaikutuksia odoteta dronedaronin ja muiden AIIRA -lääkkeiden välillä.
Yhteisvaikutukset teofylliinin (CYP 1A2 -substraatti) kanssa
Dronedaroni 400 mg kahdesti vuorokaudessa ei lisää vakaan tilan altistusta teofylliinille.
Yhteisvaikutukset metformiinin kanssa (OCT1: n ja OCT2: n substraatti)
Yhteisvaikutusta ei havaittu dronedaronin ja metformiinin, OCT1: n ja OCT2: n substraatin, välillä.
Yhteisvaikutukset omepratsolin kanssa (sytokromi CYP 2C19: n substraatti)
Dronedaroni ei vaikuta omepratsolin, sytokromi CYP 2C19: n substraatin, farmakokinetiikkaan.
Yhteisvaikutukset klopidogreelin kanssa
Dronedaroni ei vaikuta klopidogreelin ja sen aktiivisen metaboliitin farmakokinetiikkaan.
Muita tietoja
Pantopratsoli (40 mg kerran vuorokaudessa), lääke, joka nostaa mahalaukun pH: ta vaikuttamatta kuitenkaan CYP: hen, ei ole merkittävästi vuorovaikutuksessa dronedaronin farmakokinetiikan kanssa.
Greippimehu (CYP 3A4: n estäjä)
Toistuvat 300 ml: n greippimehun annokset kolme kertaa päivässä kasvattivat dronedaronialtistusta kolminkertaiseksi, joten potilaita tulee neuvoa välttämään greippimehujuomia dronedaronin annon aikana (ks. Kohta 4.4).
04.6 Raskaus ja imetys
Hedelmällisessä iässä olevat naiset ja raskaus
Tietoja dronedaronin käytöstä raskaana oleville naisille ei ole tai niitä on vain vähän.
Eläinkokeet ovat osoittaneet lisääntymistoksisuutta (ks. Kohta 5.3).
MULTAQia ei suositella raskauden aikana eikä hedelmällisessä iässä oleville naisille, jotka eivät käytä ehkäisyä.
Ruokinta-aika
Ei tiedetä, erittyykö dronedaroni ja sen metaboliitit maitoon. Saatavilla olevat farmakodynaamiset / toksikologiset tiedot eläimistä ovat osoittaneet, että dronedaroni ja sen metaboliitit erittyvät maitoon. Riskiä vastasyntyneille / imeväisille ei voida sulkea pois.
On päätettävä, lopetetaanko imetys vai lopetetaanko MULTAQ-hoito tai pidättäydytäänkö siitä ottaen huomioon imetyksen hyödyt lapselle ja hoidon hyödyt naiselle.
Hedelmällisyys
Eläinkokeet eivät ole osoittaneet dronedaroniin liittyvää hedelmällisyyden heikkenemistä.
04.7 Vaikutus ajokykyyn ja koneiden käyttökykyyn
Multaqilla ei ole haitallista vaikutusta ajokykyyn ja koneiden käyttökykyyn.
Haittavaikutukset, kuten väsymys, voivat kuitenkin heikentää ajokykyä ja koneiden käyttökykyä.
04.8 Haittavaikutukset
Yhteenveto turvallisuusprofiilista
Luonnollisten tekijöiden, kuten sukupuolen tai iän, arviointi hoidon aikana ilmenneiden haittavaikutusten esiintymistiheydestä osoitti vuorovaikutuksen sukupuolen (naispotilaiden) kanssa haittavaikutusten ja vakavien haittavaikutusten esiintyvyyden suhteen.
Kliinisissä tutkimuksissa hoidon varhainen lopettaminen haittavaikutusten vuoksi tapahtui 11,8%: lla dronedaronilla hoidetuista potilaista ja 7,7%: lla lumelääkeryhmästä. Yleisimmät syyt MULTAQ-hoidon lopettamiseen olivat ruoansulatuskanavan häiriöt (3,2% dronedaronihoitoa saaneista ja 1,8% lumelääkettä saaneista potilaista).
Yleisimmin havaitut haittavaikutukset viidessä tutkimuksessa, jotka suoritettiin dronedaronilla annoksella 400 mg kahdesti vuorokaudessa, olivat: ripuli, pahoinvointi ja oksentelu, väsymys ja voimattomuus.
Taulukko haittavaikutuksista
Dronedaronin turvallisuusprofiili annoksella 400 mg kahdesti vuorokaudessa potilaille, joilla on eteisvärinä (AF) tai eteislepatus (FLA), perustuu viiteen lumekontrolloituun tutkimukseen, joissa satunnaistettiin yhteensä 6285 potilasta. 400 mg dronedaronia kahdesti vuorokaudessa ja 2875 potilasta, jotka saivat lumelääkettä). Tutkimusten keskimääräinen altistus oli 13 kuukautta.ATHENA-tutkimuksessa seurannan enimmäiskesto oli 30 kuukautta.Jotkut haittavaikutukset havaittiin markkinoille tulon jälkeen.
Haittavaikutukset luokitellaan järjestelmien ja elinten mukaan.
Esiintymistiheydet on määritelty seuraavasti: hyvin yleinen (≥1 / 10); yleinen (≥ 1/100,
Taulukko 1: Haittavaikutukset
* (≥ 10%) 5 päivää hoidon aloittamisen jälkeen (ks. Kohta 4.4)
** (> 450 ms. Uros> 470 ms. Naaras) (ks. Kohta 4.4)
Valittujen haittavaikutusten kuvaus
Viidessä lumekontrolloidussa tutkimuksessa kongestiivinen sydämen vajaatoiminta todettiin dronedaroniryhmässä, ja ilmaantuvuus oli verrattavissa lumelääkeryhmään (hyvin yleinen, 11,2% vs. 10,9%). Tämä prosenttiosuus on otettava huomioon, kun taustalla on korkea kongestiivisen sydämen vajaatoiminnan ilmaantuvuus potilailla, joilla on eteisvärinä.Kongestiivista sydämen vajaatoimintaa on raportoitu myös markkinoille tulon jälkeen (esiintymistiheys tuntematon) (ks. Kohta 4.4).
Viidessä lumekontrolloidussa tutkimuksessa keuhkotapahtumia esiintyi 0,6%: lla dronedaroniryhmän potilaista ja 0,8%: lla lumelääkettä saaneista potilaista. Markkinoille tulon jälkeen on raportoitu interstitiaalisen keuhkosairauden tapauksia, mukaan lukien keuhkokuume ja keuhkofibroosi (esiintymistiheys tuntematon).
Epäillyistä haittavaikutuksista ilmoittaminen
Ilmoittaminen epäillyistä haittavaikutuksista, jotka ilmenevät lääkkeen myyntiluvan myöntämisen jälkeen, on tärkeää. Se mahdollistaa jatkuvan seurannan lääkkeen hyöty -haittasuhteesta. Terveydenhuollon ammattilaisia pyydetään ilmoittamaan kaikista epäillyistä haittavaikutuksista kansallisen ilmoitusjärjestelmän kautta. "Liite V.
04.9 Yliannostus
Ei tiedetä, voidaanko dronedaroni ja / tai sen metaboliitit poistaa dialyysillä (hemodialyysi, peritoneaalidialyysi tai hemofiltraatio).
Spesifistä vastalääkettä ei ole. Yliannostustapauksissa suositellaan oireenmukaista tukihoitoa oireiden lievittämiseksi.
05.0 FARMAKOLOGISET OMINAISUUDET
05.1 Farmakodynaamiset ominaisuudet
Farmakoterapeuttinen ryhmä: sydänhoito, luokan III rytmihäiriölääkkeet.
ATC -koodi: C01BD07.
Toimintamekanismi
Eläimillä dronedaroni estää eteisvärinän tai palauttaa normaalin sinusrytmin käytetyn mallin mukaan. Dronedaroni estää myös takykardian ja kammiovärinän useissa eläinmalleissa. Nämä vaikutukset johtuvat todennäköisesti sen kaikkien elektrofysiologisista ominaisuuksista. Vaughan-Williams-luokat monikanavainen salpaaja, joka estää kaliumvirtoja (mukaan lukien IK (Ach), IKur, IKr, IKs) pidentäen siten sydämen toimintapotentiaalia ja tulenkestäviä jaksoja (luokka III). Se estää myös natrium- (luokka Ib) ja kalsium- (luokka IV) virtauksia. Dronedaroni antagonisoi adrenergistä aktiivisuutta (luokka II) ei-kilpailevalla tavalla.
Farmakodynaamiset ominaisuudet
Eläinmalleissa dronedaroni alentaa sykettä. Se pidentää Wenckebach -syklin pituutta ja AH-, -PQ- ja -QT -aikavälejä tuottamatta merkittävää vaikutusta tai aiheuttamatta lievää QTc -ajan pitenemistä ja muuttamatta HV- ja -QRS -aikavälejä. Dronedaroni lisää eteisen, eteis -kammion solmun ja kammion PRE: n tehokkaita tulenkestävyysaikoja (PRE) ja pidentää niitä hieman vähäisellä nopeudella - käänteinen riippuvuus.
Dronedaroni alentaa verenpainetta ja sydänlihaksen supistuvuutta (dP / dTmax) muuttamatta vasemman kammion ejektiofraktiota ja vähentää sydänlihaksen hapen kulutusta.
Dronedaronilla on verisuonia laajentavia ominaisuuksia sepelvaltimoissa (liittyy typpioksidireitin aktivoitumiseen) ja perifeerisissä valtimoissa.
Dronedaronilla on epäsuorat antiadrenergiset vaikutukset ja osittainen antagonismi adrenergiselle stimulaatiolle. Se vähentää alfa-adrenergisten reseptorien painevastetta adrenaliinille ja beeta1- ja beeta2-reseptorien vasteita isoproterenolille.
Kliininen teho ja turvallisuus
Vähentää AF-aiheisen sairaalahoidon riskiä
Dronedaronin tehokkuus AF: hen liittyvän sairaalahoidon riskin vähentämisessä osoitettiin potilailla, joilla oli AF tai joilla on aiemmin ollut AF ja joilla on muita riskitekijöitä ATHENA-tutkimuksessa, monikeskustutkimuksessa, monikansallisessa, kaksoissokkoutetussa, satunnaistetussa, kontrolloidussa tutkimuksessa .
Potilailta vaadittiin vähintään yksi riskitekijä (mukaan lukien ikä, kohonnut verenpaine, diabetes, aiempi aivoverisuonitapahtuma, vasemman eteisen halkaisija ≥ 50 mm tai LVEF
Neljä tuhatta kuusisataa kaksikymmentäkahdeksan (4628) potilasta satunnaistettiin ja heitä hoidettiin enintään 30 kuukautta (keskimääräinen seuranta: 22 kuukautta) joko dronedaronilla, 400 mg kahdesti vuorokaudessa (2301 potilasta) tai lumelääkkeellä (2327 potilasta). sekä tavanomaista hoitoa, joka sisälsi beetasalpaajia (71%), ACE: n estäjiä tai AIIRA-lääkkeitä (69%), digitalis (14%), kalsiumkanavasalpaajia (14%), statiineja (39%), oraalisia antikoagulantteja (60) krooninen verihiutaleiden hoito (6%) ja / tai diureetit (54%).
Tutkimuksen ensisijainen päätetapahtuma oli aika ensimmäiseen sairaalahoitoon sydän- ja verisuoniperäisistä syistä tai kuolemasta mistä tahansa syystä.
Potilaat olivat 23–97 -vuotiaita ja 42% yli 75 -vuotiaita. 47 prosenttia (47%) potilaista oli naisia ja suurin osa valkoihoisia (89%).
Useimmilla potilailla oli kohonnut verenpaine (86%) ja rakenteellinen sydänsairaus (60%) (mukaan lukien sepelvaltimotauti: 30%; kongestiivinen sydämen vajaatoiminta (CHF): 30%; LVEF
Kaksikymmentäviisi prosenttia (25%) potilaista sai eteisvärinän lähtötilanteessa.
Dronedaroni vähensi sydän- ja verisuonitautien sairaalahoitoa tai mistä tahansa syystä johtuvaa kuolemaa 24,2% lumelääkkeeseen verrattuna (s
Kardiovaskulaarisen sairaalahoidon tai mistä tahansa syystä johtuvan kuoleman väheneminen oli vertailukelpoista kaikissa alaryhmissä alkuperäisistä ominaisuuksista tai annetusta lääkkeestä riippumatta (ACE: n estäjät tai AIIRA: t; beetasalpaajat, digitalis, statiinit, kalsiumkanavan salpaajat, diureetit).
Sinusyn rytmin ylläpito
EURIDIS- ja ADONIS -tutkimuksissa yhteensä 1237 potilasta, joilla oli aiempi AF- tai FLA -episodi, satunnaistettiin avohoidossa ja saivat joko 400 mg dronedaronia kahdesti vuorokaudessa (n = 828) tai lumelääkettä (n = 409) tavanomaiset hoidot (mukaan lukien suun kautta otettavat antikoagulantit, beetasalpaajat, ACE: n estäjät tai AIIRA -lääkkeet, kroonisesti käytetyt verihiutaleiden vastaiset aineet, diureetit, statiinit, digitalis ja kalsiumkanavan salpaajat). Potilaita, joilla oli ollut vähintään yksi AF / FLA -episodi dokumentoituna EKG: llä viimeisten 3 kuukauden aikana ja jotka olivat sinusrytmissä vähintään yhden tunnin ajan, seurattiin 12 kuukauden ajan. ensimmäinen lääkkeen anto sen hyvän siedettävyyden varmistamiseksi Muut rytmihäiriölääkkeet oli keskeytettävä vähintään viiden puoliintumisajan plasmasta ennen lääkkeen ensimmäistä antamista.
Potilaiden ikä vaihteli 20-88-vuotiaista, pääasiassa valkoihoisista (97%), miehistä (69%) .Yleisimpiä samanaikaisia sairauksia olivat: verenpaine (56,8%) ja rakenteellinen sydänsairaus (41,5%), mukaan lukien sepelvaltimotauti sairaus (21,8%).
EURIDIS- ja ADONIS -tutkimusten sekä yksittäisten tutkimusten yhdistetyt tiedot osoittivat, että dronedaroni viivästyttää jatkuvasti AF / FLA: n ensimmäistä uusiutumista (ensisijainen päätetapahtuma).
Dronedaroni pienensi ensimmäisen AF / FLA-taudin uusiutumisen riskiä 12 kuukauden tutkimuksen keston aikana 25% (p = 0,00007) lumelääkkeeseen verrattuna. Keskimääräinen aika satunnaistamisesta ensimmäiseen AF / FLA -uusiutumiseen dronedaroniryhmässä oli 116 päivää, mikä on 2,2 kertaa pidempi kuin lumeryhmässä (53 päivää).
DIONYSOS -tutkimuksessa verrattiin dronedaronin (400 mg kahdesti vuorokaudessa) tehoa ja turvallisuutta verrattuna amiodaroniin (600 mg vuorokaudessa 28 päivän ajan ja sitten 200 mg vuorokaudessa) 6 kuukauden aikana. Yhteensä 504 dokumentoitua AF -potilasta, 249 dronedaronilla hoidettua potilasta Amiodaronilla hoidettiin 255. Potilaat olivat 28-90 -vuotiaita, 49% oli yli 65 -vuotiaita. Ensisijaisen tehon päätetapahtuman ilmaantuvuus, joka määritellään ensimmäisenä AF: n uusiutumisena tai tutkimuslääkkeen ennenaikaisena lopettamisena suvaitsemattomuuden tai tehon puutteen vuoksi 12 kuukauden kohdalla, oli 75% dronedaroniryhmässä ja 59% dronedaroniryhmässä. suhde = 1,59, log-rank p-arvo
AF -uusiutumiset (mukaan lukien kardioversion puuttuminen) olivat yleisempiä dronedaroniryhmässä, kun taas tutkimuslääkkeen ennenaikainen lopettaminen suvaitsemattomuuden vuoksi oli yleisempi amiodaroniryhmässä. , keuhko-, neurologiset, ihon, silmän tai ruoansulatuskanavan tapahtumat tai tutkimuslääkkeen ennenaikainen lopettaminen haittavaikutuksen jälkeen väheni 20% dronedaroniryhmässä verrattuna amiodaronilla hoidettuun ryhmään (p = 0,129). Tämä lasku johtui pääasiassa kilpirauhasen ja neurologisten tapahtumien ilmaantumisesta, taipumuksesta harvempiin iho- ja silmäsairauksiin ja tutkimuslääkkeen ennenaikaiseen lopettamiseen haittatapahtumiin verrattuna amiodaronilla hoidettuun ryhmään.
Lisää ruoansulatuskanavan haittatapahtumia, pääasiassa ripulia, havaittiin dronedaroniryhmässä (12,9% vs 5,1%).
Potilaat, joilla on sydämen vajaatoiminnan oireita levossa tai vähäisellä rasituksella kuukauden sisällä ennen sairaalahoitoa tai potilaita, jotka ovat sairaalahoidossa sydämen vajaatoiminnan vuoksi kuukauden aikana Edellinen.
ANDROMEDA -tutkimukseen osallistui 627 potilasta, joilla oli vasemman kammion toimintahäiriö, sairaalahoitoon uuden tai pahentuneen sydämen vajaatoiminnan vuoksi ja joilla oli vähintään yksi hengenahdistusjakso vähäisellä rasituksella tai levossa (NYHA -luokka III tai IV) tai paroksismaalinen yöllinen hengenahdistus edellisen kuukauden aikana pääsylle. Potilaiden ikä oli 27–96 vuotta, 68% oli yli 65 -vuotiaita. Tutkimus lopetettiin ennenaikaisesti, koska kuolleiden määrä oli epätasapainossa dronedaroniryhmässä [n = 25 vs 12 (lumelääke), p = 0,027] (ks. kohdat 4.3 ja 4.4).
Potilaat, joilla on pysyvä eteisvärinä:
PALLAS-tutkimus oli satunnaistettu lumekontrolloitu tutkimus, jossa arvioitiin 400 mg: n dronedaronin kahdesti vuorokaudessa kliinistä hyötyä tavanomaisen hoidon lisänä potilailla, joilla on pysyvä eteisvärinä ja muita riskitekijöitä (potilaat, joilla on kongestiivinen sydämen vajaatoiminta? 69%, sepelvaltimotauti ? 41%, aiempi aivohalvaus tai TIA? 27%, LVEF ≤ 40%? 20,7%ja ≥ 75 -vuotiaat potilaat, joilla on kohonnut verenpaine ja diabetes? 18%). Tutkimus lopetettiin ennenaikaisesti 3149 potilaan satunnaistamisen jälkeen (lumelääke = 1577; dronedaroni = 1572), koska sydämen vajaatoiminta lisääntyi merkittävästi (lumelääke = 33; dronedaroni = 80; sydän = 2,49 (1,66-3, 74)]; aivohalvaus [plasebo = 8; dronedaroni = 17; sydän = 2,14 (0,92-4,96)] ja sydän- ja verisuoniperäiset kuolemat [lumelääke = 6; dronedaroni = 15; sydän = 2, 53 (0,98-6,53)] (ks. kohdat 4.3 ja 4.4) .
05.2 Farmakokineettiset ominaisuudet
Imeytyminen
Suun kautta annettuna, ruokittuina, dronedaroni imeytyy hyvin (vähintään 70%). Dronedaronin (ruoan kanssa annettuna) absoluuttinen hyötyosuus on kuitenkin 15% lääkkeen ensikierron metabolian vuoksi. Samanaikainen ruokailu lisää dronedaronin biologista hyötyosuutta noin 2-4 kertaa.Dronedaronin ja tärkeimmän verenkierrossa olevan aktiivisen metaboliitin (N-debutyylimetaboliitti) huippupitoisuudet plasmassa saavutetaan 3-6 tunnin kuluessa oraalisen annon jälkeen. 8 päivän hoito toistuvien 400 mg: n annosten jälkeen kahdesti vuorokaudessa ja dronedaronin keskimääräinen kertymissuhde on 2,6-4,5. Vakaan tilan dronedaronin keskimääräinen Cmax on 84-147 ng / ml ja tärkeimmän metaboliitin N-debutyylin altistus samanlainen kuin emoyhdisteen. Sekä dronedaronin että sen metaboliitin N-debutyylin farmakokinetiikka poikkeavat kohtalaisesti annoksen suhteellisuudesta: kaksinkertainen annoksen nostaminen johtaa noin 2,5-3,0-kertaiseen Cmax- ja "AUC-arvon nousuun.
Jakelu
In vitro, dronedaronin sitoutuminen plasman proteiineihin ja sen N-debutyylimetaboliittiin on vastaavasti 99,7% ja 98,5%, eikä se ole kyllästyvä. Molemmat yhdisteet sitoutuvat pääasiassa albumiiniin.
Biotransformaatio
Dronedaroni metaboloituu laajalti, pääasiassa CYP 3A4: n välityksellä (ks. Kohta 4.5). Tärkein aineenvaihduntareitti sisältää N-debutylaatioprosessin muodostaen tärkein kiertävä aktiivinen metaboliitti, jota seuraa hapetus, hapettava deaminaatio muodostaen inaktiivisen propaanihapon metaboliitin, jota seuraa hapetus ja suora hapetus. MAO: t vaikuttavat osittain dronedaronin aktiivisen metaboliitin metaboliaan (ks. Kohta 4.5).
N-debutyylimetaboliitin farmakodynaaminen aktiivisuus on 3–10 kertaa heikompi kuin dronedaroni, joka vaikuttaa dronedaronin farmakologiseen aktiivisuuteen ihmisillä.
Eliminaatio
Suun kautta annetun annoksen jälkeen noin 6% radioaktiivisesti leimatusta annoksesta erittyy virtsaan pääasiassa metaboliitteina (ei yhdisteitä erittyy muuttumattomana virtsaan) ja 84% erittyy ulosteeseen pääasiassa metaboliitteina.Dronedaronin plasmapuhdistuma vaihtelee 130 ... 150 l / h laskimonsisäisen annon jälkeen Dronedaronin lopullinen eliminaation puoliintumisaika on noin 25-30 tuntia ja sen metaboliitin N-debutyylin noin 20-25 tuntia. Potilailla 400 mg kahdesti vuorokaudessa dronedaroni ja sen metaboliitti poistuvat kokonaan plasmasta kahden viikon kuluessa hoidon lopettamisesta.
Erityisryhmät
Dronedaronin farmakokinetiikka AF -potilailla on verrattavissa terveillä koehenkilöillä havaittuun. Sukupuoli, ikä ja paino ovat dronedaronin farmakokinetiikkaan vaikuttavia tekijöitä.
Kullakin näistä tekijöistä on rajallinen "vaikutus dronedaroniin.
Seksi
Naispotilailla altistuminen dronedaronille ja sen metaboliitille N-debutyylille on keskimäärin 1,3-1,9 kertaa suurempi kuin miespotilailla.
Eläkeläiset
Dronedaronin kliinisiin tutkimuksiin osallistuneiden kokonaismäärä koostui 73%: sta 65 -vuotiaista (ja sitä vanhemmista) potilaista ja 34%: sta 75 -vuotiaista (ja sitä vanhemmista) potilaista. Altistukset dronedaronille olivat 23% korkeammat 65 -vuotiailla (ja sitä vanhemmilla) potilailla verrattuna alle 65 -vuotiaisiin potilaisiin.
Maksan vajaatoiminta
Potilailla, joilla oli kohtalainen maksan vajaatoiminta, altistus dronedaronin vapaalle fraktiolle kasvoi kaksinkertaiseksi; aktiivisen metaboliitin altistus pieneni 47% (ks. Kohta 4.2).
Vaikean maksan vajaatoiminnan vaikutusta dronedaronin farmakokinetiikkaan ei ole arvioitu (ks. Kohta 4.3).
Munuaisten vajaatoiminta
Munuaisten vajaatoiminnan vaikutusta dronedaronin farmakokinetiikkaan ei ole arvioitu erityisessä tutkimuksessa. Munuaisten vajaatoiminnan ei odoteta muuttavan dronedaronin farmakokinetiikkaa, koska muuttumattomia yhdisteitä ei eritetä virtsaan ja vain noin 6% annoksesta erittyy virtsaan metaboliitteina (ks. Kohta 4.2).
05.3 Prekliiniset tiedot turvallisuudesta
Perustuu in vivo hiiren mikrotumatestiin ja neljään testiin in vitro, dronedaroni ei osoittanut genotoksisia vaikutuksia.
Kahden vuoden karsinogeenisuustutkimuksissa suurin suun kautta annetun dronedaroniannos 24 kuukauden aikana oli 70 mg / kg / vrk rotalla ja 300 mg / kg / vrk rotalla.
Rintasyövän kasvainten esiintyvyyden lisääntyminen naarashiirillä, histiosyyttinen sarkooma hiirillä ja mesenteriaalisten imusolmukkeiden hemangiooma rotilla havaittiin vain suurimmilla testatuilla annoksilla (mikä vastaa 5-10 kertaa suurempaa altistusta verrattuna terapeuttiseen annokseen ihmisillä) ).
Hemangioomat eivät ole syöpää edeltäviä muutoksia eivätkä muutu pahanlaatuisiksi hemangiosarkoomiksi eläimillä tai ihmisillä. Mitään näistä havainnoista ei pidetty merkityksellisinä ihmisille.
Kroonisia toksisuustutkimuksia havaittiin palautuva ja lievä fosfolipidoosi (vaahtoisten makrofagien kertyminen) mesenterisissä imusolmukkeissa, pääasiassa rotilla. Tätä vaikutusta pidetään lajikohtaisena eikä sillä ole merkitystä ihmisille.
Dronedaroni aiheutti suuria vaikutuksia rotan alkion ja sikiön kehitykseen suurten annosten jälkeen, kuten lisääntynyt istutuksen jälkeinen menetys, vähentynyt sikiön ja istukan paino sekä ulkoiset, sisäelinten ja luuston epämuodostumat.
06.0 FARMASEUTTISET TIEDOT
06.1 Apuaineet
Tablettien ydin:
hypromelloosi (E464),
maissitärkkelys,
krospovidoni (E1202),
poloksameeri 407,
laktoosimonohydraatti,
vedetön kolloidinen piidioksidi,
magnesiumstearaatti (E572).
Tablettien päällystys:
hypromelloosi (E464),
makrogoli 6000,
titaanidioksidi (E171),
karnaubavaha (E903).
06.2 Yhteensopimattomuus
Ei oleellinen.
06.3 Voimassaoloaika
3 vuotta.
06.4 Säilytys
Tämä lääke ei vaadi erityisiä säilytysolosuhteita.
06.5 Välipakkauksen luonne ja pakkauksen sisältö
• Läpinäkymättömät PVC / alumiiniläpipainopakkaukset, joissa on 20, 50, 60 kalvopäällysteistä tablettia
• Läpinäkymätön PVC / alumiiniläpipainopakkaus, perforoitu kerta-annokselle, pakkauksissa, jotka sisältävät 100x1 kalvopäällysteistä tablettia
Kaikkia pakkauskokoja ei välttämättä ole myynnissä.
06.6 Käyttö- ja käsittelyohjeet
Käyttämätön lääke ja tästä lääkkeestä peräisin oleva jäte on hävitettävä paikallisten määräysten mukaisesti.
07.0 MYYNTILUVAN HALTIJA
sanofi-aventis -ryhmä
54, rue La Boétie
F-75008 Pariisi
Ranska
08.0 MYYNTILUVAN NUMERO
EU/1/09/591/001 - 20 kalvopäällysteisen tabletin laatikko
039589015
EU/1/09/591/002 - 50 kalvopäällysteisen tabletin laatikko
039589027
EU/1/09/591/003 - 60 kalvopäällysteisen tabletin laatikko
039589039
EU/1/09/591/004 - Laatikko, jossa 100x1 kalvopäällysteistä tablettia
039589041
09.0 MYYNTILUVAN TAI UUDISTAMISPÄIVÄMÄÄRÄ
Myyntiluvan myöntämisen päivämäärä: 26. marraskuuta 2009
10.0 TEKSTIN MUUTTAMISPÄIVÄMÄÄRÄ
LAUSUNTO 21.3.2017