Vaikuttavat aineet: rituksimabi
MabThera 100 mg infuusiokonsentraatti, liuosta varten
Mabthera -pakkausselosteita on saatavana seuraaviin pakkauskokoihin:- MabThera 100 mg infuusiokonsentraatti, liuosta varten
- MabThera 500 mg infuusiokonsentraatti, liuosta varten
- MabThera 1400 mg liuos ihon alle
Käyttöaiheet Miksi Mabtheraa käytetään? Mitä varten se on?
Mikä on MabThera
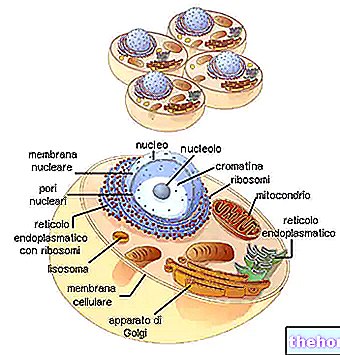
MabThera sisältää vaikuttavana aineena rituksimabia, proteiinityyppiä, jota kutsutaan monoklonaaliseksi vasta -aineeksi ja joka sitoutuu tiettyjen valkosolujen, joita kutsutaan B -lymfosyyteiksi, pintaan. Kun rituksimabi sitoutuu näiden solujen pintaan, se tappaa ne.
Mihin MabTheraa käytetään
MabTheraa voidaan käyttää monien eri sairauksien hoitoon aikuisilla. Lääkärisi voi määrätä MabTheraa seuraavien sairauksien hoitoon:
a) Non-Hodgkinin lymfooma
Non-Hodgkinin lymfooma on imukudoksen (osa immuunijärjestelmää) sairaus, johon liittyy B-lymfosyyttejä, erityinen valkosolutyyppi.
MabTheraa voidaan antaa monoterapiana (yksin) tai yhdessä muiden lääkkeiden kanssa, joita kutsutaan yhdessä kemoterapiaksi.
Potilailla, joiden hoito osoittautuu tehokkaaksi, MabTheraa voidaan käyttää ylläpitohoitona 2 vuoden ajan ensimmäisen hoidon päättymisen jälkeen.
b) Krooninen lymfaattinen leukemia
Krooninen lymfaattinen leukemia (CLL) on yleisin aikuisten leukemian muoto. KLL: ään liittyy erityinen lymfosyytti, B -solu, joka on peräisin luuytimestä ja kypsyy imusolmukkeissa. CLL -potilailla on liikaa epänormaaleja lymfosyyttejä, joista tulee Näiden epänormaalien B -lymfosyyttien lisääntyminen on syynä oireisiisi, joita sinulla saattaa olla. MabThera yhdessä kemoterapian kanssa tuhoaa nämä solut, jotka poistuvat vähitellen kehosta biologisten prosessien avulla.
c) Nivelreuma
MabTheraa käytetään nivelreuman hoitoon Nivelreuma on sairaus, joka vaikuttaa niveliin. B -lymfosyytit ovat vastuussa joistakin oireistasi. MabTheraa käytetään nivelreuman hoitoon ihmisillä, jotka ovat kokeilleet muita lääkkeitä, mutta ovat lakanneet toimimasta, eivät toimineet tarpeeksi hyvin tai aiheuttivat sivuvaikutuksia. MabTheraa käytetään yleensä yhdessä toisen metotreksaatti -nimisen lääkkeen kanssa. ja lisää kykyä suorittaa normaaleja päivittäisiä toimintoja.
Paras vaste MabTheralle on havaittu niillä, joilla on positiivinen verikoe reumatoiditekijän (RF) ja / tai antisyklisen sitrullinoidun peptidin (anti-CCP) suhteen. Molemmat testit ovat yleensä positiivisia nivelreumassa ja auttavat vahvistamaan diagnoosin.
d) Granulomatoosi, johon liittyy polyangiitti ja mikroskooppinen polyangiitti
MabTheraa käytetään granulomatoosin remission indusoimiseen polyangiitin (virallisesti Wegenerin tauti) tai mikroskooppisen polyangiitin yhteydessä yhdessä glukokortikoidien kanssa. mutta voi vaikuttaa myös muihin elimiin.
Vasta -aiheet Milloin Mabtheraa ei saa käyttää
Älä ota MabTheraa
- jos olet allerginen rituksimabille, muille rituksimabin kaltaisille proteiineille tai tämän lääkkeen jollekin muulle aineelle (lueteltu kohdassa 6);
- jos sinulla on "vakava aktiivinen infektio"
- jos immuunijärjestelmäsi on heikko;
- jos sinulla on vaikea sydämen vajaatoiminta tai vaikea hallitsematon sydänsairaus ja sinulla on nivelreuma, granulomatoosi ja polyangiitti tai mikroskooppinen polyangiitti.
Älä ota MabTheraa, jos jokin yllä olevista koskee sinua. Jos olet epävarma, keskustele lääkärin, apteekkihenkilökunnan tai sairaanhoitajan kanssa ennen kuin sinulle annetaan MabTheraa.
Käyttöä koskevat varotoimet Mitä sinun on tiedettävä, ennen kuin otat Mabtheraa
Keskustele lääkärin, apteekkihenkilökunnan tai sairaanhoitajan kanssa ennen kuin sinulle annetaan MabTheraa:
- jos sinulla on aiemmin ollut tai saattaa olla hepatiitti -infektio, kuten muutamissa tapauksissa MabThera saattaa aiheuttaa B -hepatiitin aktivoitumisen uudelleen, mikä voi hyvin harvoissa tapauksissa johtaa kuolemaan. Lääkäri seuraa tarkoin potilaita, joilla on ollut hepatiitti B -infektio, mahdollisen infektion merkkien varalta.
- jos sinulla on joskus ollut sydänvaivoja (kuten angina pectoris, sydämentykytys tai sydämen vajaatoiminta) tai sinulla on ollut hengitysvaikeuksia.
Jos jokin edellä mainituista koskee sinua (tai jos olet epävarma), keskustele lääkärin, apteekkihenkilökunnan tai sairaanhoitajan kanssa ennen kuin sinulle annetaan MabTheraa.
Jos sinulla on nivelreuma, granulomatoosi ja polyangiitti tai mikroskooppinen polyangiitti, keskustele lääkärisi kanssa
- jos luulet, että sinulla on infektio, jopa lievä kuin vilustuminen MabThera -soluja käytetään infektioiden torjuntaan ja sinun on odotettava, kunnes infektio on poistunut, ennen kuin otat MabTheraa. Kerro myös lääkärillesi, jos sinulla on ollut useita infektioita tai jos sinulla on vakavia infektioita;
- jos luulet tarvitsevasi rokotuksia lähitulevaisuudessa, mukaan lukien muihin maihin matkustamiseen tarvittavat rokotukset Joitakin rokotteita ei pidä antaa samanaikaisesti MabTheran kanssa tai kuukausina MabTheran ottamisen jälkeen. Lääkäri harkitsee, voitko ottaa rokotteita ennen MabTheran ottamista.
Lapset ja nuoret
Keskustele lääkärin, apteekkihenkilökunnan tai sairaanhoitajan kanssa ennen tämän lääkkeen antamista, jos sinä tai lapsesi olet alle 18 -vuotiaita, koska tällä hetkellä ei ole paljon tietoa MabTheran käytöstä lapsille ja nuorille.
Yhteisvaikutukset Mitkä lääkkeet tai elintarvikkeet voivat muuttaa Mabtheran vaikutusta
Kerro lääkärille, apteekkihenkilökunnalle tai sairaanhoitajalle, jos parhaillaan käytät, olet äskettäin käyttänyt tai saatat käyttää muita lääkkeitä, myös reseptilääkkeitä ja yrttilääkkeitä, koska MabThera voi vaikuttaa joidenkin lääkkeiden toimintaan ja päinvastoin.
Kerro lääkärille erityisesti:
- jos käytät verenpainelääkkeitä Sinua saatetaan pyytää lopettamaan näiden lääkkeiden käyttö 12 tunniksi ennen MabTheran ottamista, koska joillakin ihmisillä verenpaine laskee MabTheran käytön aikana;
- jos olet aiemmin käyttänyt immuunijärjestelmään vaikuttavia lääkkeitä, kuten kemoterapiaa tai immunosuppressiivisia lääkkeitä.
Jos jokin edellä mainituista koskee sinua (tai olet epävarma), keskustele lääkärin, apteekkihenkilökunnan tai sairaanhoitajan kanssa ennen kuin sinulle annetaan MabTheraa.
Varoitukset On tärkeää tietää, että:
Raskaus, imetys ja hedelmällisyys
Kerro lääkärille tai sairaanhoitajalle, jos olet raskaana, epäilet tai suunnittelet raskautta, koska MabThera voi läpäistä istukan ja vaikuttaa lapseen.
Jos on mahdollista, että tulet raskaaksi, sinun ja kumppanisi on käytettävä tehokasta ehkäisyä MabThera -hoidon aikana ja 12 kuukauden kuluessa viimeisen MabThera -hoidon saamisesta.
MabThera voi erittyä rintamaitoon, joten sinun ei tule imettää tämän lääkkeen käytön aikana etkä 12 kuukauteen viimeisen MabThera-hoidon jälkeen.
Ajaminen ja koneiden käyttö
Ei tiedetä, vaikuttaako MabThera ajokykyyn ja koneiden käyttökykyyn.
Annostus ja käyttötapa Mabtheran käyttö: Annostus
Hallinto
MabTheraa antaa sinulle lääkäri tai sairaanhoitaja, jolla on kokemusta tämän hoidon käytöstä.He seuraavat sinua tarkasti tämän lääkkeen antamisen aikana haittavaikutusten havaitsemiseksi.
MabThera annetaan aina tipoittain infuusiona laskimoon (laskimonsisäinen infuusio).
Ennen jokaista MabThera -infuusiota annettavat lääkkeet
Sinulle annetaan muita lääkkeitä (esilääkitystä) ennen MabThera -infuusiota mahdollisten haittavaikutusten välttämiseksi tai vähentämiseksi.
Kuinka paljon ja kuinka usein saat hoitoa
a) Jos saat hoitoa non-Hodgkinin lymfoomaan
- Jos sinulle annetaan vain MabTheraa
MabTheraa annetaan sinulle kerran viikossa 4 viikon ajan. Toistuvat MabThera -hoitojaksot ovat mahdollisia.
- Jos sinulle annetaan MabTheraa yhdessä kemoterapian kanssa
Saat MabTheraa samana päivänä, kun saat kemoterapiaa; niiden antaminen tapahtuu yleensä 3 viikon välein enintään 8 kertaa
- Jos hoito reagoi hyvin, MabTheraa voidaan antaa ylläpitohoitona 2-3 kuukauden välein kahden vuoden ajan. Lääkärisi voi muuttaa tätä lääkehoitoa lääkevasteesi perusteella.
b) jos saat kroonisen lymfaattisen leukemian hoitoa
Jos saat MabTheraa yhdessä kemoterapian kanssa, saat MabThera -infuusioita syklin 1 päivänä 0 ja sitten kunkin syklin päivänä yhteensä 6 jaksoa. Jokainen sykli kestää 28 päivää. MabThera -infuusion jälkeen tulee antaa solunsalpaajahoitoa, ja lääkäri päättää, saatko samanaikaista tukihoitoa.
c) jos saat nivelreuman hoitoa
Jokainen hoitojakso koostuu kahdesta erillisestä infuusiosta, jotka annetaan kahden viikon välein. Toistuvat MabThera -hoitojaksot ovat mahdollisia. Lääkärisi päättää sairautesi merkkien ja oireiden perusteella, milloin sinulle annetaan kursseja. Tämä voi tapahtua useita kuukausia.
d) jos saat granulomatoosihoitoa polyangiitilla tai mikroskooppisella polyangiitilla
MabThera -hoito sisältää neljä erillistä infuusiota viikoittain. Kortikosteroideja annetaan injektiona ennen MabThera -hoidon aloittamista. Lääkäri voi milloin tahansa aloittaa suun kautta otettavan kortikosteroidiannon sairautesi hoitamiseksi.
Jos sinulla on kysymyksiä tämän lääkkeen käytöstä, käänny lääkärin, apteekkihenkilökunnan tai sairaanhoitajan puoleen.
Sivuvaikutukset Mitkä ovat Mabtheran sivuvaikutukset
Kuten kaikki lääkkeet, tämäkin lääke voi aiheuttaa haittavaikutuksia. Kaikki eivät kuitenkaan niitä saa.
Useimmat haittavaikutukset ovat lieviä tai kohtalaisia, mutta joissakin tapauksissa ne voivat olla vakavia ja vaatia hoitoa. Jotkut näistä reaktioista ovat harvoin olleet kuolemaan johtavia.
Infuusioreaktiot
Ensimmäisen infuusion aikana tai kahden ensimmäisen tunnin aikana sen jälkeen voi kehittyä kuumetta, vilunväristyksiä ja vapinaa. Joillakin potilailla saattaa harvemmin olla kipua infuusiokohdassa, rakkuloita, ihon kutinaa, huonovointisuutta, väsymystä, päänsärkyä, hengitysvaikeuksia, kielen tai kurkun turpoamista, ärsytystä tai vuotavaa nenää, oksentelua, lämpimän tai lämpimän tunteen sydämentykytystä, sydänkohtausta tai verihiutaleiden määrässä. Jos sinulla on sydänsairaus tai angina pectoris, nämä reaktiot voivat pahentua. Jos sinulla ilmenee jokin näistä oireista, kerro siitä välittömästi infuusiota antavalle henkilölle, koska infuusionopeutta on ehkä hidastettava tai se on lopetettava. Lisähoitoa voidaan tarvita, esimerkiksi antihistamiinilla tai parasetamolilla. infuusio voidaan jatkaa. Näitä reaktioita esiintyy harvemmin toisen infuusion jälkeen. Lääkäri voi päättää lopettaa MabThera -hoidon, jos nämä reaktiot ovat vakavia.
Infektiot
Kerro heti lääkärille, jos sinulla on infektion merkkejä, mukaan lukien:
- kuume, yskä, kurkkukipu, polttaminen virtsatessa, heikko olo tai yleinen huonovointisuus
- muistin heikkeneminen, ahdistunut ajattelu, kävelyvaikeudet tai näön menetys - nämä voivat johtua hyvin harvinaisesta vakavasta kuolemaan johtaneesta infektiosta (etenevä multifokaalinen leukoenkefalopatia tai PML). Saatat kehittää infektioita helpommin MabThera -hoidon aikana.
- Nämä ovat usein vilustumista, mutta keuhkokuumetta tai virtsatietulehduksia on esiintynyt. Nämä olosuhteet on lueteltu alla olevassa "Muut haittavaikutukset" -luettelossa.
Jos sinua hoidetaan nivelreumasta, löydät nämä tiedot myös lääkärisi antamasta potilaskortista. On tärkeää, että pidät tämän hälytyskortin mukanasi ja näytät sen perheenjäsenellesi muista huolehtia hänestä.
Ihon reaktiot
Hyvin harvoin voi esiintyä vakavia ihoreaktioita, joihin liittyy rakkuloita ja jotka voivat olla hengenvaarallisia. Iholla tai limakalvoilla, kuten suun sisällä, sukuelinten alueella tai silmäluomien alueella, voi esiintyä punoitusta, johon usein liittyy rakkuloita, ja kuumetta voi esiintyä. Kerro lääkärillesi heti, jos saat jonkin näistä oireista.
Muut haittavaikutukset
a) jos saat hoitoa non-Hodgkinin lymfoomaan tai krooniseen lymfaattiseen leukemiaan
Hyvin yleiset haittavaikutukset (voi esiintyä useammalla kuin yhdellä henkilöllä 10: stä):
- bakteeri- tai virusinfektiot, keuhkoputkentulehdus
- alhainen valkosolujen määrä, johon voi liittyä kuumetta tai ilman, tai verihiutaleet (verisolut)
- pahoinvointi
- päänahan kaljuuntuminen, vilunväristykset, päänsärky
- immuunijärjestelmän heikkeneminen - johtuen tiettyjen immunoglobuliinien (IgG) vasta -aineiden määrän vähenemisestä veressä, jotka auttavat kehoa suojautumaan infektioilta.
Yleiset haittavaikutukset (voi esiintyä enintään 1 käyttäjällä 10: stä):
- veri -infektiot (sepsis), keuhkokuume, vyöruusu, vilustuminen, keuhkoputkitulehdus, sieni -infektiot, tuntemattomat infektiot, sinuiitti, hepatiitti B
- alhainen punasolujen määrä (anemia), alhainen kaikkien verisolujen määrä
- allergiset reaktiot (yliherkkyys)
- korkea verensokeri, laihtuminen, kasvojen ja vartalon turvotus, korkea "LDH -entsyymin" pitoisuus veressä, alhainen veren kalsiumpitoisuus
- epänormaalit tuntemukset iholla - kuten tunnottomuus, pistely, pistely, polttaminen, venytetyn ihon tunne, heikentynyt kosketus
- levottomuuden tunne, nukahtamisvaikeudet
- kasvojen ja muiden ihoalueiden voimakas punoitus verisuonten laajentumisen seurauksena
- huimausta tai ahdistusta
- lisääntynyt kyynelvuoto, kyynelkanavaongelmat, silmätulehdus (sidekalvotulehdus)
- jatkuva soiminen korvissa, kipu korvassa
- sydänongelmat - kuten sydänkohtaus, epäsäännöllinen tai nopea syke
- korkea tai matala verenpaine (verenpaineen lasku erityisesti seisoessa)
- hengitysteiden lihasten supistuminen, joka aiheuttaa hengityksen vinkumista (bronkospasmi), tulehdus, ärsytys keuhkoissa, kurkussa ja poskionteloissa, hengenahdistus, vuotava nenä
- oksentelu, ripuli, vatsakipu, kurkun ja suun ärsytys tai haavaumat, nielemisongelmat, ummetus, ruoansulatushäiriöt
- syömishäiriöt: riittämätön ruokavalio, joka johtaa laihtumiseen
- nokkosihottuma, lisääntynyt hikoilu, yöhikoilu
- lihasongelmat - kuten lihasjäykkyys, nivel- tai lihaskipu, selkä- ja niskakipu
- yleinen huonovointisuus, levottomuus tai väsymys, vapina, flunssan merkit
- monielinvika.
Melko harvinaiset haittavaikutukset (voi esiintyä enintään 1 käyttäjällä 100: sta):
- hyytymisongelmat, vähentynyt punasolujen tuotanto ja lisääntynyt punasolujen tuhoutuminen (hemolyyttinen ja aplastinen anemia), imusolmukkeiden turvotus tai laajentuminen
- heikko mieliala ja kiinnostuksen tai nautinnon menettäminen, hermostuneisuus
- makuun liittyvät ongelmat - kuten makuaistin muutokset
- sydänongelmat - kuten hidas syke tai rintakipu (angina pectoris)
- astma, riittämätön hapen määrä elimistöön
- vatsan turvotus.
Hyvin harvinaiset haittavaikutukset (voi esiintyä enintään 1 käyttäjällä 10000: sta):
- tietyntyyppisten vasta -aineiden (immunoglobuliinit - IgM) määrän lyhytaikainen lisääntyminen veressä, veren kemiallinen muutos kuolevien syöpäsolujen hajoamisesta johtuen
- käsivarsien ja jalkojen hermojen vaurioituminen, kasvojen halvaantuminen
- sydämen vajaatoiminta
- verisuonitulehdus, mukaan lukien iho -oireita aiheuttavat
- hengitysvajaus
- suolen seinämän vaurio (perforaatio)
- vakavia iho -ongelmia rakkuloiden kanssa, mahdollisesti kuolemaan johtavia. Iholla tai limakalvoilla, kuten suun, sukupuolielinten tai silmäluomien pinnalla, voi esiintyä punoitusta, johon usein liittyy rakkuloita, ja kuumetta.
- munuaisten vajaatoiminta
- vakava näön menetys.
Tuntematon (näiden haittavaikutusten esiintymistiheyttä ei tunneta):
- ei-välitön valkosolujen väheneminen
- verihiutaleiden määrän väheneminen pian infuusion jälkeen - palautuva tila, mutta harvinaisissa tapauksissa hengenvaarallinen
- kuulon menetys, muiden aistien menetys.
b) jos sinua hoidetaan nivelreumasta
Hyvin yleiset haittavaikutukset (voi esiintyä useammalla kuin yhdellä henkilöllä 10: stä):
- infektiot, kuten keuhkokuume (bakteeri)
- kipu virtsatessa (virtsatieinfektio)
- allergisia reaktioita, joita todennäköisesti esiintyy infuusion aikana, mutta jotka voivat ilmetä jopa 24 tuntia infuusion jälkeen
- verenpaineen muutokset, pahoinvointi, ihottuma, kuume, kutiava tunne, vuotava tai tukkoinen nenä, aivastelu, vapina, nopea syke ja väsymys
- päänsärky
- muutokset lääkärin edellyttämissä laboratoriokokeissa. Näitä ovat esimerkiksi tiettyjen erityisten proteiinien (immunoglobuliinien) määrän väheneminen, jotka auttavat suojautumaan infektioilta.
Yleiset haittavaikutukset (voi esiintyä enintään 1 käyttäjällä 10: stä):
- infektiot, kuten keuhkoputkitulehdus (keuhkoputkentulehdus)
- kipu ja täyteyden tunne nenän, poskien ja silmien takana (sinuiitti), vatsakipu, oksentelu ja ripuli, hengitysvaikeudet
- jalkojen sieni -infektio (urheilijan jalka)
- korkea veren kolesterolitaso
- epänormaalit tuntemukset iholla, kuten tunnottomuus, pistely, pistely tai polttaminen, iskias, migreeni, huimaus
- hiustenlähtö
- ahdistus, masennus
- ruoansulatushäiriöt, ripuli, hapon refluksointi, kurkun ja suun ärsytys ja / tai haavaumat
- kipu vatsassa, selässä, lihaksissa ja / tai nivelissä.
Melko harvinaiset haittavaikutukset (voi esiintyä enintään 1 käyttäjällä 100: sta):
- ylimääräinen nesteen kertyminen kasvoihin ja vartaloon
- tulehdus, ärsytys ja / tai jännitys keuhkoissa, kurkussa, yskä
- ihoreaktiot, mukaan lukien nokkosihottuma, kutina, ihottuma
- allergiset reaktiot, mukaan lukien hengityksen vinkuminen tai hengenahdistus, kasvojen ja kielen turvotus, romahtaminen.
Hyvin harvinaiset haittavaikutukset (voi esiintyä enintään 1 käyttäjällä 10000: sta):
- oireyhtymä, joka ilmenee muutaman viikon kuluessa MabThera-infuusiosta, mukaan lukien allergiset reaktiot, kuten ihottuma, kutina, nivelkivut, imusolmukkeiden turvotus ja kuume
- vakavia ihoreaktioita ja rakkuloita, jotka voivat olla hengenvaarallisia. Iholla tai limakalvoilla, kuten suun sisällä, sukuelinten alueella tai silmäluomien alueella, voi esiintyä punoitusta, johon usein liittyy rakkuloita, ja kuumetta voi esiintyä.
Muita harvoin raportoituja MabThera -hoidon sivuvaikutuksia ovat infektioiden torjumiseen käytettävien valkosolujen (neutrofiilien) määrän väheneminen. Jotkut infektiot voivat olla vakavia (katso tämän osan infektiotiedot).
c) jos saat granulomatoosihoitoa polyangiitilla tai mikroskooppista polyangiittia
Hyvin yleiset haittavaikutukset (voi esiintyä useammalla kuin yhdellä henkilöllä 10: stä):
- infektiot, kuten keuhkoinfektiot, virtsatieinfektiot (kivulias virtsaaminen), vilustuminen ja herpesinfektiot
- allergisia reaktioita, joita todennäköisesti esiintyy infuusion aikana, mutta jotka voivat ilmetä jopa 24 tuntia infuusion jälkeen
- ripuli
- yskä tai hengenahdistus
- nenäverenvuoto
- kohonnut verenpaine
- kipu nivelissä tai selässä
- lihasten nykiminen tai vapina
- huimata
- vapina (vapina, usein käsissä)
- unihäiriöt (unettomuus)
- käsien ja nilkkojen turvotus.
Yleiset haittavaikutukset (voi esiintyä enintään 1 käyttäjällä 10: stä):
- ruoansulatushäiriöt
- ummetus
- ihottumat, mukaan lukien akne tai viat
- ihon punoitus tai punoitus
- tukkoinen nenä
- lihasjäykkyys tai lihaskipu
- kipu lihaksissa tai käsissä tai jaloissa
- alhainen punasolujen määrä (anemia)
- alhainen verihiutaleiden määrä veressä lisää kaliumia veressä
- sydämen rytmin tai sykkeen muutokset normaalia nopeammin.
Hyvin harvinaiset haittavaikutukset (voi esiintyä enintään 1 käyttäjällä 10000: sta):
- vakavia ihoreaktioita ja rakkuloita, jotka voivat olla hengenvaarallisia. Iholla tai limakalvoilla, kuten suun, sukupuolielinten tai silmäluomien pinnalla, voi esiintyä punoitusta, johon usein liittyy rakkuloita, ja kuumetta.
- aiemman hepatiitti B -infektion uusiutuminen.
MabThera voi myös aiheuttaa muutoksia lääkärisi edellyttämiin laboratoriokokeisiin.
Jos käytät MabTheraa yhdessä muiden lääkkeiden kanssa, osa haittavaikutuksista saattaa johtua muista lääkkeistä.
Sivuvaikutusten ilmoittaminen
Jos havaitset haittavaikutuksia, käänny lääkärin, apteekkihenkilökunnan tai sairaanhoitajan puoleen. Tämä koskee myös kaikkia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Voit ilmoittaa haittavaikutuksista myös suoraan liitteessä V luetellun kansallisen ilmoitusjärjestelmän kautta. antaa lisätietoja tämän lääkkeen turvallisuudesta.
Vanhentuminen ja säilyttäminen
Ei lasten ulottuville eikä näkyville.
Älä käytä tätä lääkettä pakkauksessa mainitun viimeisen käyttöpäivämäärän (EXP) jälkeen. Viimeinen käyttöpäivä viittaa kuukauden viimeiseen päivään.
Säilytä jääkaapissa (2 ° C - 8 ° C). Säilytä säiliö ulkopakkauksessa valolta suojaamiseksi.
Älä heitä lääkkeitä viemäriin tai talousjätteisiin. Kysy apteekista, kuinka heittää pois lääkkeet, joita et enää käytä. Tämä auttaa suojelemaan ympäristöä.
Mitä MabThera sisältää
- MabTheran vaikuttava aine on rituksimabi. Injektiopullo sisältää 100 mg rituksimabia (10 mg / ml).
- Muut aineet ovat natriumsitraatti, polysorbaatti 80, natriumkloridi, natriumhydroksidi, suolahappo ja injektionesteisiin käytettävä vesi.
Miltä MabThera näyttää ja pakkauksen sisältö
MabThera on kirkas ja väritön liuos, joka toimitetaan infuusiokonsentraattina. 10 ml: n injektiopullot ovat saatavana 2 injektiopullon pakkauksissa.
Lähdepakkaus: AIFA (Italian lääkevirasto). Sisältö julkaistu tammikuussa 2016. Esitetyt tiedot eivät välttämättä ole ajan tasalla.
Jotta saat käyttöösi uusimman version, on suositeltavaa käyttää AIFA: n (Italian Medicines Agency) verkkosivustoa. Vastuuvapauslauseke ja hyödyllistä tietoa.
01.0 LÄÄKEVALMISTEEN NIMI
MABTHERA 100 MG KONSENTRAATTI infuusionestettä varten, liuos
02.0 LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS
Yksi ml sisältää 10 mg rituksimabia.
Yksi injektiopullo sisältää 100 mg rituksimabia.
Rituksimabi on geneettisesti muokattu kimeerinen hiiren / ihmisen monoklonaalinen vasta -aine, joka koostuu glykosyloidusta immunoglobuliinista, jossa on ihmisen IgG1 -vakioalueet ja hiiren kevytketjun ja raskaan ketjun vaihtelevan alueen sekvenssit.
Vasta -aine tuotetaan käyttämällä nisäkässolususpensioviljelmää (kiinanhamsterin munasarja) ja puhdistetaan affiinikromatografialla ja ioninvaihdolla, mukaan lukien erityiset virusten inaktivointi- ja poistomenettelyt.
Täydellinen apuaineluettelo, katso kohta 6.1.
03.0 LÄÄKEMUOTO
Infuusiokonsentraatti, liuosta varten.
Kirkas ja väritön neste.
04.0 KLIINISET TIEDOT
04.1 Käyttöaiheet
MabThera on tarkoitettu aikuisille seuraaviin käyttöaiheisiin:
Non-Hodgkinin lymfooma (NHL)
MabThera on tarkoitettu hoitoon aiemmin hoitamattomille potilaille, joilla on vaiheen III-IV follikulaarinen lymfooma yhdessä kemoterapian kanssa.
MabThera -ylläpitohoito on tarkoitettu follikulaarisen lymfooman potilaiden hoitoon, jotka reagoivat induktiohoitoon.
MabThera-monoterapia on tarkoitettu potilaiden hoitoon, joilla on vaiheen III-IV follikulaarinen lymfooma, jotka ovat kemoterapiaresistenttejä tai joilla on toinen tai myöhempi uusiutuminen kemoterapian jälkeen.
MabThera on tarkoitettu potilaille, joilla on CD20-positiivinen diffuusi suurisoluinen non-Hodgkin-lymfooma yhdessä CHOP-solunsalpaajahoidon (syklofosfamidi, doksorubisiini, vinkristiini, prednisoloni) kanssa.
Krooninen lymfaattinen leukemia (CLL)
MabThera yhdessä kemoterapian kanssa on tarkoitettu potilaiden hoitoon, joilla on aiemmin hoitamaton ja uusiutunut / tulenkestävä krooninen lymfaattinen leukemia. Tehosta ja turvallisuudesta on vain vähän tietoja potilaista, jotka ovat aiemmin saaneet monoklonaalisia vasta -aineita, mukaan lukien MabThera, tai potilaista, jotka eivät ole aikaisempia MabThera plus -hoitoja.
Katso lisätietoja kohdasta 5.1.
Nivelreuma
MabThera yhdessä metotreksaatin kanssa on tarkoitettu vaikean aktiivisen nivelreuman hoitoon aikuispotilaille, jotka ovat osoittaneet "riittämättömän vasteen" tai suvaitsemattomuuden muihin sairautta modifioiviin reumalääkkeisiin, mukaan lukien yksi tai useampi tuumorinekroositekijän estäjä. (TNF).
MabTheran on osoitettu vähentävän nivelvaurioiden etenemistä röntgensäteillä arvioituna ja parantavan fyysistä toimintaa, kun sitä annetaan yhdessä metotreksaatin kanssa.
Granulomatoosi, johon liittyy polyangiitti ja mikroskooppinen polyangiitti
MabThera yhdessä glukokortikoidien kanssa on tarkoitettu remission indusoimiseksi aikuispotilaille, joilla on granulomatoosi (Wegenerin) polyangiitti (GPA) ja vaikea aktiivinen mikroskooppinen polyangiitti (MPA).
04.2 Annostus ja antotapa
MabThera tulee antaa kokeneen terveydenhuollon ammattilaisen tarkassa valvonnassa ja ympäristössä, jossa elvytyslaitteet ovat heti saatavilla (ks. Kohta 4.4).
Esilääkitys kuumetta alentavalla lääkkeellä ja antihistamiinilla, esimerkiksi parasetamolilla ja difenhydramiinilla, on aina otettava ennen jokaista MabTheran antoa.
Potilailla, joilla on non-Hodgkinin lymfooma ja krooninen lymfaattinen leukemia (CLL), esilääkitystä glukokortikoideilla on harkittava, jos MabTheraa ei anneta yhdessä glukokortikoideja sisältävän solunsalpaajahoidon kanssa.
Potilailla, joilla on nivelreuma, esilääkitys laskimonsisäisellä metyyliprednisolonilla 100 mg on saatettava päätökseen 30 minuuttia ennen MabThera-infuusiota infuusioon liittyvien reaktioiden (IRR) ilmaantuvuuden ja vakavuuden vähentämiseksi.
Potilaille, jotka kärsivät granulomatoosista, johon liittyy polyangiitti (Wegenerin tauti) tai mikroskooppinen polyangiitti, suositellaan laskimonsisäistä metyyliprednisoloniannosta 1000 mg / vrk 1-3 päivän ajan ennen ensimmäistä MabThera -infuusiota (viimeinen metyyliprednisoloniannos voidaan antaa samana päivänä ensimmäisen MabThera -infuusion jälkeen) Tämän jälkeen on annettava suun kautta annettavaa prednisonia annoksella 1 mg / kg / vrk (80 mg / vrk ei saa ylittää ja asteittainen pienentäminen on tehtävä mahdollisimman nopeasti kliinisestä tilasta riippuen). ja MabThera -hoidon jälkeen.
Annostus
& EGRAVE; On tärkeää tarkistaa lääkkeen etiketti varmistaakseen, että sopiva formulaatio (laskimonsisäinen tai ihonalainen) annetaan potilaalle määräyksen mukaisesti.
Non-Hodgkinin lymfooma
Follikulaarinen non-Hodgkinin lymfooma
Yhdistyshoito
Suositeltu MabThera -annos yhdessä kemoterapian kanssa aikaisemmin hoitamattomien tai uusiutuneiden / refraktaaristen potilaiden, joilla on follikulaarinen lymfooma, induktiohoitoon on 375 mg / m2 kehon pinta -alaa sykliä kohti, enintään 8 sykliä.
MabThera tulee antaa jokaisen solunsalpaajahoitojakson päivänä 1 i.v. kemoterapian glukokortikoidikomponentti tarvittaessa.
Ylläpitohoito
• Aiemmin hoitamaton follikulaarinen lymfooma
Suositeltu MabThera -annos ylläpitohoitona aiemmin hoitamattomille follikulaarista lymfoomaa sairastaville potilaille, jotka ovat tehonneet induktiohoitoon, on: 375 mg / m2 kehon pinta -alaa kerran kahdessa kuukaudessa (alkaen 2 kuukautta viimeisen hoitoannoksen jälkeen). etenemistä tai enintään kahden vuoden ajan.
• Uusiutunut / tulenkestävä follikulaarinen lymfooma
Suositeltu MabThera -annos, jota käytetään ylläpitohoitona potilaille, joilla on uusiutunut / resistentti follikulaarinen lymfooma ja jotka ovat vastanneet induktiohoitoon, on 375 mg / m2 kehon pinta -alaa kerran kolmessa kuukaudessa (alkaen 3 kuukautta viimeisen hoitoannoksen jälkeen). taudin etenemistä tai enintään kahden vuoden ajan.
Monoterapia
• Uusiutunut / tulenkestävä follikulaarinen lymfooma
Suositeltu MabThera-monoterapian annos, jota käytetään induktiohoitona aikuispotilaille, joilla on vaiheen III-IV follikulaarinen lymfooma ja jotka ovat kemoresistenttejä tai jotka ovat toisessa tai myöhemmässä uusiutumisessa kemoterapian jälkeen, on 375 mg / m2 kehon pinta-alaa laskimoinfuusiona. kerran viikossa neljän viikon ajan.
Jos MabThera -monoterapiaa käytetään uudelleen potilaille, jotka ovat tehonneet aiempaan MabThera -monoterapiahoitoon uusiutuneen / tulenkestävän follikulaarisen lymfooman hoitoon, suositeltu annos on 375 mg / m2 kehon pinta -alaa laskimoinfuusiona kerran viikossa neljän viikon ajan (ks. Kohta 5.1). ).
Diffuusiinen suuri B-solun non-Hodgkinin lymfooma
MabTheraa on käytettävä yhdessä CHOP -solunsalpaajahoidon kanssa. Suositeltu annos on 375 mg / m2 kehon pinta -alaa, joka annetaan jokaisen solunsalpaajahoidon ensimmäisenä päivänä 8 syklin ajan CHOP: n glukokortikoidikomponentin laskimonsisäisen infuusion jälkeen. MabTheran turvallisuutta ja tehoa yhdessä muiden solunsalpaajahoitojen kanssa diffuusissa suurten B-solujen non-Hodgkin-lymfoomassa ei ole vielä varmistettu.
Annoksen säätö hoidon aikana
MabTheran annoksen pienentämistä ei suositella. Kun MabTheraa annetaan yhdessä solunsalpaajahoidon kanssa, kemoterapialääkkeiden tavanomaisia annoksia on pienennettävä.
Krooninen lymfaattinen leukemia
Ennaltaehkäisyä riittävällä nesteytyksellä ja urikostaattien antamisella, joka alkaa 48 tuntia ennen hoidon aloittamista, suositellaan CLL -potilaille kasvainlyysioireyhtymän riskin pienentämiseksi.LLL -potilaille, joiden lymfosyyttimäärä on> 25 x 109 / l, on suositeltavaa antaa prednisonia / 100 mg prednisolonia laskimoon juuri ennen MabThera -infuusiota akuuttien infuusioreaktioiden ja / tai sytokiinien vapautumisoireyhtymän nopeuden ja vakavuuden vähentämiseksi.
Suositeltu MabThera -annos yhdessä kemoterapian kanssa aikaisemmin hoitamattomille ja uusiutuneille / tulenkestäville potilaille on 375 mg / m2 kehon pinta -alaa ensimmäisen hoitojakson päivänä 0, jota seuraa 500 mg / m2 kehon pinta -ala jokaisen seuraavan hoitopäivän päivänä 1 sykli yhteensä 6 sykliä. Kemoterapia tulee antaa MabThera -infuusion jälkeen.
Nivelreuma
MabTheraa saaville potilaille tulee antaa potilaskortti jokaisen infuusion yhteydessä.
MabThera -hoito koostuu kahdesta 1000 mg: n laskimonsisäisestä infuusiosta. Suositeltu MabThera -annos on 1000 mg laskimoinfuusiona, jota seuraa toinen 1000 mg: n laskimonsisäinen infuusio kahden viikon kuluttua.
Lisähoidon tarve on arvioitava 24 viikkoa edellisen syklin jälkeen. Uudelleenhoito on suoritettava tuolloin, jos taudin jäännösaktiivisuus säilyy, muutoin uudelleenhoitoa tulee lykätä, kunnes taudin jäännösaktiivisuus ilmenee uudelleen.
Käytettävissä olevat tiedot viittaavat siihen, että kliininen vaste saavutetaan yleensä 16-24 viikon kuluessa ensimmäisestä hoitojaksosta. Potilailla, jotka eivät näe terapeuttista hyötyä tänä aikana, on harkittava huolellisesti, jatketaanko hoitoa.
Granulomatoosi, johon liittyy polyangiitti ja mikroskooppinen polyangiitti
MabTheralla hoidetuille potilaille on annettava potilaskortti jokaisen infuusion yhteydessä.
Suositeltu MabThera -annos granulomatoosin remission induktioterapiassa polyangiitin ja mikroskooppisen polyangiitin kanssa on 375 mg / m2 kehon pinta -alasta laskimoinfuusiona kerran viikossa 4 viikon ajan (yhteensä 4 infuusiota).
Potilaille, joilla on granulomatoosi, polyangiitti ja mikroskooppinen polyangiitti, MabThera -hoidon aikana ja sen jälkeen suositellaan keuhkokuumeen ehkäisyä. Pneumocystis jiroveci, (PCP), tapauksen mukaan.
Erityisryhmät
Pediatriset potilaat
MabTheran turvallisuutta ja tehoa lapsille ja alle 18 -vuotiaille nuorille ei ole vielä varmistettu.Tietoja ei ole saatavilla.
Iäkkäät potilaat
Annosta ei tarvitse muuttaa iäkkäille potilaille (> 65 -vuotiaat).
Antotapa
Valmis MabThera -liuos tulee antaa infuusiona laskimoon erityistä linjaa pitkin. Sitä ei saa antaa laskimonsisäisenä painalluksena tai boluksena. Potilaita on seurattava huolellisesti sytokiinien vapautumisoireyhtymän varalta (ks. Kohta 4.4) .Potilaille, joille kehittyy vakavia reaktioita, erityisesti vaikeaa hengenahdistusta, bronkospasmia tai hypoksiaa, infuusio on lopetettava välittömästi. Non-Hodgkin-lymfoomaa sairastavat potilaat tulee sitten arvioida kasvaimen hajoamisoireyhtymän esiintymisen varalta suorittamalla asianmukaiset laboratoriokokeet ja keuhkoinfiltraation esiintyminen rintakehän röntgenkuvauksella.Kaikilla potilailla infuusiota ei saa jatkaa ennen kuin kaikki oireet ja laboratorioarvojen normalisointi sekä rintakehän röntgenkuvaus. Vasta sen jälkeen infuusiota voidaan jatkaa alkuperäisellä nopeudella, joka on vähennetty puoleen aikaisemmin käytetystä.
Lievät tai kohtalaiset infuusioon liittyvät reaktiot (ks. Kohta 4.8) vastaavat yleensä infuusionopeuden hidastumiseen, kun oireet paranevat, infuusionopeutta voidaan lisätä.
Ensimmäinen infuusio
Suositeltu ensimmäinen infuusionopeus on 50 mg / h; ensimmäisten 30 minuutin jälkeen sitä voidaan nostaa 50 mg / h välein 30 minuutin välein, enintään 400 mg / h.
Seuraavat infuusiot
Kaikille käyttöaiheille
Seuraavat MabThera -annokset voidaan antaa alkuinfuusionopeudella 100 mg / h ja lisätä 100 mg / h 30 minuutin välein, enintään 400 mg / h.
Vain nivelreumalle
Vaihtoehtoinen järjestelmä seuraavien infuusioiden nopeampaa antamista varten
Jos potilailla ei ole ilmennyt vakavaa infuusioon liittyvää reaktiota ensimmäisellä tai seuraavilla infuusioilla, jotka annetaan MabTheran 1000 mg: n annoksella tavanomaisen infuusio-ohjelman mukaisesti, toinen ja seuraavat infuusiot voidaan antaa nopeammin, samalla nopeudella edellisten infuusioiden pitoisuus (4 mg / ml 250 ml: n tilavuudelle).
Aloita infuusio nopeudella 250 mg / h ensimmäisten 30 minuutin ajan ja sitten 600 mg / h seuraavien 90 minuutin ajan.Jos nopeampi infuusio on hyvin siedetty, samaa infuusio -ohjelmaa voidaan käyttää seuraavien infuusioiden antamiseen.
Nopeampaa infuusiota ei saa antaa potilaille, joilla on kliinisesti merkittäviä sydän- ja verisuonitauteja, mukaan lukien rytmihäiriöt, tai jotka ovat kokeneet vakavia reaktioita rituksimabi -infuusioon tai aikaisempaan biologiseen hoitoon.
04.3 Vasta -aiheet
Vasta-aiheet ei-Hodgkinin lymfoomassa ja kroonisessa lymfaattisessa leukemiassa
Yliherkkyys vaikuttavalle aineelle, hiiren proteiineille tai jollekin muulle kohdassa 6.1 luetellulle apuaineelle.
Aktiiviset, vaikeat infektiot (ks. Kohta 4.4).
Potilaat, joilla on vakavasti heikentynyt immuunijärjestelmä.
Vasta -aiheet nivelreumassa, granulomatoosissa, jossa on polyangiitti ja mikroskooppinen polyangiitti
Yliherkkyys vaikuttavalle aineelle, hiiren proteiineille tai jollekin muulle kohdassa 6.1 luetellulle apuaineelle.
Aktiiviset, vaikeat infektiot (ks. Kohta 4.4).
Potilaat, joilla on vakavasti heikentynyt immuunijärjestelmä.
Vaikea sydämen vajaatoiminta (New York Heart Association -luokka IV) tai vaikea, hallitsematon sydänsairaus (katso muut sydänsairaudet kohdasta 4.4).
04.4 Varoitukset ja käyttöön liittyvät varotoimet
Biologisten lääkkeiden jäljitettävyyden parantamiseksi valmisteen nimi MabThera on merkittävä selvästi potilastietoihin.
Progressiivinen multifokaalinen leukoenkefalopatia
Kaikille potilaille, jotka ovat saaneet MabTheraa nivelreuman, granulomatoosin, polyangiitin ja mikroskooppisen polyangiitin hoitoon, on annettava potilaan hälytyskortti jokaisen infuusion yhteydessä.
Hyvin harvinaisia kuolemaan johtaneita PML -tapauksia on raportoitu MabTheran käytön jälkeen. Potilaita on seurattava säännöllisin väliajoin uusien tai pahenevien neurologisten oireiden tai PML: ään viittaavien oireiden varalta. Jos epäillään PML: ää, jatkuva anto on keskeytettävä, kunnes Lääkärin on arvioitava potilas sen määrittämiseksi, viittaavatko oireet neurologiseen toimintahäiriöön, ja jos on, voiko nämä oireet mahdollisesti viitata PML: ään. Neurologista neuvontaa on haettava, jos se on kliinisesti osoitettu.
Jos olet epävarma, tulee harkita lisäarviointia, mukaan lukien testit, kuten MRI mieluiten kontrastilla, aivo -selkäydinneste (CSF) -testi JC -viruksen DNA: n arvioimiseksi ja toistuvat neurologiset arvioinnit.
Lääkärien tulee olla erityisen varovaisia oireista, jotka viittaavat PML: ään, joita potilas ei ehkä huomaa (esimerkiksi kognitiiviset, neurologiset tai psykiatriset oireet). Potilasta on myös neuvottava ilmoittamaan hoidosta kumppanilleen tai hoitajalleen, koska hän voi huomata oireita, joista potilas ei tiedä.
Jos potilaalle kehittyy PML, MabTheran anto on lopetettava pysyvästi.
Immuunijärjestelmän uudelleenrakentamisen jälkeen immuunipuutteisilla potilailla, joilla oli PML, havaittiin vakautumista tai paranemista. Ei tiedetä, johtaako PML: n varhainen havaitseminen ja MabThera -hoidon lopettaminen samanlaiseen vakautumiseen tai parantumiseen.
Non-Hodgkinin lymfooma ja krooninen lymfaattinen leukemia
Infuusioon liittyvät reaktiot
MabThera liittyy infuusioon liittyviin reaktioihin, jotka voivat mahdollisesti liittyä sytokiinien ja / tai muiden kemiallisten välittäjien vapautumiseen .. Sytokiinien vapautumisoireyhtymä voi olla kliinisesti erottamaton akuuteista yliherkkyysreaktioista.
Tämä reaktiosarja, joka sisältää sytokiinien vapautumisoireyhtymän, kasvaimen hajoamisoireyhtymän sekä anafylaktiset ja yliherkkyysreaktiot, kuvataan alla. Nämä reaktiot eivät liity erityisesti MabTheran antoreittiin, ja ne voidaan havaita molemmilla formulaatioilla.
Vakavia ja kuolemaan johtavia infuusioon liittyviä reaktioita on raportoitu laskimonsisäisen MabThera-valmisteen markkinoille tulon jälkeen, ja se ilmaantuu 30 minuutin-2 tunnin kuluessa ensimmäisen MabThera-infuusion aloittamisesta. Näille reaktioille oli ominaista keuhkotapahtumat ja joissakin tapauksia olivat nopea kasvaimen hajoaminen ja kasvaimen hajoamisoireyhtymän oireet sekä kuume, vilunväristykset, vilunväristykset, hypotensio, nokkosihottuma, angioedeema ja muut oireet (ks. kohta 4.8).
Vaikealle sytokiinien vapautumisoireyhtymälle on ominaista vaikea hengenahdistus, johon usein liittyy bronkospasmi ja hypoksia sekä kuume, vilunväristykset, vilunväristykset, nokkosihottuma ja angioedeema. Tämä oireyhtymä voi liittyä joihinkin tuumorilyysioireyhtymän piirteisiin, kuten hyperurikemiaan, hyperkalemiaan, hypokalsemiaan, hyperfosfatemiaan, akuuttiin munuaisten vajaatoimintaan, laktaattidehydrogenaasin (LDH) pitoisuuden suurenemiseen, ja se voi liittyä akuuttiin hengitysvajaukseen ja kuolemaan. Akuuttiin hengitysvajeeseen voi liittyä tapahtumia, kuten keuhkojen välitukos tai keuhkoödeema, joka näkyy rintakehän röntgenkuvauksessa.Oireyhtymä ilmenee usein 1-2 tunnin kuluessa ensimmäisen infuusion aloittamisesta. Potilailla, joilla on aiemmin ollut keuhkojen vajaatoimintaa tai keuhkosyövän tunkeutumista, saattaa olla suurempi riski saada huonot tulokset ja heitä tulee hoitaa varovaisemmin. Potilaiden, joille kehittyy vaikea sytokiinien vapautumisoireyhtymä, infuusio on lopetettava välittömästi (ks. Kohta 4.2) ja heille on annettava aggressiivista oireenmukaista hoitoa. Koska kliinisten oireiden alkuvaiheen paranemista voi seurata paheneminen, näitä potilaita on seurattava huolellisesti, kunnes kasvaimen hajoamisoireyhtymä ja keuhkojen tunkeutuminen on ratkaistu tai suljettu pois.
Potilaiden jatkohoito oireiden ja merkkien täydellisen häviämisen jälkeen on harvoin johtanut vaikean sytokiinien vapautumisoireyhtymän uusiutumiseen.
Potilaita, joilla on suuri kasvainkuormitus tai suuri määrä (≥ 25 x 109 / l) kiertäviä neoplastisia soluja, kuten CLL -potilaita, joilla saattaa olla lisääntynyt riski erityisen vaikeasta sytokiinien vapautumisoireyhtymästä, tulee hoitaa äärimmäisen varovasti. Näitä potilaita on seurattava erittäin tarkasti ensimmäisen infuusion aikana. Tällaisilla potilailla on harkittava hitaamman infuusionopeuden käyttöä ensimmäisessä infuusiossa tai jaettua annosta kahden päivän aikana ensimmäisen syklin aikana ja jokaisen seuraavan jakson aikana, jos lymfosyyttimäärä on edelleen> 25 x 109 / l.
Kaikenlaisia infuusioon liittyviä haittavaikutuksia (mukaan lukien sytokiinien vapautumisoireyhtymä, johon liittyy hypotensio ja bronkospasmi 10%: lla potilaista) on havaittu 77%: lla MabTheraa saaneista potilaista (ks. Kohta 4.8) .Nämä oireet ovat yleensä palautuvia. MabThera -infuusiosta ja antipyreettisistä lääkkeistä, antihistamiineista ja joskus hapesta, suonensisäisestä suolaliuoksesta tai keuhkoputkia laajentavista lääkkeistä ja tarvittaessa glukokortikoideista. Vaikeista reaktioista katso yllä kuvattu sytokiinien vapautumisoireyhtymä.
Anafylaktisia ja muita yliherkkyysreaktioita on raportoitu potilailla laskimoon annettujen proteiinien jälkeen. Toisin kuin sytokiinien vapautumisoireyhtymä, yliherkkyysreaktiot ilmenevät tyypillisesti minuuteissa infuusion aloittamisesta. Jos MabThera -hoidon aikana ilmenee allerginen reaktio, lääkkeitä yliherkkyysreaktioiden hoitoon, esim. epinefriinin (adrenaliinin), antihistamiinien ja glukokortikoidien on oltava saatavilla välittömästi. Yliherkkyyteen liittyviä reaktioita on raportoitu harvemmin kuin sytokiinien vapautumiseen liittyviä.
Joissakin tapauksissa raportoituja lisäreaktioita olivat sydäninfarkti, eteisvärinä, keuhkoödeema ja akuutti palautuva trombosytopenia. MabThera -hoidon aikana saattaa ilmetä hypotensiota, joten verenpainelääkkeiden käytön lopettamista on harkittava 12 tuntia ennen MabThera -infuusiota.
Sydänhäiriöt
MabTheraa saaneilla potilailla on esiintynyt angina pectorista, sydämen rytmihäiriöitä, kuten eteislepatusta ja -värinää, sydämen vajaatoimintaa ja / tai sydäninfarktia. Siksi potilaita, joilla on ollut sydänsairaus ja / tai sydäntoksinen kemoterapia, on seurattava huolellisesti.
Hematologinen myrkyllisyys
Vaikka MabThera ei yksinään ole myelosuppressiivinen, on oltava erityisen varovainen, kun harkitaan potilaiden hoitoa, joilla on autologisia luuytimen verihiutaleiden neutrofiilejä ja muita riskiryhmiä, joilla luultavasti on heikentynyt luuydintoiminto aiheuttamatta myelotoksisuutta.
Täydellinen verenkuva, mukaan lukien neutrofiilit ja verihiutaleiden määrä, on otettava säännöllisesti MabThera -hoidon aikana.
Infektiot
MabThera -hoidon aikana voi esiintyä vakavia infektioita, mukaan lukien kuolemantapaukset (ks. Kohta 4.8).
MabTheraa ei saa käyttää potilaille, joilla on vakavia aktiivisia infektioita (esim. Tuberkuloosi, sepsis ja opportunistiset infektiot, ks. Kohta 4.3).
Lääkärien tulee olla varovaisia, kun he harkitsevat MabTheran käyttöä potilailla, joilla on ollut toistuvia tai kroonisia infektioita tai joilla on perussairauksia, jotka voivat edelleen altistaa potilaita vakaville infektioille (ks. Kohta 4.8).
MabTheraa saaneilla potilailla on raportoitu tapauksia hepatiitti B: n uudelleenaktivoitumisesta, mukaan lukien raportit fulminantista hepatiitista, joka on johtanut kuolemaan. Useimmat näistä potilaista saivat myös sytotoksista kemoterapiaa. Rajalliset tiedot tutkimuksesta, joka koski potilaita, joilla oli uusiutunut / tulenkestävä KLL, viittaavat siihen, että MabThera -hoito voi myös pahentaa primaaristen hepatiitti B -infektioiden tulosta. Hepatiitti B -virus (HBV) -seulonta on suoritettava kaikille potilaille. Ennen MabThera -hoidon aloittamista ja Näihin testeihin voidaan sitten täydentää muita asianmukaisia markkereita paikallisten ohjeiden mukaisesti. Potilaita, joilla on aktiivinen hepatiitti B -infektio, ei tule hoitaa MabTheralla. Potilaat, joilla on positiivinen hepatiitti B -serologia (sekä HBsAg että HBcAb), on arvioitava Hepatologi B -lääkärin tehtävä ennen hoidon aloittamista, ja häntä on seurattava ja seurattava paikallisten kliinisten standardien mukaisesti hepatiitti B: n uudelleenaktivoitumisen estämiseksi.
Hyvin harvinaisia tapauksia progressiivisesta multifokaalisesta leukoenkefalopatiasta (PML) on raportoitu MabTheran markkinoille tulon jälkeen NHL: ssä ja CLL: ssä (ks. Kohta 4.8) Useimmat potilaat olivat saaneet MabTheraa yhdistelmänä solunsalpaajahoidon kanssa tai osana hematopoieettista kantasolusiirto-ohjelmaa.
Rokotus
Rokotusten turvallisuutta elävillä virusrokotteilla MabThera-hoidon jälkeen ei ole tutkittu NHL- ja CLL-potilailla, eikä rokotusta elävillä virusrokotteilla suositella. Ei-satunnaistetussa tutkimuksessa potilailla, joilla oli uusiutunut matala-asteinen NHL ja jotka saivat MabThera-monoterapiaa verrattuna hoitamattomiin terveisiin vapaaehtoisiin kontrolleihin, vaste tetanus-tehosteantigeenejä vastaan oli pienempi (16% vs. 81%) ja Keyhole Limpet Hemosyaniini (KLH) -neoantigeenit (4% vs. 76%, kun vasta-ainetiitterin nousu on yli 2-kertainen). . pre-terapeuttiset vasta-aineet antigeenipaneelia vastaan (Streptococcus pneumoniae, influenssa A, sikotauti, vihurirokko, vesirokko) säilyi vähintään 6 kuukautta MabThera -hoidon jälkeen.
Ihon reaktiot
Vakavia ihoreaktioita, kuten toksista epidermaalista nekrolyysiä (Lyellin oireyhtymä) ja Stevens-Johnsonin oireyhtymää, joista osa on johtanut kuolemaan, on raportoitu (ks. Kohta 4.8). Jos tällaisia tapahtumia ilmenee, jos suhdetta MabTheraan epäillään, hoito on lopetettava pysyvästi. Nivelreuma, granulomatoosi ja polyangiitti sekä mikroskooppinen polyangiitti.
Potilaat, joilla ei ollut metotreksaattia (MTX)
MabTheran käyttöä ei suositella potilaille, jotka eivät ole saaneet MTX-hoitoa, koska hyöty-riskisuhdetta ei ole vahvistettu.
Infuusioon liittyvät reaktiot
MabThera liittyy infuusioon liittyviin reaktioihin (IRR), jotka voivat liittyä sytokiinien ja / tai muiden kemiallisten välittäjien vapautumiseen. Esilääkitys kipulääkkeillä ja kuumetta alentavilla lääkkeillä ja antihistamiinilääkkeillä tulee aina antaa ennen jokaista MabThera-infuusiota. Jos sinulla on nivelreuma, esilääkitys glukokortikoideilla on aina annettava ennen jokaista MabThera -infuusiota infuusioreaktioiden esiintymistiheyden ja vaikeusasteen vähentämiseksi (ks. kohdat 4.2 ja 4.8).
Vakavia kuolemaan johtaneita IRR -tapauksia on raportoitu potilailla, joilla on nivelreuma markkinoille tulon jälkeen.
Nivelreuman hoidossa useimmat infuusioon liittyvät reaktiot olivat kliinisissä tutkimuksissa voimakkuudeltaan lieviä tai kohtalaisia. Yleisimmät oireet olivat allergiset reaktiot, kuten päänsärky, kutina, kurkun ärsytys, punoitus, ihottuma, nokkosihottuma, verenpaine ja kuume. Yleensä joidenkin infuusioreaktioiden saaneiden potilaiden osuus oli suurempi ensimmäisen infuusion jälkeen kuin toisen hoitojakson toisen infuusioreaktion jälkeen. Ilmoitetut reaktiot olivat yleensä palautuvia, kun infuusionopeutta hidastettiin tai MabThera lopetettiin ja antipyreettisiä lääkkeitä, antihistamiineja ja joskus happea, suolaliuosta tai keuhkoputkia laajentavia lääkkeitä ja glukokortikoideja otettiin tarvittaessa. Jos potilaalla on aiemmin ollut sydän- ja keuhko -haittavaikutuksia, lopeta MabThera -hoito väliaikaisesti tai pysyvästi. Useimmissa tapauksissa infuusio voidaan jatkaa vähentämällä nopeutta 50%: iin (esim. 100 mg / h: sta 50 mg / h: een), kun oireet ovat täysin hävinneet.
Lääkkeet yliherkkyysreaktioiden hoitoon, esim.epinefriinin (adrenaliinin), antihistamiinien ja glukokortikoidien on oltava saatavilla välittömästi käytettäväksi, jos MabThera -hoidon aikana ilmenee allergisia reaktioita.
MabTheran turvallisuudesta potilailla, joilla on kohtalainen sydämen vajaatoiminta (NYHA -luokka III) tai vaikea, hallitsematon sydänsairaus, ei ole tietoja. MabThera-hoitoa saaneilla potilailla on havaittu aiemmin esiintyneen sydäniskemian, kuten angina pectoriksen, muuttuvan oireelliseksi, samoin kuin eteisvärinä ja värinä.Siksi potilailla, joilla on ollut sydänsairaus ja joilla on aiemmat reaktiot kardiopulmonaaliset haittatapahtumat, infuusioreaktioista johtuvien sydän- ja verisuonitaudin komplikaatioiden riski on otettava huomioon ennen MabThera-hoitoa ja potilaita on seurattava tarkasti annostelun aikana. MabThera -infuusio.
IRR -arvot potilailla, joilla oli polyangiitti ja mikroskooppinen polyangiitti, olivat samankaltaisia kuin nivelreumapotilailla tehdyissä kliinisissä tutkimuksissa (ks. Kohta 4.8).
Sydänhäiriöt
MabTheraa saaneilla potilailla on esiintynyt angina pectorista, sydämen rytmihäiriöitä, kuten eteislepatusta ja -värinää, sydämen vajaatoimintaa ja / tai sydäninfarktia. Siksi potilaita, joilla on ollut sydänsairaus, on seurattava tarkasti (ks. Yllä oleva "Infuusioon liittyvät reaktiot").
Infektiot
MabTheran vaikutusmekanismin ja sen tiedon perusteella, että B -soluilla on tärkeä rooli normaalin immuunivasteen ylläpitämisessä, potilailla on lisääntynyt infektioriski MabThera -hoidon jälkeen (ks. Kohta 5.1). Vakavia infektioita, mukaan lukien kuolemaan johtavia tapahtumia MabThera -hoito (ks. Kohta 4.8) MabTheraa ei saa antaa potilaille, joilla on vaikea aktiivinen infektio (esim. Tuberkuloosi, sepsis ja opportunistiset infektiot, ks. Kohta 4.3) tai potilaille, joilla on vaikea immuunivaste.
(esim. missä CD4- tai CD8 -arvot ovat erittäin alhaiset). Lääkärien on noudatettava varovaisuutta harkittaessa MabTheran käyttöä potilailla, joilla on aiemmin ollut toistuvia tai kroonisia infektioita tai joilla on perussairauksia, jotka voivat edelleen altistaa potilaita vakaville infektioille, kuten hypogammaglobulinemia (ks. Kohta 4.8). Immunoglobuliinit määritetään ennen MabThera -hoidon aloittamista.
Potilaat, joilla on infektion merkkejä ja oireita MabThera -hoidon jälkeen, on arvioitava välittömästi ja hoidettava asianmukaisesti. Ennen seuraavan MabThera-hoidon aloittamista potilaat on arvioitava uudelleen mahdollisen infektioriskin varalta.
Hyvin harvoin kuolemaan johtavaa etenevää multifokaalista leukoenkefalopatiaa (PML) on raportoitu MabTheran käytön jälkeen nivelreuman ja autoimmuunisairauksien, mukaan lukien systeeminen lupus erythematosus (SLE) ja vaskuliitti, hoitoon.
Hepatiitti B -infektio
Hepatiitti B: n uudelleenaktivoitumistapauksia, mukaan lukien kuolemaan johtaneet, on raportoitu potilailla, joilla on nivelreuma, granulomatoosi, polyangiitti ja mikroskooppinen polyangiitti, jotka ovat saaneet MabTheraa.
Hepatiitti B -viruksen (HBV) seulonta on suoritettava kaikille potilaille ennen MabThera -hoidon aloittamista, ja siihen on sisällyttävä vähintään HBsAg- ja HBcAb -testaus. Näitä testejä voidaan tällöin täydentää muilla sopivilla markkereilla paikallisten ohjeiden mukaisesti. B -infektiota ei tule hoitaa MabTheralla. Potilaat, joilla on positiivinen hepatiitti B -serologia (sekä HBsAg että HBcAb), on arvioitava hepatologin lääkärin toimesta ja heitä on seurattava ja seurattava paikallisten kliinisten standardien mukaisesti hepatiitti B: n uudelleenaktivoitumisen estämiseksi.
Myöhäinen neutropenia
Mittaa neutrofiilit ennen jokaista MabThera -hoitojaksoa ja säännöllisin väliajoin, enintään 6 kuukauden kuluttua hoidon lopettamisesta ja jos sinulla on infektion merkkejä tai oireita (ks. Kohta 4.8).
Ihon reaktiot
Vakavia ihoreaktioita, kuten toksista epidermaalista nekrolyysiä (Lyellin oireyhtymä) ja Stevens-Johnsonin oireyhtymää, joista osa on johtanut kuolemaan, on raportoitu (ks. Kohta 4.8). Jos tällaisia tapahtumia ilmenee, jos suhdetta MabTheraan epäillään, hoito on lopetettava pysyvästi.
Rokotus
Lääkärien tulee tarkistaa potilaan rokotustila ja noudattaa voimassa olevia rokotusohjeita ennen MabThera -hoitoa Rokotus on saatettava päätökseen vähintään 4 viikkoa ennen MabThera -valmisteen ensimmäistä antamista.
Rokotuksen turvallisuutta elävillä virusrokotteilla MabThera -hoidon jälkeen ei ole tutkittu, joten rokotusta elävillä virusrokotteilla ei suositella MabThera -hoidon aikana tai perifeeristen B -solujen ehtymisen aikana.
MabTheralla hoidetut potilaat voivat saada ei-eläviä virusrokotuksia. Kuitenkin vasteita ei-eläviin rokotteisiin voidaan alentaa. Satunnaistetussa tutkimuksessa nivelreumapotilailla, jotka saivat MabTheraa ja metotreksaattia, vaste oli samankaltainen kuin potilailla, jotka saivat vain metotreksaattia jäykkäkouristuksen tehosteantigeeneille (39% vs. 42%), alennettiin polysakkaridirokotetta. Pneumokokki (43% vs. 82%: sta vähintään kahteen pneumokokkivasta-aineiden vasta-aineen serotyyppiin) ja KLH-neoantigeeneihin (47% vs. 93%), kun sitä annetaan 6 kuukautta MabTheran jälkeen. Jos ei-eläviä virusrokotuksia tarvitaan MabThera-hoidon aikana, ne on suoritettava vähintään 4 viikkoa ennen seuraavan MabThera-hoitojakson alkua.
"Maailmanlaajuisessa kokemuksessa MabTheran toistuvista hoidoista vuoden aikana" nivelreuman ympäristössä potilaiden prosenttiosuus, joilla on positiivinen vasta -ainetiitteri S. pneumoniae, influenssa, sikotauti, vihurirokko, vesirokko ja jäykkäkouristustoksiini olivat yleensä samanlaisia kuin lähtötasot.
Muiden DMARD -lääkkeiden samanaikainen / peräkkäinen käyttö nivelreuman hoidossa
MabTheran ja muiden kuin nivelreuman käyttöaiheessa ja annostuksessa mainittujen reumalääkkeiden samanaikaista käyttöä ei suositella.
Muiden DMARD -lääkkeiden (mukaan lukien TNF: n estäjät ja muut biologiset aineet) MabThera -valmisteen käytön jälkeisen käytön turvallisuuden arvioimiseksi kliinisistä tutkimuksista on vain vähän tietoja (ks. Kohta 4.5). käytetään potilailla, jotka ovat aiemmin saaneet MabTheraa, mutta potilaita on kuitenkin seurattava tarkasti infektio -oireiden varalta, jos biologisia aineita ja / tai DMARD -lääkkeitä käytetään MabThera -hoidon jälkeen.
Kasvaimet
Immunomodulaattorit voivat lisätä syöpäriskiä. Koska MabTheran käytöstä nivelreumapotilailla on vain vähän kokemusta (ks. Kohta 4.8), nykyiset tiedot eivät näytä viittaavan suurentuneeseen pahanlaatuisuuden riskiin, mutta kiinteiden kasvainten kehittymisen mahdollista riskiä ei tällä hetkellä voida sulkea pois.
04.5 Yhteisvaikutukset muiden lääkevalmisteiden kanssa sekä muut yhteisvaikutukset
Tällä hetkellä on vain vähän tietoa mahdollisista yhteisvaikutuksista MabTheran kanssa.
CLL-potilailla samanaikainen anto MabTheran kanssa ei näytä vaikuttavan fludarabiinin tai syklofosfamidin farmakokinetiikkaan. Lisäksi fludarabiinilla ja syklofosfamidilla ei ole ilmeistä vaikutusta MabTheran farmakokinetiikkaan.
Samanaikainen käyttö metotreksaatin kanssa ei vaikuttanut MabTheran farmakokinetiikkaan nivelreumapotilailla.
Potilailla, joille on kehittynyt hiiren vastaisia tai kimeerisiä vasta-aineita (HAMA / HACA), voi esiintyä allergisia tai yliherkkyysreaktioita hoidettaessa muilla diagnostisilla tai terapeuttisilla monoklonaalisilla vasta-aineilla.
Nivelreumapotilailla 283 potilasta sai myöhemmin biologista DMARD -hoitoa MabTheran jälkeen. Näillä potilailla kliinisesti merkittävien infektioiden määrä MabThera-hoidon aikana oli 6,01 / 100 potilasvuotta verrattuna 4,97 tapaukseen 100 potilasvuotta kohti biologisen DMARD-hoidon jälkeen.
04.6 Raskaus ja imetys
Ehkäisy miehillä ja naisilla
Koska rituksimabilla on pitkä retentioaika potilailla, joilla on B-soluvaje, hedelmällisessä iässä olevien naisten tulee käyttää tehokkaita ehkäisymenetelmiä hoidon aikana ja enintään 12 kuukauden ajan MabThera-hoidon päättymisen jälkeen.
Raskaus
IgG -immunoglobuliinien tiedetään läpäisevän istukan.
Imeväisten B -solutasoja äidin MabThera -hoidon jälkeen ei ole arvioitu kliinisissä tutkimuksissa. Raskaana oleville naisille tehdyistä tutkimuksista ei ole riittävästi ja hyvin kontrolloitua tietoa, mutta ohimenevää B-solujen ehtymistä ja lymfosytopeniaa on raportoitu imeväisillä, jotka ovat syntyneet MabTheralle raskauden aikana altistuneille äideille. Samanlaisia vaikutuksia havaittiin eläinkokeissa (ks. Kohta 5.3). Tästä syystä MabTheraa ei saa antaa raskaana oleville naisille, ellei mahdollinen hyöty ole suurempi kuin mahdollinen riski.
Imetys
Ei tiedetä, erittyykö rituksimabi äidinmaitoon. Koska äidin IgG erittyy kuitenkin äidinmaitoon ja rituksimabia havaittiin imettävillä apinoilla, naisten ei pitäisi imettää MabThera -hoidon aikana ja 12 kuukauden ajan MabThera -hoidon jälkeen.
Hedelmällisyys
Eläinkokeet eivät osoittaneet, että rituksimabilla olisi haitallisia vaikutuksia lisääntymiselimiin.
04.7 Vaikutus ajokykyyn ja koneiden käyttökykyyn
MabTheran vaikutuksista ajokykyyn ja koneiden käyttökykyyn ei ole tehty tutkimuksia, vaikka tähän mennessä raportoidut farmakologiset vaikutukset ja haittavaikutukset viittaavat siihen, että MabTheralla ei ole haitallista vaikutusta ajokykyyn tai koneiden käyttökykyyn.
04.8 Haittavaikutukset
Kokemusta ei-Hodgkinin lymfoomasta ja kroonisesta lymfaattisesta leukemiasta
Yhteenveto turvallisuusprofiilista
MabTheran yleinen turvallisuusprofiili non-Hodgkinin lymfooman ja kroonisen lymfaattisen leukemian hoidossa perustuu kliinisissä tutkimuksissa ja markkinoille tulon jälkeisessä seurannassa olevien potilaiden tietoihin. Näitä potilaita hoidettiin MabTheralla monoterapiana (induktiohoitona tai induktion jälkeisenä ylläpitohoitona) tai yhdistelmänä kemoterapian kanssa.
Yleisimmin havaitut haittavaikutukset MabTheraa saaneilla potilailla olivat IRR -reaktiot, joita esiintyi suurimmalla osalla potilaista ensimmäisen infuusion aikana. Infuusioon liittyvien oireiden ilmaantuvuus vähenee merkittävästi seuraavien infuusioiden yhteydessä ja on alle 1% kahdeksan MabThera-annoksen jälkeen.
Tartuntatapahtumia (pääasiassa bakteereja ja viruksia) esiintyi noin 30–55%: lla kliinisissä tutkimuksissa hoidetuista NHL-potilaista ja noin 30–50%: lla kliinisissä tutkimuksissa hoidetuista CLL-potilaista. Yleisimmin raportoidut tai havaitut vakavat haittavaikutukset olivat:
• IRR (mukaan lukien sytokiinien vapautumisoireyhtymä ja tuumorilyysioireyhtymä), ks. Kohta 4.4.
• Infektiot, ks. Kohta 4.4.
• Sydän- ja verisuonitapahtumat, ks. Kohta 4.4.
Muita raportoituja vakavia haittavaikutuksia ovat hepatiitti B: n uudelleenaktivointi ja PML (ks. Kohta 4.4).
Luettelo haittavaikutuksista taulukon muodossa
Taulukossa 1. on esitetty yhteenveto haittavaikutusten esiintymistiheydestä, joka on raportoitu pelkästään MabTheran tai yhdistelmänä solunsalpaajahoidon kanssa. Kussakin yleisyysluokassa haittavaikutukset on lueteltu vakavuuden mukaan alenevassa järjestyksessä. Esiintymistiheys määritellään hyvin yleiseksi (≥ 1/10), yleiseksi ( ≥ 1/100 -
Haittavaikutukset, jotka on tunnistettu vain markkinoille tulon jälkeen ja joiden esiintymistiheyttä ei voida arvioida, on lueteltu kohdassa "tuntematon".
Taulukko 1 Haittavaikutukset, jotka on raportoitu kliinisissä tutkimuksissa tai markkinoille tulon jälkeisessä seurannassa NHL- ja CLL-potilailla, jotka ovat saaneet MabTheraa monoterapiana / ylläpitohoitona tai yhdistelmänä solunsalpaajahoidon kanssa
Seuraavat termit on raportoitu haittavaikutuksina kliinisissä tutkimuksissa; kuitenkin hematologista toksisuutta, neutropeenista infektiota, virtsatieinfektiota, aistihäiriöitä, kuumeita raportoitiin MabThera -haarojen esiintymistiheyden ollessa sama tai pienempi kuin kontrolliryhmissä.
Infuusioon liittyvän reaktion tyypillisiä merkkejä ja oireita on raportoitu yli 50%: lla potilaista kliinisissä tutkimuksissa, ja niitä on havaittu pääasiassa ensimmäisen infuusion aikana, yleensä kahden ensimmäisen tunnin aikana. Muita oireita ovat punoitus, angioedeema, bronkospasmi, oksentelu, pahoinvointi, nokkosihottuma / ihottuma, väsymys, päänsärky, kurkun ärsytys, nuha, kutina, kipu, takykardia, hypertensio, hypotensio, hengenahdistus, dyspepsia, astenia ja kasvaimen hajoamisoireyhtymän oireet. -reaktioita (kuten bronkospasmi, hypotensio) esiintyi jopa 12%: ssa tapauksista. Joissakin tapauksissa raportoituja lisäreaktioita olivat sydäninfarkti, eteisvärinä, keuhkoödeema ja akuutti palautuva trombosytopenia. Olemassa olevien sydänsairauksien paheneminen, kuten angina pectoris tai kongestiivinen sydämen vajaatoiminta tai vaikea sydänsairaus (sydämen vajaatoiminta, sydäninfarkti, eteisvärinä), keuhkoödeema, monielinvika, kasvaimen hajoamisoireyhtymä, sytokiinien vapautumisoireyhtymä, munuaisten vajaatoiminta ja hengityselimet vikaa on raportoitu harvemmin tai tuntemattomasti. Infuusioon liittyvien oireiden ilmaantuvuus väheni huomattavasti seuraavien infuusioiden yhteydessä ja on
Kuvaus haittavaikutusten valikoimasta
Infektiot
MabThera aiheuttaa B-solujen ehtymistä noin 70-80%: lla potilaista, mutta tämä tapahtuma on liitetty seerumin immunoglobuliinin vähenemiseen vain pienellä osalla potilaista.
Paikallisia Candida -infektioita, kuten herpes zoster, on raportoitu useammin MabThera -haarassa satunnaistetuissa tutkimuksissa. Vakavia infektioita raportoitiin noin 4%: lla MabThera -monoterapiaa saaneista potilaista. Kaikkien MabThera-ylläpitohoitojen aikana havaittiin korkeampia infektioita, mukaan lukien asteen 3 tai 4 infektiot verrattuna havaintoon. Kahden vuoden hoitojakson aikana ei raportoitu kumulatiivista toksisuutta infektioiden suhteen. muita vakavia virusinfektioita, joko uusia, aktivoituneita tai pahentuneita, on raportoitu MabThera -hoidon aikana, joista osa oli kuolemaan johtaneita. ovat herpeettisten virusten (Cytomegalovirus, Varicella Zoster virus ja Herpes Simplex), JC -viruksen (progressiivinen multifokaalinen leukoenkefalopatia (PML)) ja virushepatiitti C: n aiheuttamia infektioita. Myös kuolemaan johtaneita PML -tapauksia on raportoitu kliinisissä tutkimuksissa ja niitä on esiintynyt ti sairauden etenemisen ja uudelleenhoidon jälkeen. Hepatiitti B: n uudelleenaktivaatiotapauksia on raportoitu, joista suurin osa esiintyi potilailla, jotka saivat MabTheraa yhdessä sytotoksisen solunsalpaajahoidon kanssa. Potilailla, joilla oli uusiutunut / tulenkestävä KLL, asteen 3/4 hepatiitti B -infektion (uudelleenaktivointi ja primaarinen infektio) ilmaantuvuus oli 2% R-FC: ssä ja 0% FC: ssä. Kaposin sarkooman etenemistä havaittiin MabTheraa saaneilla potilailla. aiemmin olemassa oleva Kaposin sarkooma Näitä tapauksia esiintyi hyväksymättömissä käyttöaiheissa ja suurin osa potilaista oli HIV-positiivisia.
Hematologiset haittavaikutukset
Kliinisissä tutkimuksissa, joissa MabTheraa käytettiin monoterapiana 4 viikon ajan, hematologisia poikkeavuuksia esiintyi pienellä osalla potilaista ja ne olivat yleensä lieviä ja palautuvia. Vaikeaa (asteen 3/4) neutropeniaa raportoitiin 4,2%: lla potilaista, anemiaa 1,1%: lla ja trombosytopeniaa 1,7%: lla potilaista. Kahden vuoden MabThera-ylläpitohoidon aikana leukopenia (5% vs 2%, luokka 3/4) ja neutropenia (10%) vs 4%, luokka 3/4) raportoitiin useammin kuin havainto. Trombosytopenian ilmaantuvuus oli alhainen (vs. CHOP 79%, R-FC 23% vsHR 12%), neutropenia (R-CVP 24% vs CVP 14%; R-CHOP 97% vs CHOP 88%, R-FC 30% vs HR 19% aiemmin hoitamattomassa CLL: ssä), pancytopenia (R-FC 3% vs CF 1% aiemmin hoitamattomassa CLL: ssä), raportoitiin yleensä useammin kuin pelkällä solunsalpaajahoidolla. Kuitenkin korkeampi neutropenian ilmaantuvuus MabTheraa ja solunsalpaajahoitoa saaneilla potilailla ei liittynyt suurempiin infektioiden ja tartuntojen ilmaantuvuuteen verrattuna pelkästään solunsalpaajahoitoa saaneisiin potilaisiin. Aiemmin hoitamattomat ja uusiutuneet / tulenkestävät CLL -tutkimukset osoittivat, että 25% R-FC: n kanssa neutropenia oli pitkittynyt (määritelty neutrofiilien granulosyyttimääräksi alle 1x109 / l päivien 24 ja 42 välillä viimeisen annoksen jälkeen) tai ilmeni myöhään (määritelty neutrofiilien granulosyyttimääräksi alle 1x109 / l päivän 42 jälkeen) viimeisen annoksen jälkeen potilailla, joilla ei ollut aiemmin pitkittynyttä neutropeniaa tai jotka toipuivat ennen päivää 42) MabThera- ja CF -hoidon jälkeen.
Anemian ilmaantuvuudessa ei ole raportoitu eroja Muutamia myöhäisen neutropenian tapauksia on raportoitu yli neljä viikkoa viimeisen MabThera -infuusion jälkeen. Ensimmäisen linjan CLL-tutkimuksessa Binet-vaiheen C potilailla esiintyi enemmän haittavaikutuksia R-FC-ryhmässä kuin FC-ryhmässä (R-FC 83% vs HR 71%). Uusiutuneessa / tulenkestävässä CLL -tutkimuksessa asteen 3/4 trombosytopeniaa raportoitiin 11%: lla RFC -ryhmän potilaista ja 9%: lla CF -ryhmän potilaista.
MabThera -tutkimuksissa Waldestromin makroglobulinemiaa sairastavilla potilailla on havaittu ohimenevää seerumin IgM -tason nousua hoidon aloittamisen jälkeen, mikä saattaa liittyä hyperviskositeettiin ja siihen liittyviin oireisiin. kuukaudet.
Kardiovaskulaariset haittavaikutukset
Pelkällä MabTheralla tehdyissä kliinisissä tutkimuksissa sydän- ja verisuonireaktioita raportoitiin 18,8%: lla potilaista, joilla oli hypotensio ja hypertensio yleisimmin raportoituna tapahtumana. Infuusion aikana on raportoitu 3. tai 4. asteen rytmihäiriöitä (mukaan lukien kammio- ja supraventrikulaarinen takykardia) ja angina pectorista. Ylläpitohoidon aikana asteen 3/4 sydänsairauksien ilmaantuvuus oli vertailukelpoista hoidetuilla potilailla. MabThera ja havainto. raportoitu vakavina haittatapahtumina (mukaan lukien eteisvärinä, sydäninfarkti, vasemman kammion vajaatoiminta, sydäniskemia) 3%: lla MabTheraa saaneista potilaista verrattuna asteen 3 ja 4 sydämen rytmihäiriöihin, erityisesti supraventrikulaarisiin rytmihäiriöihin, kuten takykardia ja eteisvärinä. korkeampi RCHOP -ryhmässä (14 potilasta, 6,9%) verrattuna CHOP -ryhmään (3 potilasta, 1,5%). Kaikki nämä rytmihäiriöt ilmenivät MabThera-infuusion yhteydessä tai liittyivät altistaviin tiloihin, kuten kuumeeseen, infektioon, akuuttiin sydäninfarktiin tai olemassa olevaan hengityselinten ja sydän- ja verisuonitauteihin. R-CHOP- ja CHOP-ryhmän välillä ei havaittu eroa muiden asteen 3 ja 4 sydäntapahtumien, mukaan lukien sydämen vajaatoiminta, sydänsairaus ja sepelvaltimotaudin ilmenemismuodot, esiintyvyys. KLL: ssä asteen 3 tai 4 sydänsairauksien yleinen ilmaantuvuus oli alhainen sekä ensimmäisen linjan tutkimuksessa (4% R-FC, 3% FC) että uusiutumis- / tulenkestävässä tutkimuksessa (4% R-FC, 4% FC) .
Hengityselimet
Interstitiaalisen keuhkosairauden tapauksia, joista osa on johtanut kuolemaan, on raportoitu.
Neurologiset patologiat
Hoitojakson aikana (induktiohoidon vaihe, joka koostuu R-CHOP: sta enintään kahdeksan syklin ajan) neljällä potilaalla (2%), jotka saivat R-CHOP-hoitoa ja joilla kaikilla oli sydän- ja verisuonitautien riskitekijöitä, ilmeni aivoverenkierron tromboembolisia onnettomuuksia ensimmäisen hoitojakson aikana. Hoitoryhmien välillä ei ollut eroa muiden tromboembolisten tapahtumien esiintyvyydessä. Sitä vastoin kolmella potilaalla (1,5%) oli aivoverisuonitapahtumia CHOP -ryhmässä, jotka kaikki ilmenivät seuranta -aikana. CLL, asteen 3 tai 4 hermostohäiriöiden yleinen ilmaantuvuus oli alhainen sekä ensimmäisen linjan tutkimuksessa (4% R-FC, 4% FC) että uusiutumis- / tulenkestävässä tutkimuksessa (3% R-FC, 3% FC) .
Positiivisen palautuvan enkefalopatian oireyhtymän (PRES) / posteriorisen palautuvan leukoenkefalopatian oireyhtymän (RPLS) tapauksia on raportoitu. Merkkejä ja oireita olivat näköhäiriöt, päänsärky, kohtaukset ja muutokset henkisessä tilassa, johon liittyi hypertensio tai ilman sitä. PRES / RPLS -diagnoosi vaatii vahvistuksen kuvantaminen aivojen. Raportoiduissa tapauksissa on tunnistettu PRES / RPLS -riskitekijöitä, mukaan lukien potilaan samanaikainen sairaus, kohonnut verenpaine, immunosuppressiivinen hoito ja / tai kemoterapia.
Ruoansulatuselimistö
Ruoansulatuskanavan perforaatiota on havaittu joissakin tapauksissa kuolemaan potilailla, jotka saavat MabTheraa non-Hodgkin-lymfooman hoitoon. Useimmissa tapauksissa MabTheraa annettiin kemoterapian kanssa.
IgG -tasot
Kliinisessä tutkimuksessa, jossa arvioitiin MabTheraa ylläpitohoidossa uusiutuneen / tulenkestävän follikulaarisen lymfooman hoidossa, IgG -tasojen mediaani oli alle normaalin alarajan (LLN) (
Pieniä hypogammaglobulinemiaan liittyviä spontaaneja ja kirjallisia tapauksia, joissain tapauksissa vakavia ja jotka vaativat pitkäaikaista immunoglobuliinikorvaushoitoa, on havaittu MabTheraa saaneilla lapsipotilailla. Pitkäaikaisen B-solujen ehtymisen seurauksia lapsipotilailla ei tunneta.
Iho ja ihonalainen kudos
Hyvin harvoin on raportoitu toksisen epidermaalisen nekrolyysin (Lyellin oireyhtymä) ja Stevens-Johnsonin oireyhtymän tapauksia, joista osa on johtanut kuolemaan.
Potilaiden alaryhmät - MabThera -monoterapia
Iäkkäät potilaat (≥ 65 -vuotiaat):
Kaikkien asteen ja asteen 3/4 haittavaikutusten ilmaantuvuus oli samanlainen iäkkäillä ja nuoremmilla potilailla (
Massiivinen sairaus
"Asteen 3/4 haittavaikutusten ilmaantuvuus oli suurempi potilailla, joilla oli massiivinen sairaus, kuin potilailla, joilla ei ollut tilaa vievää tautia (25,6% vs 15,4%). Kaikkien vaikeusasteisten haittavaikutusten ilmaantuvuus oli samanlainen näissä kahdessa ryhmässä.
Uudelleenhoito
Niiden potilaiden osuus, jotka ilmoittivat haittavaikutuksista uudelleenhoidon aikana MabThera -hoidon aikana, oli samanlainen kuin niiden potilaiden osuus, jotka ilmoittivat haittavaikutuksista alkuvaiheen aikana (kaikki asteen ja asteen 3/4 haittavaikutukset).
Potilaiden alaryhmät - yhdistelmähoito MabTheran kanssa
Iäkkäät potilaat (≥ 65 vuotta)
Asteen 3/4 haittavaikutusten ilmaantuvuus veressä ja imukudoksessa oli suurempi iäkkäillä potilailla kuin nuoremmilla potilailla (
Kokemusta nivelreumasta
Yhteenveto turvallisuusprofiilista
MabTheran yleinen turvallisuusprofiili nivelreumassa perustuu kliinisissä tutkimuksissa hoidetuista potilaista ja markkinoille tulon jälkeisestä seurannasta saatuihin tietoihin.
MabTheran turvallisuusprofiili potilailla, joilla on kohtalainen tai vaikea nivelreuma, on yhteenveto alla olevissa kohdissa. Kliinisissä tutkimuksissa yli 3100 potilasta sai vähintään yhden hoitojakson ja niitä seurattiin 6 kuukauden ja yli 5 vuoden ajan; noin 2400 potilasta sai kaksi tai useampia hoitojaksoja, ja yli 1000 potilasta sai 5 tai useampia hoitojaksoja. Turvallisuustiedot, jotka on kerätty markkinoille tulon jälkeen, heijastavat odotettua haittavaikutusprofiilia, joka on jo havaittu MabTheran kliinisissä tutkimuksissa (ks. Kohta 4.4).
Potilaat saivat 2 1000 mg MabThera-annosta kahden viikon välein yhdessä metotreksaatin kanssa (10-25 mg / viikko). MabThera -infuusioita annettiin 100 mg: n metyyliprednisoloni -laskimonsisäisen infuusion jälkeen; potilaat saivat myös suun kautta annettavaa prednisonihoitoa 15 päivän ajan.
Luettelo haittavaikutuksista taulukon muodossa
Haittavaikutukset on lueteltu taulukossa 2. Esiintymistiheys määritellään hyvin yleiseksi (≥ 1/10), yleiseksi (≥ 1/100 -
Yleisimmät haittavaikutukset, joiden uskotaan johtuvan MabTheran ottamisesta, olivat IRR -reaktioita. Vakavat infuusioreaktiot olivat harvinaisia (0,5% potilaista) ja esiintyivät pääasiassa ensimmäisen hoitojakson aikana. Nivelreuman kliinisissä MabTheralla tehdyissä tutkimuksissa havaittujen haittavaikutusten lisäksi markkinoille tulon jälkeen on raportoitu progressiivista multifokaalista leukoenkefalopatiaa (PML) ja seerumitaudin kaltaista reaktiota.
Taulukko 2 Yhteenveto kliinisissä tutkimuksissa tai markkinoille tulon jälkeisessä seurannassa raportoiduista haittavaikutuksista, joita ilmeni nivelreumapotilailla, jotka saivat MabTheraa.
Toistuvat syklit
Toistuviin hoitojaksoihin liittyy samanlainen haittavaikutusprofiili kuin ensimmäisen altistuksen jälkeen. Kaikkien haittavaikutusten määrä ensimmäisen MabThera -altistuksen jälkeen oli korkein ensimmäisten 6 kuukauden aikana ja laski sen jälkeen. Tämä koski pääasiassa IRR -reaktioita (useimmiten ensimmäisen hoidon aikana), nivelreuman pahenemista ja infektioita; kaikki nämä olivat useammin ensimmäisten 6 hoitokuukauden aikana.
Infuusioon liittyvät reaktiot
Kliinisissä tutkimuksissa yleisimmät haittavaikutukset MabThera -hoidon jälkeen olivat IRR -reaktiot (ks. Taulukko 2). MabThera -hoitoa saaneista 3189 potilaasta 1135: llä (36%) oli vähintään yksi infuusioreaktio, ja 733/3189 (23%) potilaista koki IRR: n ensimmäisen MabThera -hoidon ensimmäisen infuusion jälkeen. Infuusioreaktioiden ilmaantuvuus vähenee seuraavien infuusioiden jälkeen .. Kliinisissä tutkimuksissa alle 1% (17/3189) potilaista koki vakavan infuusion. Kliinisissä tutkimuksissa ei ollut yleisiä myrkyllisyyskriteerejä (CTC), asteen 4 IRR -arvoja eikä IRR -aiheuttamia kuolemia. CTC -asteen 3 tapahtumien ja hoidon lopettamiseen johtaneiden infuusioreaktioiden osuus väheni hoitojen aikana ja oli harvinaista syklistä 3 lähtien. Laskimonsisäinen glukokortikoidi-esilääkitys vähensi merkittävästi infuusioreaktioiden ilmaantuvuutta ja vakavuutta (ks. Kohdat 4.2 ja 4.4) Vakavia kuolemaan johtaneita infuusioreaktioita on raportoitu markkinoille tulon jälkeen.
Tutkimuksessa, jonka tarkoituksena oli arvioida "nopeamman MabThera -infuusion turvallisuutta nivelreumaa sairastavilla potilailla, potilailla, joilla oli kohtalainen tai vaikea aktiivinen nivelreuma ja joilla ei ilmennyt vakavaa IRR: ää ensimmäisen tutkitun infuusion aikana tai 24 tunnin kuluessa sen jälkeen, annettiin saat 2 tunnin MabThera-infuusion laskimoon. Potilaita, joilla on ollut vakava infuusioreaktio nivelreuman biologiseen hoitoon, ei otettu tutkimukseen. Infuusioreaktioiden ilmaantuvuus, tyypit ja vakavuus olivat yhdenmukaisia historiallisten tietojen kanssa, eikä vakavia IRR -arvoja havaittu.
Kuvaus haittavaikutusten valikoimasta
Infektiot
Infektioiden yleinen ilmaantuvuus oli MabThera-ryhmässä noin 94 tapausta 100 potilasvuotta kohden. se oli noin 4 sadasta potilasvuodesta. Vakavien infektioiden ilmaantuvuus ei osoittanut merkittävää lisääntymistä toistuvien MabThera -hoitojaksojen jälkeen.Kliinisissä tutkimuksissa on raportoitu alahengitystieinfektioita (mukaan lukien keuhkokuume), ja esiintyvyys on samanlainen MabThera -ryhmissä kuin MabThera -ryhmissä. on raportoitu MabTheran käytön jälkeen autoimmuunisairauksien hoitoon. Näitä ovat nivelreuma ja käyttöaiheista poikkeavat autoimmuunisairaudet, kuten systeeminen lupus erythematosus (SLE) ja vaskuliitti. Hepatiitti B: n uusiutumista on raportoitu potilailla, joilla on non-Hodgkinin lymfooma ja jotka ovat saaneet MabTheraa yhdessä sytotoksisen solunsalpaajahoidon kanssa (ks. Non-Hodgkinin lymfooma). .) Hepatiitti B -infektion uudelleen aktivoitumista on myös raportoitu hyvin harvoin RA -potilailla, jotka ovat saaneet MabTheraa (ks. Kohta 4.4).
Kardiovaskulaariset haittavaikutukset
Vakavia sydänreaktioita havaittiin "esiintymistiheydellä 1,3 / 100 potilasvuotta MabThera-hoitoa saaneilla ja 1,3 / 100 potilasvuotta plaseboa saaneilla potilailla. Sydämen reaktioita (kaikki tai vaikeat) sairastavien potilaiden osuus ei lisääntynyt eri syklit.
Neurologiset tapahtumat
Positiivisen palautuvan enkefalopatian oireyhtymän (PRES) / posteriorisen palautuvan leukoenkefalopatian oireyhtymän (RPLS) tapauksia on raportoitu. Merkkejä ja oireita olivat näköhäiriöt, päänsärky, kouristukset ja muuttunut mielenterveys, johon liittyi hypertensio tai ilman sitä. PRES / RPLS -diagnoosi vaatii vahvistuksen aivokuvantamisen avulla. Kuvatuissa tapauksissa oli tunnettuja PRES / RPLS -riskitekijöitä, mukaan lukien potilaiden perussairaus, kohonnut verenpaine, immunosuppressiivinen hoito ja / tai kemoterapia.
Neutropenia
Neutropeniatapauksia on havaittu MabThera -hoidon jälkeen, joista suurin osa oli ohimeneviä ja voimakkuudeltaan lieviä tai kohtalaisia. Neutropeniaa voi esiintyä useita kuukausia MabTheran annon jälkeen (ks. Kohta 4.4).
Lumekontrolloiduissa kliinisissä tutkimuksissa 0,94%: lle (13/382) MabTheraa saaneista potilaista ja 0,27%: lle (2/731) lumelääkettä saaneista potilaista kehittyi vaikea neutropenia.
Neutropeenisia tapahtumia, mukaan lukien vaikea ja jatkuva myöhään alkava neutropenia, joista osa on liittynyt kuolemaan johtaviin infektioihin, on raportoitu harvoin markkinoille tulon jälkeen.
Iho ja ihonalainen kudos
Hyvin harvoin on raportoitu toksisen epidermaalisen nekrolyysin (Lyellin oireyhtymä) ja Stevens-Johnsonin oireyhtymän tapauksia, joista osa on johtanut kuolemaan.
Laboratorioiden poikkeavuudet
Hypogammaglobulinemiaa (IgG tai IgM alle normaalin alarajan) on havaittu MabTheraa saaneilla nivelreumapotilailla. Yleisten tai vakavien infektioiden määrä ei lisääntynyt alhaisen IgG- tai IgM -tason jälkeen (ks. Kohta 4.4).
Pieniä hypogammaglobulinemiaan liittyviä spontaaneja ja kirjallisia tapauksia, joissain tapauksissa vakavia ja jotka vaativat pitkäaikaista immunoglobuliinikorvaushoitoa, on havaittu MabTheraa saaneilla lapsipotilailla. Pitkäaikaisen B-solujen ehtymisen seurauksia lapsipotilailla ei tunneta.
Kokemusta granulomatoosista polyangiitin ja mikroskooppisen polyangiitin kanssa
Kliinisessä tutkimuksessa granulomatoosista, johon liittyi polyangiitti ja mikroskooppinen polyangiitti, 99 potilasta sai MabTheraa (375 mg / m2, kerran viikossa 4 viikon ajan) ja glukokortikoideja (ks. Kohta 5.1).
Luettelo haittavaikutuksista taulukon muodossa
Taulukossa 3 luetellut haittavaikutukset edustavat kaikkia haittavaikutuksia, joita esiintyi ilmaantuvuudella ≥ 5% MabThera -ryhmässä.
Taulukko 3. Haittavaikutukset, joita esiintyy vuonna ≥ 5% potilaista, jotka saivat MabTheraa ja useammin kuin vertailuryhmä 6 kuukauden keskeisessä kliinisessä tutkimuksessa.
Valikoima haittavaikutuksia
Infuusioon liittyvät reaktiot
Infuusioreaktiot kliinisissä tutkimuksissa, jotka viittasivat granulomatoosiin polyangiitilla ja mikroskooppisella polyangiitilla, määriteltiin haittavaikutuksiksi, jotka ilmenivät 24 tunnin kuluessa infuusiosta, ja tutkijat pitivät infuusioon liittyvänä turvallisuuspopulaatiossa. 99 potilasta sai MabTheraa ja 12% koki vähintään yhden IRR -reaktion. Kaikki IRR: t olivat luokkaa 1 tai 2 CTC: n mukaan. Yleisimpiä IRR -reaktioita olivat sytokiinien vapautumisoireyhtymä, kuumat aallot, kurkun ärsytys ja vapina.MabTheraa annettiin yhdessä laskimonsisäisten glukokortikoidien kanssa, mikä voi vähentää näiden tapahtumien esiintyvyyttä ja vakavuutta.
Infektiot
99 MabTheralla hoidetulla potilaalla infektioiden kokonaismäärä oli noin 237 /100 potilasvuotta (95%: n luottamusväli 197--285) 6 kuukauden ensisijaisessa päätetapahtumassa.Tulehdukset olivat pääasiassa lieviä tai kohtalaisia ja koostuivat pääasiassa hengitystieinfektioista. vakavia infektioita oli noin 25 /100 potilasvuotta.MabThera-ryhmän yleisimmin raportoitu vakava infektio oli keuhkokuume, jonka esiintyvyys oli 4%.
Kasvaimet
Pahanlaatuisten kasvainten ilmaantuvuus potilailla, joita hoidettiin MabTheralla kliinisissä tutkimuksissa, joissa viitattiin granulomatoosiin, johon liittyi polyangiitti ja mikroskooppinen polyangiitti, oli 2,00 / 100 potilasvuotta yhteisen tutkimuksen päättymispäivänä (kun viimeinen potilas suoritti seuranta-ajan).-ylös). Standardoidun ilmaantuvuussuhteen perusteella pahanlaatuisten kasvainten ilmaantuvuus näyttää olevan samanlainen kuin aiemmin raportoitu potilailla, joilla on ANCA: han liittyvä vaskuliitti.
Kardiovaskulaariset haittavaikutukset
Sydäntapahtumia esiintyi noin 273 /100 potilasvuotta (95 %: n luottamusväli 149-470) 6 kuukauden ensisijaisessa päätetapahtumassa.Vakavien sydäntapahtumien esiintyvyys oli 2,2 100 potilasvuotta kohden (95 %: n luottamusväli 3-15) Yleisimmin raportoitu haittatapahtuma oli takykardia (4%) ja eteisvärinä (3%) (ks. Kohta 4.4).
Neurologiset tapahtumat
Positiivisen palautuvan enkefalopatian oireyhtymän (PRES) / posteriorisen palautuvan leukoenkefalopatian oireyhtymän (RPLS) tapauksia on raportoitu. Merkkejä ja oireita olivat näköhäiriöt, päänsärky, kouristukset ja muuttunut henkinen tila, johon liittyi hypertensio tai ilman sitä. PRES / RPLS -diagnoosi vaatii vahvistuksen aivokuvantamisen avulla. Kuvatuissa tapauksissa oli tunnettuja PRES / RPLS -riskitekijöitä, mukaan lukien potilaiden perussairaus, verenpaine, immunosuppressiivinen hoito ja / tai kemoterapia.
B -hepatiitin uudelleenaktivointi
Pieniä tapauksia hepatiitti B: n uudelleenaktivoinnista, joista osa on johtanut kuolemaan, on raportoitu potilailla, joilla on granulomatoosi, polyangiitti ja mikroskooppinen polyangiitti, joita on hoidettu MabTheralla markkinoille tulon jälkeen.
Hypogammaglobulinemia
Hypogammaglobulinemiaa (IgA, IgG tai IgM alle normaalin alarajan) on havaittu MabTheraa saaneilla potilailla, joilla on granulomatoosi, polyangiitti ja mikroskooppinen polyangiitti. Kuuden kuukauden pituisessa, monikeskuksisessa, satunnaistetussa, kaksoissokkoutetussa, aktiivisesti kontrolloidussa ei-alemmuustutkimuksessa MabThera-ryhmässä 27%: lla, 58%: lla ja 51%: lla potilaista, joilla oli normaali lähtötason immunoglobuliinipitoisuus, oli alhainen IgA-taso, IgG ja IgM, vastaavasti 25%, 50% ja 46% syklofosfamidiryhmästä. Yleisiä infektioita tai vakavia infektioita ei havaittu potilailla, joilla oli alhainen IgA-, IgG- tai IgM -pitoisuus.
Neutropenia
Monikeskustutkimuksessa, satunnaistetussa, kaksoissokkoutetussa, aktiivisesti kontrolloidussa ei-alemmuustutkimuksessa, jossa MabTheraa käytettiin granulomatoosiin polyangiitin ja mikroskooppisen polyangiitin kanssa, 24% MabThera-ryhmän potilaista (yksi sykli) ja 23% potilaista syklofosfamidiryhmässä on saanut CTC -asteen 3 tai korkeamman neutropenian. Neutropenia ei liittynyt havaittujen vakavien infektioiden lisääntymiseen MabTheraa saaneilla potilailla. Useiden MabThera -hoitojaksojen vaikutusta neutropenian kehittymiseen potilailla, joilla on granulomatoosi, johon liittyy polyangiitti ja mikroskooppinen polyangiitti, ei ole tutkittu kliinisissä tutkimuksissa.
Ihon ja ihonalaisen kudoksen häiriöt:
Toksisen epidermaalisen nekrolyysin (Lyellin oireyhtymä) ja Stevens-Johnsonin oireyhtymää, joista osa on johtanut kuolemaan, on raportoitu hyvin harvoin.
Epäillyistä haittavaikutuksista ilmoittaminen
Ilmoittaminen epäillyistä haittavaikutuksista, jotka ilmenevät lääkkeen myyntiluvan myöntämisen jälkeen, on tärkeä, koska se mahdollistaa lääkkeen hyöty -haitta -tasapainon jatkuvan seurannan Terveydenhuollon ammattilaisia pyydetään ilmoittamaan kaikista epäillyistä haittavaikutuksista kansallisen ilmoitusjärjestelmän kautta.
04.9 Yliannostus
Kokemusta ihmisillä tehdyistä kliinisistä tutkimuksista, joissa annokset ovat suurempia kuin laskimonsisäiseen MabThera -valmisteeseen hyväksytyt annokset, on vain vähän. Suurin ihmisillä testattu MabTheran laskimonsisäinen annos on tähän mennessä testattu 5000 mg (2250 mg / m2). potilailla, joilla on krooninen lymfaattinen leukemia. Muita turvallisuusmerkkejä ei tunnistettu.
Yliannostusta sairastavien potilaiden on lopetettava infuusio välittömästi ja seurattava tarkasti.
Markkinoille tulon jälkeen on raportoitu viisi MabThera -yliannostustapausta. Kolme näistä tapauksista ei raportoinut haittavaikutuksista. Kaksi raportoitua haittatapahtumaa olivat influenssan kaltaiset oireet 1,8 g rituksimabiannoksella ja kuolemaan johtava hengitysvajaus 2 g rituksimabiannoksella.
05.0 FARMAKOLOGISET OMINAISUUDET
05.1 Farmakodynaamiset ominaisuudet
Farmakoterapeuttinen ryhmä: syöpälääkkeet, monoklonaaliset vasta -aineet, ATC -koodi: L01X C02.
Rituksimabi sitoutuu spesifisesti transmembraaniseen CD20-antigeeniin, ei-glykosyloituun fosfoproteiiniin, jota esiintyy pre-B-lymfosyyteissä ja kypsissä B-lymfosyyteissä.
CD20 esiintyy normaaleissa ja neoplastisissa B-soluissa, mutta ei hematopoieettisissa kantasoluissa, pro-B-soluissa, normaaleissa plasmasoluissa tai muissa normaaleissa kudoksissa. Antigeeniä ei sisällytetä vasta -aineeseen sitoutumisen jälkeen eikä se leviä solun pinnalta. CD20 ei kiertä veressä vapaana antigeeninä eikä siksi kilpaile vasta -aineen sitoutumisen kanssa. Rituksimabin Fab -domeeni sitoutuu B20 -lymfosyyttien CD20 -antigeeniin ja Fc-domeeni voivat aktivoida immuunijärjestelmän efektoritoimintoja, joiden tarkoituksena on aiheuttaa B-solujen hajoamista. Mahdollisia efektorivälitteisen solulyysin mekanismeja ovat komplementeista riippuvainen sytotoksisuus (CDC) sitoutumalla C1q: een ja vasta-aineesta riippuvaiseen solun sytotoksisuuteen (ADCC). ), jota välittää yksi tai useampi Fcy -reseptori granulosyyttien, makrofagien ja NK -solujen pinnalla.Rituksimabin sitoutumisen CD20 -antigeeniin B -lymfosyyteissä on myös osoitettu indusoivan solukuoleman apoptoosilla.
Perifeeristen B -solujen määrä laski alle normaalin ensimmäisen MabThera -annoksen jälkeen. Potilailla, joilla hoidetaan hematologisia syöpiä, B -solujen toipuminen aloitetaan 6 kuukauden kuluessa hoidosta ja yleensä palautuu normaalille tasolle 12 kuukauden kuluessa hoidon päättymisestä, vaikka toipuminen voi olla pidempää joillakin potilailla (toipumisajan mediaani on 23 kuukautta induktion jälkeen) hoito). Potilailla, joilla oli nivelreuma, havaittiin välittömästi perifeerisen veren B -solujen ehtyminen kahden MabThera -annoksen ollessa 1000 mg, ja ne erotettiin 14 päivän välein. Perifeeristen B -solujen määrä alkaa kasvaa viikosta 24 lähtien, ja useimmilla potilailla on havaittu toipumisen merkkejä viikolta 40 alkaen sekä MabTheraa annettaessa yksinään että yhdessä metotreksaatin kanssa. Pieni osa potilaista koki pitkittynyttä perifeeristen B -solujen ehtymistä vähintään 2 vuoden ajan viimeisen MabThera -annoksen jälkeen.Potilailla, joilla on granulomatoosi, polyangiitti tai mikroskooppinen polyangiitti, perifeerisen veren B -solujen määrä laski 2: een ja pysyi tällä tasolla useimmat potilaat asti Aika piste 6 kuukautta. Useimmilla potilailla (81%) ilmeni merkkejä B -solujen rekonstituutiosta, joiden määrä oli> 10 solua / μl 12 kuukauden kuluessa, ja saavutti 87% potilaista 18 kuukauteen mennessä.
Kliininen kokemus non-Hodgkinin lymfoomasta ja kroonisesta lymfaattisesta leukemiasta
Follikulaarinen lymfooma
Monoterapia
Ensimmäinen hoito, viikoittain 4 annosta
Keskeisessä tutkimuksessa 166 potilasta, joilla oli uusiutunut tai kemoresistentti heikkolaatuinen tai follikulaarinen B-solu NHL, sai 375 mg / m2 MabTheraa laskimoinfuusiona kerran viikossa neljän viikon ajan. Kokonaisvasteiden (ORR) prosenttiosuus väestöstä arvioitiin "aikomus käsitellä analyysiä (ITT) oli 48% (95%: n luottamusväli 41% - 56%), 6% täydellisiä vasteita (CR) ja 42% osittaisia vasteita (PR). Mediaaniaika etenemiseen (TTP) ennusteessa vasteeseen vastanneilla potilailla oli 13,0 kuukautta. Alaryhmäanalyysissä ORR oli suurempi potilailla, joilla oli IWF -histologinen alatyyppi B, C ja D verrattuna potilaisiin, joilla oli IWF -histologinen alatyyppi A (58% vs 12%), potilailla, joiden leesion halkaisija oli suurempi 7 cm (53% vs. 38%) ) ja potilailla, joilla on kemoherkkä uusiutuminen, verrattuna potilaisiin, joilla on kemoresistentti uusiutuminen (määritelty vasteen kestoksi)
ORR potilailla, jotka olivat aiemmin saaneet autologista luuydinsiirtoa (ABMT), oli 78% verrattuna 43%: iin potilaista, jotka eivät olleet aiemmin saaneet ABMT: tä. , ekstranodaalisen sairauden esiintymisellä ei ollut tilastollisesti merkittävää vaikutusta (Fisherin tarkka testi) MabThera -vasteeseen.Vasteprosentin ja luuytimen osallistumisen välillä havaittiin tilastollisesti merkitsevä korrelaatio. ilman luuytimen osallistumista (p = 0,0186). Tätä havaintoa ei tue ns. "vaiheittainen logistinen regressio" -analyysi, jossa seuraavat tekijät tunnistettiin ennustavaksi tekijäksi: histologinen tyyppi, lähtötilanteen bcl-2-positiivisuus, resistenssi viimeiselle kemoterapialle ja massiivinen sairaus.
Ensimmäinen hoito, viikoittain 8 annosta
Monikeskustutkimuksessa, jossa oli yksi käsivarsi, 37 potilasta, joilla oli uusiutunut tai kemoresistentti, heikkolaatuinen tai follikulaarinen B-solu NHL, sai MabTheraa 375 mg / m2 viikoittain laskimonsisäisenä infuusiona kahdeksan annoksen ajan. ORR oli 57% (95%: n luottamusväli (CI): 41% - 73%; CR 14%, PR 43%).
Ensimmäinen hoito, massiivinen sairaus, viikoittain 4 annosta
Kolmen tutkimuksen tietokannassa 39 potilasta, joilla oli uusiutunut tai kemoresistentti NHL, massiivinen sairaus (yksittäinen vaurio ≥ 10 cm), heikkolaatuinen tai follikulaarinen B-solusairaus, saivat MabTheraa 375 mg / m2 viikoittain laskimonsisäisenä infuusiona neljälle annoksia. ORR oli 36% (95%: n luottamusväli 21% - 51%; CR 3%, PR 33%).
Uudelleenhoito, viikoittain 4 annosta
Monikeskustutkimuksessa, jossa oli yksi käsivarsi, 58 potilasta, joilla oli uusiutunut tai kemoresistentti heikkolaatuinen tai follikulaarinen B-solu NHL ja jotka olivat saavuttaneet objektiivisen kliinisen vasteen edellisestä MabThera-hoidosta, saivat 375 mg / m2 MabTheraa. viikoittainen laskimonsisäinen infuusio neljälle annokselle. Kolme näistä potilaista oli saanut kaksi MabThera -kurssia ennen ilmoittautumista ja sai siten kolmannen kurssin tutkimuksessa. Kaksi potilasta hoidettiin kahdesti tutkimuksessa. Tutkimuksen 60 uusintahoidon aikana ORR oli 38% (95%: n luottamusväli 26% - 51%; 10% CR, 28% PR). . Nämä tiedot ovat parempia kuin MTPTheran ensimmäisen hoitojakson (12,4 kuukautta) jälkeen saatu TTP.
Ensimmäinen hoito yhdistettynä kemoterapiaan
Satunnaistetussa avoimessa kliinisessä tutkimuksessa yhteensä 322 aiemmin hoitamatonta potilasta, joilla oli follikulaarinen lymfooma, satunnaistettiin joko CVP-solunsalpaajahoitoon (syklofosfamidi 750 mg / m2, vinkristiini 1,4 mg / m2 enintään 2 mg päivänä 1 ja prednisoloni 40 mg / m2 / vrk päivinä 1-5) 3 viikon välein 8 syklin ajan tai MabThera 375 mg / m2 yhdessä CVP: n (R-CVP) kanssa. MabTheraa annettiin kunkin hoitojakson ensimmäisenä päivänä. Yhteensä 321 potilasta (162 R-CVP, 159 CVP) sai hoitoa, ja niiden tehokkuus analysoitiin. Potilaiden seurannan mediaani oli 53 kuukautta. R-CVP: stä oli merkittävää hyötyä CVP: hen verrattuna ensisijaisena päätetapahtumana eli ajankohtana hoidon epäonnistumiseen (27 kuukautta vs. 6,6 kuukautta, p
Ero hoitoryhmien välillä kokonaiseloonjäämisessä osoitti merkittävää kliinistä eroa (p = 0,029, log-rank-testi kerrostettu keskuksen mukaan): 53 kuukauden eloonjäämisaste oli 80,9% R-ryhmän potilaista. CVP verrattuna 71,1%: iin potilaita CVP -ryhmässä.
Tulokset kolmesta muusta satunnaistetusta tutkimuksesta, joissa käytettiin MabTheraa yhdessä muiden kuin CVP-solunsalpaajahoitojen kanssa (CHOP, MCP, CHVP / Interferon-a), osoittivat myös merkittäviä parannuksia vasteissa, ajasta riippuvissa parametreissa ja kokonaiseloonjäämisessä. Kaikkien neljän tutkimuksen tärkeimmät tulokset on esitetty taulukossa 4.
Taulukko 4 Yhteenveto keskeisistä havainnoista neljästä satunnaistetusta vaiheen III tutkimuksesta, joissa arvioitiin MabTheran hyötyä erilaisilla solunsalpaajahoidoilla follikulaarisessa lymfoomassa.
EFS - Tapahtumaton selviytyminen
TTP - Aika etenemiseen tai kuolemaan
PFS - Progression Free Survival
TTF - Aika hoidon epäonnistumiseen
Käyttöjärjestelmän prosenttiosuudet - eloonjäämisasteet analyysin aikaan
Ylläpitohoito
Aiemmin hoitamaton follikulaarinen lymfooma
Prospektiivisessa, avoimessa, kansainvälisessä, monikeskustutkimuksen, vaiheen III tutkimuksessa 1193 potilasta, joilla oli aiemmin hoitamaton pitkälle edennyt follikulaarinen lymfooma, sai induktiohoitoa R-CHOP (n = 881), R-CVP (n = 268) tai R-FCM (n = 44), tutkijan valinnan perusteella. Yhteensä 1078 potilasta vastasi induktiohoitoon, joista 1018 satunnaistettiin saamaan MabThera -ylläpitohoitoa (n = 505) tai havaintoa (n = 513). Molemmat hoitoryhmät olivat tasapainossa lähtötilanteen ominaisuuksien ja sairauden tilan suhteen. Ylläpitohoito MabTheralla koostui yhdestä MabThera -infuusiosta, joka annettiin 375 mg / m2 kehon pinta -alaa 2 kuukauden välein taudin etenemiseen saakka tai enintään 2 vuoden ajan.
Keskimääräisen 25 kuukauden havaintoajan jälkeen satunnaistamisesta MabThera-ylläpitohoito paransi kliinisesti merkitsevää ja tilastollisesti merkitsevää parannusta tutkijan arvioimassa etenemisvapaan eloonjäämisen (PFS) ensisijaisessa päätetapahtumassa verrattuna havaintoon potilailla, joilla oli aiemmin hoitamaton follikulaarinen lymfooma (taulukko 5).
Merkittävää hyötyä MabThera-ylläpitohoidosta havaittiin myös toissijaisten päätetapahtumien vapaan eloonjäämisen (EFS), seuraavan lymfoomahoidon (TNLT) aika, seuraavan kemoterapian aika (TNCT) ja kokonaisvaste (ORR) (taulukko 5) . Ensisijaisen analyysin tulokset vahvistettiin pidemmällä seurannalla (havaintoajan mediaani: 48 kuukautta ja 73 kuukautta), ja päivitetyt tulokset lisättiin taulukkoon 5 havainnollistamaan vertailuaikaa 25, 48 ja 73 kuukaudet.
Taulukko 5 Huoltovaihe: Yhteenveto MabTheran vs.havainto 73 kuukauden keskimääräisen havaintoajan jälkeen (verrattuna 25 kuukauden mediaanitarkkausaikaan perustuvan ensisijaisen analyysin tuloksiin ja 48 kuukauden havaintoajan mediaaniin perustuvaan päivitettyyn analyysiin)
* Huoltojen / havaintojen lopussa; # p-arvot chi-neliötestistä.
Pääarvot vastaavat 73 kuukauden mediaanihuollon kestoa, kursivoidut suluissa olevat arvot vastaavat 48 kuukauden keskimääräistä havaintoaikaa ja suluissa olevat arvot vastaavat 25 kuukauden havaintoajan mediaania analyysi).
PFS: eteneminen ilman taudin etenemistä; EFS: tapahtumaton selviytyminen; Käyttöjärjestelmä: kokonaiselossaoloaika; TNLT: aika seuraavaan lymfoomahoitoon; TNCT: aika seuraavaan solunsalpaajahoitoon; ORR: kokonaisvaste: NR: ei tavoitettavissa katkaista kliininen; TAI: kertoimien suhde.
Ylläpitohoidosta MabTheralla oli johdonmukaista hyötyä kaikissa testatuissa alaryhmissä: sukupuoli (mies, nainen), ikä (= 60 vuotta), FLIPI-pisteet (= 3), induktiohoito (R-CHOP, R-CVP tai R-FCM) ja riippumatta induktiohoidon vasteen laadusta (CR, CRu tai PR). Ylläpitohoidon hyödyn tutkimusanalyysit osoittivat vähäisempää vaikutusta iäkkäillä potilailla (> 70 -vuotiaat), mutta otoskoko oli pieni.
Uusiutunut / tulenkestävä follikulaarinen lymfooma
Prospektiivisessa, avoimessa, kansainvälisessä, monikeskustutkimuksen, vaiheen III tutkimuksessa 465 potilasta, joilla oli uusiutunut / resistentti follikulaarinen lymfooma, satunnaistettiin ensimmäisessä vaiheessa CHOP-hoitoon (syklofosfamidi, doksorubisiini, vinkristiini ja prednisoloni; n = 231) o MabThera plus CHOP (R-CHOP, n = 234). Molemmat hoitoryhmät olivat tasapainossa lähtötilanteen ominaisuuksien ja sairauden tilan suhteen. Yhteensä 334 potilasta, jotka saavuttivat täydellisen tai osittaisen remission induktiohoidon jälkeen, satunnaistettiin toiseen vaiheeseen MabThera -ylläpitohoitoon (n = 167) tai havaintoon (n = 167). Ylläpitohoito MabTheralla koostui yhdestä MabThera -infuusiosta 375 mg / m2 kehon pinta -alaa 3 kuukauden välein taudin etenemiseen saakka tai enintään kahden vuoden ajan.
Lopullinen tehokkuusanalyysi sisälsi kaikki potilaat, jotka oli satunnaistettu tutkimuksen molempiin osiin. Kun induktiovaiheeseen satunnaistetuilla potilailla havaittu mediaani oli 31 kuukautta, R-CHOP paransi merkittävästi lymfoomaa sairastavien potilaiden ennustetta. CHOP (katso taulukko 6).
Taulukko 6 Induktiovaihe: luettelo CHOP: n tehokkuustuloksista verrattuna R-CHOP: iin (havaintoajan mediaani 31 kuukautta).
1) Arvio laskettiin suhteellisella riskillä.
2) Viimeisin kasvainvaste tutkijan arvioimana. "Ensisijainen" tilastollinen "vasteen" testi oli CR: n ja PR: n trenditesti suhteessa vastaamatta jättämiseen (s
Lyhenteet: EI, ei saatavilla; ORR: prosenttiosuus maailmanlaajuisista vastauksista; CR: täydellinen vastaus; PR: osittainen vaste.
Tutkimuksen ylläpitovaiheeseen satunnaistetuilla potilailla havaittu mediaani oli 28 kuukautta satunnaistamisesta ylläpitoon. Ylläpitohoito MabTheralla johti kliinisesti merkittävään ja tilastollisesti merkitsevään paranemiseen ensisijaisessa päätetapahtumassa, PFS (aika satunnaistamisesta ylläpitoon uusiutumiseen, taudin etenemiseen tai kuolemaan) verrattuna pelkästään havaintoon (p
Taulukko 7 Ylläpitovaihe: luettelo MabTheran tehon tuloksista suhteessa havaintoon (28 kuukauden keskimääräinen havaintoaika).
NR: ei saavutettu; a: Koskee vain potilaita, jotka saavuttavat CR: n.
MabThera-ylläpitohoidon hyöty vahvistettiin kaikissa analysoiduissa alaryhmissä riippumatta induktio-ohjelmasta (CHOP tai R-CHOP) tai induktiohoidon vasteen laadusta (CR tai PR) riippumatta (taulukko 7). Ylläpitohoito MabTheralla pidentää merkittävästi PFS: n mediaania potilailla, jotka vastasivat CHOP -induktiohoitoon (PFS -mediaani 37,5 kuukautta vs 11,6 kuukautta, p
Diffuusiinen suuri B-solun non-Hodgkinin lymfooma
Satunnaistetussa, avoimessa tutkimuksessa yhteensä 399 aiemmin hoitamatonta iäkästä potilasta (60-80-vuotiaat), joilla oli diffuusi suuri B-solulymfooma, sai tavanomaisen CHOP-kemoterapian (syklofosfamidi 750 mg / m2, doksorubisiini 50 mg / m2), vinkristiini 1,4 mg / m2-enintään 2 mg päivänä 1 ja prednisoloni 40 mg / m2 / vrk päivinä 1-5) joka kolmas viikko kahdeksan jakson ajan tai MabThera 375 mg / m2 yhdessä CHOP: n kanssa (R -CHOP).
MabThera annettiin hoitojakson ensimmäisenä päivänä.
Tehoa koskevien tietojen lopullinen analyysi sisälsi kaikki satunnaistetut potilaat (197 CHOP, 202 R-CHOP) ja sen seurannan mediaani oli noin 31 kuukautta.Kaksi hoitoryhmää olivat tasapainossa taudin ominaisuuksien ja lähtötilanteen suhteen. Lopullinen analyysi vahvisti, että R-CHOP-hoitoon liittyi kliinisesti merkittävä ja tilastollisesti merkitsevä parannus tapahtumaton eloonjäämisen kestoon (ensisijainen tehokkuusparametri; tapahtumat olivat kuolema, uusiutuminen tai lymfooman eteneminen tai siirtyminen uuteen lymfoomahoito) (p = 0,0001). Kaplan-Meierin arvio tapahtumittoman eloonjäämisen mediaanista oli 35 kuukautta R-CHOP-ryhmässä verrattuna 13 kuukauteen CHOP-ryhmässä, mikä pienentää riskiä 41%. 24 kuukauden kuluttua kokonaiselossaoloarvio oli 68,2% R-CHOP-ryhmässä ja 57,4% CHOP-ryhmässä. Myöhempi analyysi kokonaiseloonjäämisestä, joka suoritettiin seuranta-ajan mediaanilla 60 kuukautta, vahvisti R-CHOP-hoidon hyödyn verrattuna CHOP: iin (p = 0,0071), mikä pienentää riskiä 32%.
Kaikkien toissijaisten parametrien analyysi (vaste, tauditon eloonjääminen, tauditon eloonjääminen, vasteen kesto) vahvisti R-CHOP-hoidon tehokkuuden verrattuna CHOP: iin. Täydellinen vaste 8 syklin jälkeen oli 76,2% R-CHOP-ryhmässä ja 62,4% CHOP-ryhmässä (p = 0,0028). Taudin etenemisen riski pieneni 46% ja uusiutumisen riski 51%.
Kaikissa potilasryhmissä (sukupuoli, ikä, ikäkohtainen IPI, Ann Arborin vaihe, ECOG, β2-mikroglobuliini, LDH, albumiini, B-oireet, iso tauti, ekstranodaaliset kohdat, luuytimen osallisuus), riskisuhteet tapahtumaton eloonjääminen ja kokonaiselossaolo (RCHOP verrattuna CHOP: iin) olivat alle 0,83 ja 0,95. R-CHOP liittyi parempaan ennusteeseen sekä korkean että matalan riskin potilailla iän mukautetun IPI: n mukaan.
Kliiniset laboratoriotiedot
Vastauksia ei havaittu 67 potilaalta, joille tehtiin ihmisen vasta -aine -hiiri (HAMA) -testi. 356 potilaasta, joille tehtiin HACA -testi, 1,1%: lla (4 potilasta) he saivat positiivisen tuloksen.
Krooninen lymfaattinen leukemia
Kahdessa satunnaistetussa avoimessa tutkimuksessa yhteensä 817 aiemmin hoitamatonta CLL-potilasta ja 552 potilasta, joilla oli uusiutunut / tulenkestävä CLL, satunnaistettiin saamaan CF-solunsalpaajahoitoa (fludarabiini 25 mg / m2, syklofosfamidi 250 mg / m2, päivät 1-3) 4 viikkoa 6 syklin ajan tai MabThera yhdessä FC: n (R-FC) kanssa. MabTheraa annettiin 375 mg / m2: n annoksena ensimmäisen hoitojakson aikana, yksi päivä ennen kemoterapiaa, ja annoksena 500 mg / m2 jokaisen seuraavan hoitojakson päivänä 1. Potilaat suljettiin pois uusiutuneesta / tulenkestävästä CLL -tutkimuksesta, jos he olivat aiemmin saaneet monoklonaalisia vasta -aineita tai jos he olivat refraktorisia (määritelty osittaisen remission saavuttamatta jättämiseksi vähintään 6 kuukaudeksi) fludarabiinille tai jollekin nukleosidianalogille. Yhteensä 810 potilasta (403 R-FC, 407 FC) ensimmäisen linjan tutkimuksessa (taulukko 8a ja taulukko 8b) ja 552 potilasta (276 R-FC, 276 FC) uusiutuneessa / tulenkestävässä tutkimuksessa (taulukko 9), analysoitiin niiden tehokkuus.
Ensimmäisen linjan tutkimuksessa 48,1 kuukauden mediaaniajan jälkeen PFS-mediaani oli 55 kuukautta R-FC-ryhmässä ja 33 kuukautta FC-ryhmässä (p
Kokonaiselossaoloanalyysi osoitti merkittävän hyödyn RFC-hoidosta verrattuna pelkästään CF-solunsalpaajahoitoon (p = 0,0319, log-rank-testi) (taulukko 8a) .PFS-hyötyä havaittiin johdonmukaisesti useimmissa potilaiden alaryhmissä, jotka analysoitiin sairauden lähtötilanteen riskin mukaan (erityisesti Binet AC -vaiheet) ) (taulukko 8b).
Taulukko 8a Kroonisen lymfaattisen leukemian ensilinjan hoito MabThera plus CF: n tehokkuustulosten kuvaus vs. Pelkkä HR - 48,1 kuukauden mediaanitarkkailuaika.
Vastausten prosenttiosuus ja prosenttiosuus CR: stä analysoituna chi-neliötestin mukaan. NR: ei saavutettu; ei: ei
sovellettavissa.
*: Koskee vain potilaita, jotka saavat CR, nPR, PR.
**: Koskee vain potilaita, jotka saavuttavat CR: n.
Taulukko 8b Kroonisen lymfosyyttisen leukemian ensilinjan hoito Riski etenemättömästä eloonjäämisestä Binet-vaiheen (ITT) mukaan-48,1 kuukauden mediaanitarkkailuaika
CI: Luottamusväli.
Uusiutumis- / tulenkestävässä tutkimuksessa etenemisvapaan eloonjäämisen mediaani (ensisijainen päätetapahtuma) oli 30,6 kuukautta R-FC-ryhmässä ja 20,6 kuukautta FC-ryhmässä (p = 0,0002, log-rank-testi).
PFS -hyötyä havaittiin lähes kaikissa potilaiden alaryhmissä, jotka analysoitiin sairauden lähtötilanteen riskin mukaan. R-FC-ryhmässä raportoitiin lievää mutta ei merkittävää paranemista kokonaiseloonjäämisessä verrattuna FC-ryhmään.
Taulukko 9 Uusiutuneen / tulenkestävän kroonisen lymfosyyttisen leukemian hoito - kuvaus MabThera plus HR -hoidon tehokkuustuloksista pelkästään HR: stä (havaintoajan mediaani 25,3 kuukautta).
Vastausten prosenttiosuus ja prosenttiosuus CR: stä analysoituna chi-neliötestin mukaan.
*: koskee vain potilaita, jotka saavat CR: n, nPR: n, PR: n; NR = ei saavutettu; n.a. = ei sovelleta.
**: Koskee vain potilaita, jotka saavuttavat CR: n.
Myös muiden MabTheraa yhdessä muiden solunsalpaajahoitojen (mukaan lukien CHOP, FCM, PC, PCM, bendamustiini ja kladribiini) yhdistelmähoitotutkimusten tulokset aiemmin hoitamattomien ja / tai uusiutuneiden CLL / tulenkestävien potilaiden hoitoon osoittivat "korkean prosenttiosuuden" globaaleista vasteista, joista on hyötyä prosentuaalisena elinaikana, vaikkakin myrkyllisyys on hieman suurempi (erityisesti myelotoksisuus). Nämä tutkimukset tukevat MabTheran käyttöä minkä tahansa kemoterapian kanssa.
Tiedot noin 180 MabThera-hoitoa saaneesta potilaasta osoittivat kliinistä hyötyä (mukaan lukien CR) ja tukevat uudelleenhoitoa MabTheralla.
Pediatriset potilaat
Euroopan lääkevirasto on myöntänyt vapautuksen velvoitteesta toimittaa tutkimustulokset MabThera -valmisteen käytöstä kaikkien pediatristen potilasryhmien hoidossa follikulaarisen lymfooman ja kroonisen lymfaattisen leukemian osalta. Katso kohdasta 4.2 ohjeet käytöstä lapsille.
Kliininen kokemus nivelreumasta
MabTheran teho ja turvallisuus nivelreuman oireiden ja oireiden lievittämisessä potilailla, joiden vaste TNF-estäjille ei ole riittävä, osoitettiin keskeisessä, satunnaistetussa, kontrolloidussa, kaksoissokkoutetussa monikeskustutkimuksessa (tutkimus 1).
Tutkimuksessa 1 arvioitiin 517 potilasta, joilla oli riittämätön vaste tai jotka eivät siedä yhtä tai useampaa TNF -estäjää. Tukikelpoisilla potilailla oli "aktiivinen nivelreuma, joka on diagnosoitu American College of Rheumatology (ACR) -kriteerien mukaan". MabThera annettiin 2 infuusiona i.v. 15 päivän välein. Potilaat saivat 2 x 1000 mg laskimonsisäistä MabThera -infuusiota tai lumelääkettä yhdessä MTX: n kanssa. Kaikki potilaat saivat samanaikaisesti 60 mg prednisolonia suun kautta päivinä 2-7 ja 30 mg päivinä 8-14 ensimmäisen infuusion jälkeen. Ensisijainen päätetapahtuma oli niiden potilaiden osuus, jotka saavuttivat ACR20-vasteen viikolla 24. Potilaita seurattiin yli 24 viikon ajan pitkän aikavälin tavoitteiden saavuttamiseksi, mukaan lukien röntgenkuvaus 56 viikon ja 104 viikon aikana. Tänä aikana 81% alkuperäisestä lumelääkeryhmästä sai MabTheraa viikkojen 24 ja 56 välillä osana "avointa" protokollan jatkotutkimusta.
MabTheran tutkimukset potilailla, joilla on vaiheen niveltulehdus aikaisin (potilaat, joita ei ole aiemmin hoidettu metotreksaatilla ja potilaat, joiden vaste metotreksaatille on riittämätön, mutta joita ei ole vielä hoidettu TNF-alfa-estäjillä) saavuttivat ensisijaiset päätetapahtumansa. MabTheraa ei ole tarkoitettu näille potilaille, koska turvallisuustiedot pitkäaikaisesta MabThera-hoidosta ovat riittämättömiä erityisesti syövän tai PML: n kehittymisen riskin osalta.
Taudin toiminnan tulokset
MabThera yhdessä metotreksaatin kanssa lisäsi merkittävästi niiden potilaiden osuutta, joiden ACR -vaste parani vähintään 20% verrattuna pelkkää metotreksaattia saaneisiin potilaisiin (taulukko 10). Kaikissa keskeisissä tutkimuksissa hoidon hyöty oli samanlainen potilailla iästä, sukupuolesta, kehon pinta -alasta, rodusta, aiempien hoitojen määrästä tai sairauden tilasta riippumatta.
Kliinisesti ja tilastollisesti merkittäviä parannuksia havaittiin myös kaikissa ACR -vasteen yksittäisissä komponenteissa (kivulias ja turvonnut nivelmäärät, potilaan ja lääkärin kokonaisarvio, vammaisuusindeksi (HAQ), kivun arviointi ja C -reaktiivinen proteiini (mg / dl)).
Taulukko 10 Kliinisen vasteen tulokset tutkimuksen 1 ensisijaisessa päätetapahtumassa (ITT -populaatio).
† Tulos 24 viikossa.
Merkittävä ero lumelääkkeeseen + MTX al Aika piste ensisijainen: *** p ≤ 0,0001.
Potilailla, jotka saivat MabTheraa yhdessä metotreksaatin kanssa, DAS28 -arvo laski merkittävästi enemmän (Taudin aktiivisuuspisteet) verrattuna pelkkää metotreksaattia saaneisiin potilaisiin (taulukko 9). Samoin kaikissa tutkimuksissa EULAR -vastaus (Euroopan liiga reumaa vastaan) hyvästä kohtalaiseen saavutettiin huomattavasti enemmän potilaita, jotka saivat MabTheraa ja metotreksaattia kuin potilaat, jotka saivat pelkkää metotreksaattia (taulukko 10).
Radiologinen vaste
Rakenteelliset nivelvauriot todettiin radiologisesti ja ilmaistiin muutoksena modifioidussa terävässä kokonaispistemäärässä (mTSS) ja sen osissa, eroosiopisteessä ja nivelraon kaventumispisteessä.
Tutkimuksessa 1, joka suoritettiin potilailla, joiden vaste oli riittämätön tai jotka eivät siedä hoitoja yhdellä tai useammalla TNF -antagonistilla, jotka saivat MabTheraa yhdessä metotreksaatin kanssa, potilailla oli merkittävästi pienempi röntgenkuvaus viikolla 56 kuin niillä, jotka olivat alun perin saaneet pelkkää metotreksaattia. Alun perin pelkällä metotreksaatilla hoidetuista potilaista 81% sai MabTheraa pelastushoitona viikkojen 16 ja 24 välillä tai tutkimuksen jatkeena ennen viikkoa 56. Lisäksi suurempi osa potilaista, jotka saivat "alkuperäisen MabThera -hoidon" / MTX ei osoittanut eroosioleesioiden etenemistä 56 viikon aikana (taulukko 11).
Taulukko 11 Radiologiset tulokset vuoden kuluttua (mITT -populaatio)
150 potilasta, jotka alun perin satunnaistettiin tutkimuksessa 1 lumelääkettä ja MTX: ää varten, saivat vähintään yhden RTX + MTX -kurssin
Vuodessa.
* s
Nivelvaurioiden etenemisen hidastumista havaittiin myös pitkällä aikavälillä. Kahden vuoden radiografiaanalyysi tutkimuksessa 1 osoitti, että rakenteellisten nivelvaurioiden eteneminen väheni merkittävästi potilailla, jotka saivat MabTheraa yhdessä metotreksaatin kanssa verrattuna pelkkään metotreksaattiin. ja huomattavasti suurempi prosenttiosuus potilaista, joilla nivelvaurio ei ole edennyt yli 2 vuoteen.
Fyysinen toiminta ja elämänlaatu
Vammaisuusindeksin (HAQ-DI) ja astenian (FACIT-Fatigue) merkittäviä laskuja havaittiin MabTheraa saaneilla potilailla verrattuna pelkkää metotreksaattia saaneisiin potilaisiin. Niiden MabTheraa saaneiden potilaiden osuus, joilla oli kliinisesti merkittävä vähäinen ero (MCID) HAQ-DI: ssä (määritelty yksittäisen kokonaispistemäärän pienenemisenä> 0,22), oli myös suurempi kuin pelkkää metotreksaattia saaneilla potilailla. (Taulukko 12) .
Elämänlaadun kannalta merkittävä terveyden paraneminen on osoitettu parantamalla merkittävästi sekä SF-36: n fyysistä terveystulosta (PHS) että mielenterveystulosta (MHS) .Lisäksi merkittävästi suurempi prosenttiosuus potilaista saavutti MCID: n näille pisteille (taulukko 12).
Taulukko 12 Fyysinen toiminta ja elämänlaatutulokset viikolla 24 tutkimuksissa 1.
† Tulokset viikolla 24.
Merkittävä ero lumelääkkeeseen Aika piste ensisijainen: * s
MCID HAQ-DI ≥0,22, MCID SF-36 PHS> 5,42, MCID SF-36 MHS> 6,33.
Teho seropositiivisilla potilailla, joilla on auto-vasta-aineita (RF- tai anti-CCP)
Reumatoidinen tekijä (RF) ja / tai syklinen peptidisitrullinaatti (anti-CCP) seropositiiviset potilaat, jotka saivat MabTheraa yhdessä metotreksaatin kanssa, osoittivat paremman vasteen kuin potilaat, jotka olivat negatiivisia molemmille.
Tehokkuustulokset MabThera-hoitoa saaneilla potilailla analysoitiin autovasta-aineiden tilan perusteella ennen hoidon aloittamista. Viikolla 24 potilailla, jotka olivat lähtötilanteessa seropositiivisia RF- ja / tai anti-CCP-vasta-aineille, saavutettiin merkittävästi suurempi ACR20- ja 50-vaste kuin seronegatiivisilla potilailla (p = 0,0312 ja p = 0,0096) (taulukko 13). Nämä tulokset toistettiin viikolla 48, jolloin autovasta-aineiden seropositiivisuus lisäsi merkittävästi ACR70: n saavuttamisen todennäköisyyttä. Viikolla 48 seropositiiviset potilaat saavuttavat ACR-vasteen 2-3 kertaa todennäköisemmin kuin seronegatiiviset potilaat. Seropositiivisilla oli myös merkittävästi pienempi DAS28 -ESR kuin seronegatiiviset potilaat.
Taulukko 13 Yhteenveto tehosta perustuen autovasta -aineiden lähtötasoon.
Merkittävät tasot määriteltiin seuraavasti * s
Pitkäaikainen teho toistuvilla hoitokursseilla
MabThera-hoito yhdessä metotreksaatin kanssa useiden syklien aikana paransi dramaattisesti nivelreuman kliinisiä oireita ja oireita, kuten ACR-, DAS28-VES- ja EULAR-vasteet osoittavat, ja ne olivat ilmeisiä kaikissa tutkituissa populaatioissa. Niitä havaittiin. fyysinen toiminta, kuten HAQ-DI-pisteet osoittavat, ja prosenttiosuus potilaista, jotka saavuttivat MCID: n HAQ-DI: lle.
Tulokset kliinisestä laboratoriosta
Kliinisissä tutkimuksissa yhteensä 392 potilaalla 3095 (12,7%) nivelreumapotilaalla oli positiivinen HACA -tulos MabThera -hoidon jälkeen. Useimmilla potilailla HACA: n puhkeamiseen ei liittynyt kliinistä pahenemista tai lisääntynyttä reaktioriskiä seuraaviin infuusioihin.HACA: n esiintyminen voi liittyä infuusio- tai allergisten reaktioiden pahenemiseen seuraavien hoitojaksojen toisen infuusion jälkeen.
Pediatriset potilaat
Euroopan lääkevirasto on myöntänyt vapautuksen velvoitteesta toimittaa tutkimustulokset MabThera -valmisteen käytöstä kaikissa pediatristen potilasryhmien autoimmuunisairauksissa, ks. Kohta 4.2 ohjeet käytöstä pediatristen potilaiden hoidossa.
Kliininen kokemus granulomatoosista polyangiitilla (Wegenerin) ja mikroskooppisella polyangiitilla Yhteensä 197 potilasta, jotka olivat 15 -vuotiaita ja sitä vanhempia ja joilla oli aktiivinen ja vaikea polyangiitti, polyangiitti (75%) ja mikroskooppinen polyangiitti (24%), ja hoidettiin monikeskuksessa, satunnaistettu, kaksoissokkoutettu, aktiivinen vertailu, joka ei ole huonompi.
Potilaat satunnaistettiin suhteessa 1: 1 saamaan joko oraalista syklofosfamidia päivittäin (2 mg / kg / vrk) 3-6 kuukauden ajan tai MabTheraa (375 mg / m2) kerran viikossa 4 viikon ajan. Kaikki potilaat syklofosfamidiryhmässä saivat atsatiopriini-ylläpitohoitoa seurannan aikana. Molempien käsivarsien potilaat saivat 1000 mg laskimonsisäistä bolusmetyyliprednisolonia (tai muuta vastaavaa glukokortikoidiannosta) päivässä 1-3 päivän ajan ja sen jälkeen suun kautta otettavaa prednisonia (1 mg / kg / vrk, enintään 80 mg / vrk). Prednisonin vähentäminen saatiin päätökseen kuuden kuukauden kuluessa tutkimushoidon aloittamisesta. Ensisijainen päätetapahtuman mitta oli täydellisen remission saavuttaminen 6 kuukauden kuluttua, Birminghamin vaskuliittitoiminta Wegenerin granulomatoosille (BVAS / WG) 0 ja glukokortikoidihoidon puuttumiselle. Oletusarvoinen ei-huonompi marginaali hoitojen väliselle erotukselle oli 20%. Tutkimus osoitti, että MabThera ei ollut huonompi kuin syklofosfamidi täydelliseen remissioon (CR) 6 kuukauden kohdalla (taulukko 14). Tehoa havaittiin sekä äskettäin diagnosoiduilla potilailla että potilailla, joilla oli uusiutuva sairaus (taulukko 15).
Taulukko 14 Prosenttiosuus potilaista, jotka saivat täydellisen remission 6 kuukauden kuluttua (hoitoaikana oleva väestö *).
Taulukko 15 Täydellinen remissio 6 kuukauden kuluttua sairauden tilasta.
Pahimman tapauksen attribuutiota sovelletaan potilaisiin, joiden tiedot puuttuvat.
Täydellinen remissio 12 ja 18 kuukauden iässä
MabThera -ryhmässä 48% potilaista saavutti CR: n 12 kuukauden kohdalla ja 39% potilaista CR: n 18 kuukauden kuluttua. Potilailla, joita hoidettiin syklofosfamidilla (jota seurasi atsatiopriini täydellisen remission ylläpitämiseksi), 39% potilaista saavutti CR: n 12 kuukauden kuluttua ja 33% potilaista CR: n 18 kuukauden kuluttua. Kuukaudesta 12 kuukauteen 18 havaittiin 8 uusiutumista MabThera -ryhmässä ja 4 syklofosfamidiryhmässä.
Uudelleenhoito MabTheralla
Tutkijan arvion perusteella 15 potilasta sai toisen MabThera -hoitojakson taudin uusiutumisen hoitoon, joka tapahtui 6–18 kuukauden kuluttua ensimmäisestä MabThera -hoitojaksosta. Tämänhetkisen tutkimuksen rajoitetut tiedot estävät johtopäätöksiä lääkkeen tehosta myöhemmillä MabThera -kursseilla granulomatoosipotilailla, joilla on polyangiitti ja mikroskooppinen polyangiitti.
Jatkuva immunosuppressiivinen hoito voi olla erityisen tarkoituksenmukaista potilailla, joilla on uusiutumisriski (esim. Joilla on aiemmin ollut uusiutumisia ja granulomatoosi ja polyangiitti, tai potilailla, joilla on B-solujen rekonstituutio PR3-ANCA: n lisäksi seurannan aikana). Kun remissio on saavutettu MabThera -hoidolla, immunosuppressiivisen hoidon jatkamista voidaan harkita uusiutumisen estämiseksi. MabTheran tehoa ja turvallisuutta ylläpitohoidossa ei ole varmistettu.
Laboratoriokokeet
Yhteensä 23/99 (23%) tutkimuksessa MabTheraa saaneista potilaista osoitti positiivisen HACA -arvon 18 kuukauden kuluessa. Yksikään 99 potilaasta, jotka saivat MabTheraa, ei ollut HACA -positiivinen seulonnassa. HACA: n kehittymisen kliininen merkitys MabTheralla hoidetuilla potilailla on epäselvä.
05,2 "Farmakokineettiset ominaisuudet
Non-Hodgkinin lymfooma
Perustuu "populaatiofarmakokineettiseen analyysiin 298 NHL -potilaasta, jotka saivat" yhden tai useamman MabThera -infuusion yksin tai yhdistelmänä CHOP -hoidon kanssa (käytetyt MabThera -annokset 100-500 mg / m2), tyypilliset populaatioarviot epäspesifinen puhdistuma (CL1), spesifinen puhdistuma (CL2), johon todennäköisesti liittyi B -soluja tai tuumorimassa, ja keskusosaston jakautumistilavuus (V1) olivat 0,14 l / vrk, 0,59 l / vrk ja 2,7 l. MabTheran arvioitu terminaalisen eliminaation puoliintumisajan mediaani oli 22 päivää (vaihteluväli: 6,1-52 päivää) Lähtötilanteen CD19-positiivinen solumäärä ja mitattavissa olevien kasvainleesioiden halkaisija vaikuttivat osittain MabTheran CL2-vaihteluihin, kuten 161: stä saadut tiedot osoittavat potilaat, jotka saivat 375 mg / m2 laskimonsisäisenä infuusiona 4 viikoittaista annosta.Potilailla, joilla oli suurempi CD19-positiivinen solumäärä tai suurempia kasvainleesioita, oli korkeampi CL2. -positiivinen solumäärä ja kasvainleesion halkaisija. V1 vaihteli kehon pinta -alan mukaan (Kehon pinta -ala, BSA) ja CHOP -hoito. Tämä vaihtelu V1: ssä (27,1% ja 19,0%), joka määritettiin BSA -alueen (1,53-2,32 m2) ja samanaikaisen CHOP -hoidon perusteella, oli suhteellisen pieni.Ikä, sukupuoli ja suorituskyky WHO: n asemalla ei ollut vaikutusta MabTheran farmakokinetiikkaan. analyysi viittaa siihen, että MabThera -annoksen muuttaminen minkä tahansa arvioidun kovarianssin kanssa ei todennäköisesti vähennä merkittävästi sen farmakokineettistä vaihtelua.
MabThera, joka annettiin laskimonsisäisenä infuusiona 375 mg / m2 viikoittain 4 annoksena 203: lle NHL -potilaalle, jotka eivät olleet saaneet MabTheraa, johti keskimääräiseen Cmax -arvoon 486 mcg / ml neljännen infuusion jälkeen (vaihteluväli: 77,5-996, 6 mcg / ml). Rituksimabi havaittiin potilaan seerumissa 3 - 6 kuukautta viimeisen hoidon päättymisen jälkeen.
375 mg / m2 MabTheran annon jälkeen laskimoon viikoittain 8 annoksen jälkeen 37 NHL -potilaalle, keskimääräinen C -arvo nousi jokaisen seuraavan infuusion yhteydessä, vaihdellen keskimäärin 243 mcg / ml (vaihteluväli: 16--582 mcg / ml) ensimmäisen infuusion jälkeen 550 mcg / ml (vaihteluväli) : 171 - 1177 mcg / ml) kahdeksannen infuusion jälkeen.
MabTheran farmakokineettinen profiili, kun sitä annettiin 6 infuusiona 375 mg / m2 yhdessä 6 CHOP -kemoterapiasyklin kanssa, oli samanlainen kuin yksin MabTheran kanssa.
Krooninen lymfaattinen leukemia
MabTheraa annettiin laskimonsisäisenä infuusiona, ja ensimmäisen syklin annos 375 mg / m2 nostettiin 500 mg / m2: ksi jokaista seuraavaa sykliä kohden, 5 annosta yhdessä fludarabiinin ja syklofosfamidin kanssa CLL -potilailla. Keskimääräinen Cmax (N = 15) viidennen 500 mg / m2 -infuusion jälkeen oli 408 mcg / ml (vaihteluväli 97-764 mcg / ml) ja keskimääräinen terminaalinen puoliintumisaika oli 32 päivää (vaihteluväli 14-62 päivää).
Nivelreuma
Kahden MabThera-infuusion jälkeen 1000 mg: n annoksella kahden viikon välein keskimääräinen terminaalinen puoliintumisaika oli 20,8 päivää (vaihteluväli 8,58--35,9 päivää), keskimääräinen systeeminen puhdistuma oli 0,23 l / vrk (vaihteluväli 0,091--0,67 / ja keskimääräinen vakaan tilan jakautumistilavuus oli 4,6 l (vaihteluväli 1,7-7,51 l). Samojen tietojen populaatio antoi samat systeemisen puhdistuman ja puoliintumisajan keskiarvot 0,26 l / vrk ja 20,4 vrk, vastaavasti. Populaatiofarmakokineettiset analyysit paljastivat, että BSA ja sukupuoli olivat merkittävimmät kovariantit selittämään farmakokineettisten parametrien yksilöiden välistä vaihtelua. BSA: n säätämisen jälkeen miespotilailla oli suurempi jakautumistilavuus ja nopeampi puhdistuma kuin naisilla. Sukupuoleen liittyviä farmakokineettisiä eroja ei pidetty kliinisesti merkityksellisinä, eikä annoksen muuttaminen ollut tarpeen. Farmakokineettisiä tietoja ei ole saatavilla potilaista, joilla on munuaisten tai maksan vajaatoiminta.
Rituksimabin farmakokinetiikkaa arvioitiin kahden laskimonsisäisen (i.v.) 500 mg: n ja 1000 mg: n annoksen jälkeen päivinä 1 ja 15 neljässä tutkimuksessa. Kaikissa näissä tutkimuksissa rituksimabin farmakokinetiikka oli suhteessa annokseen rajoitetulla annostusalueella.Rituksimabin keskimääräinen seerumin Cmax ensimmäisen infuusion jälkeen vaihteli välillä 157 - 171 mcg / ml 2 x 500 mg: n annoksella ja välillä 298 - 298 - 341 mcg / ml 2 x 1000 mg: n annoksella. Toisen infuusion jälkeen keskimääräinen Cmax -arvo oli välillä 183 - 198 mcg / ml 2 µ 500 mg: n annoksella ja 355 - 404 mcg / ml 2 annoksen kohdalla Lopullisen eliminaation keskimääräinen puoliintumisaika oli 15–16 päivää 2 x 500 mg: n annoksella ja 17–21 vuorokautta 2 annoksen ollessa 1000 mg. Cmax oli 16–19%, korkeampi toisen infuusion jälkeen verrattuna molempien annosten ensimmäiseen infuusioon.
Rituksimabin farmakokinetiikkaa arvioitiin kahden i.v. 500 mg ja 1000 mg toisen syklin uudelleenkäsittelyn jälkeen. Rituksimabin keskimääräinen seerumin Cmax ensimmäisen infuusion jälkeen vaihteli välillä 170 - 175 mcg / ml 2 x 500 mg: n annoksella ja 317 - 370 mcg / ml 2 x 1000 mg: n annoksella. Toisen infuusion jälkeen keskimääräinen Cmax -arvo oli 207 mcg / ml 2 x 500 mg: n annoksella ja 377 - 386 mcg / ml 2 x 1000 mg: n annoksella. Keskimääräinen terminaalinen eliminaation puoliintumisaika toisen infuusion jälkeen toisen syklin jälkeen oli 19 päivää 2 x 500 mg: n annoksella ja 21-22 päivää 2 x 1000 mg: n annoksella. Rituksimabin farmakokineettiset parametrit olivat vertailukelpoisia kahden hoitojakson aikana.
Farmakokineettiset parametrit niiden potilaiden populaatiossa, joiden vaste TNF-vasta-aineille oli riittämätön ja joille annettiin sama annostusohjelma (2 x 1000 mg laskimoon, kahden viikon välein), olivat samanlaiset keskimääräisen seerumin maksimipitoisuuden ollessa 369 mcg / ml ja life "keskimääräinen terminaali 19,2 päivää.
Granulomatoosi ja polyangiitti ja mikroskooppinen polyangiitti Perustuu populaatiofarmakokineettisiin analyyseihin, jotka koskevat tietoja 97 potilaasta, joilla oli polyangiitti- ja mikroskooppinen polyangiitti-granulomatoosi ja jotka saivat 375 mg / m2 MabTheraa kerran viikossa neljän viikon ajan, keskimääräinen eliminaation puoliintumisaika oli 23 päivää (vaihteluväli) 9-49 päivää).Rituksimabin keskimääräinen puhdistuma ja jakautumistilavuus olivat 0,313 l / vrk (vaihteluväli 0,116-0,726 l / vrk) ja 4,50 l (vaihteluväli 2,25-7,39 l). Rituksimabin farmakokineettiset parametrit näillä potilailla näyttävät samanlaisilta kuin nivelreumapotilailla.
05.3 Prekliiniset tiedot turvallisuudesta
Rituksimabi oli erittäin spesifinen B20 -solujen CD20 -antigeenille cynomolgus ne eivät paljastaneet muita vaikutuksia kuin odotettu farmakologinen B -solujen ehtyminen perifeerisestä verestä ja imusolmukekudoksesta.
Evoluutiotoksisuustutkimuksia tehtiin apinoilla cynomolgus annoksilla enintään 100 mg / kg (hoito raskauspäivinä 20-50) ja ovat osoittaneet, että rituksimabin aiheuttamaa sikiötoksisuutta ei ole todistettu. farmakologia, joka säilyi syntymän jälkeen ja johon liittyi IgG -tasojen lasku vastasyntyneillä eläimillä.B -solujen määrä palautui normaaliksi näillä eläimillä 6 kuukauden kuluessa syntymästä eikä heikentänyt immunisaatioreaktioita.
Normaaleja testejä mutageenisuuden tutkimiseksi ei ole suoritettu, koska nämä testit eivät ole merkityksellisiä tälle molekyylille. Rituksimabin karsinogeenisuuden määrittämiseksi ei ole tehty pitkäaikaisia eläinkokeita.
Rituksimabin vaikutuksia hedelmällisyyteen ei ole tehty erityisiä tutkimuksia. Yleensä apinoiden toksisuustutkimuksissacynomolgus haitallisia vaikutuksia miesten tai naisten lisääntymiselimiin ei havaittu.
06.0 FARMASEUTTISET TIEDOT
06.1 Apuaineet
Natriumsitraatti
Polysorbaatti 80
Natriumkloridia
Natriumhydroksidia
Suolahappo
Injektionesteisiin käytettävä vesi
06.2 Yhteensopimattomuus
MabTheran ja polyvinyylikloridi- tai polyeteenipussien tai infuusiolaitteiden välillä ei havaittu yhteensopimattomuutta.
06.3 Voimassaoloaika
30 kuukautta
Infuusioon valmistettu MabThera -liuos on fysikaalisesti ja kemiallisesti stabiili 24 tunnin ajan 2 ° C - 8 ° C: n lämpötilassa ja sen jälkeen 12 tunnin ajan huoneenlämmössä.
Mikrobiologisesta näkökulmasta valmistettu infuusioliuos on käytettävä välittömästi.Jos sitä ei käytetä välittömästi, säilytysaika ja -olosuhteet ennen käyttöä ovat käyttäjän vastuulla eivätkä yleensä ylity. 24 tuntia lämpötilassa 2 ° C - 8 ° C, ellei laimennusta ole tapahtunut kontrolloiduissa ja validoiduissa aseptisissa olosuhteissa.
06.4 Säilytys
Säilytä jääkaapissa (2 ° C - 8 ° C). Säilytä säiliö ulkopakkauksessa valolta suojaamiseksi.
Säilytysolosuhteet lääkevalmisteen laimentamisen jälkeen, ks. Kohta 6.3.
06.5 Välipakkauksen luonne ja pakkauksen sisältö
Kirkkaat tyypin I lasipullot, joissa on butyylikumitulppa ja jotka sisältävät 100 mg rituksimabia 10 ml: ssa. Pakkauksessa 2 injektiopulloa.
06.6 Käyttö- ja käsittelyohjeet
MabThera toimitetaan steriileissä, säilöntäaineettomissa, ei-pyrogeenisissä kertakäyttöisissä injektiopulloissa.
Imuroi tarvittava määrä MabTheraa steriileissä olosuhteissa ja laimenna laskettuun pitoisuuteen 1-4 mg / ml rituksimabia infuusiopussiin, joka sisältää steriiliä ei-pyrogeenistä 9 mg / ml (0,9%) natriumkloridiliuosta. ) tai 5% D-glukoosia vedessä. Liuos sekoitetaan kääntämällä pussi hitaasti ylösalaisin vaahtoamisen välttämiseksi. On huolehdittava valmistettujen liuosten steriiliyden varmistamisesta. Koska lääkevalmiste ei sisällä antimikrobisia säilöntäaineita tai bakteriostaattisia aineita, on noudatettava aseptisia tekniikoita. Parenteraaliset lääkkeet on tarkistettava silmämääräisesti hiukkasten tai värimuutosten varalta ennen antamista.
Käyttämätön lääke ja tästä lääkkeestä peräisin oleva jäte on hävitettävä paikallisten määräysten mukaisesti.
07.0 MYYNTILUVAN HALTIJA
Roche Registration Limited
6 Falcon Way
Shire Park
Welwynin puutarhakaupunki
AL7 1TW
Iso -Britannia
08.0 MYYNTILUVAN NUMERO
EU/1/98/067/001
033315019
09.0 MYYNTILUVAN TAI UUDISTAMISPÄIVÄMÄÄRÄ
Myyntiluvan myöntämisen päivämäärä: 2. kesäkuuta 1998
Viimeisimmän uudistamisen päivämäärä: 2. kesäkuuta 2008
10.0 TEKSTIN MUUTTAMISPÄIVÄMÄÄRÄ
11.0 RADIOHUOLLOJEN TÄYDELLISET TIEDOT SISÄISESTÄ SÄTEILYN DOSIMETRIAA
12.0 RADIOHUOLLOILLE LISÄTIETOA KOSKEVAT LISÄOHJEET ALKUPERÄISTÄ VALMISTELUA JA LAADUNVALVONTAA